1 . 现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为
的电子式为___________ 。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)某同学推断 元素基态原子的核外电子轨道表示式为
元素基态原子的核外电子轨道表示式为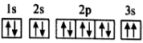 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了___________ ,该元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ ,实验室用一种黄色溶液检验 时产生蓝色沉淀该反应的离子方程式为
时产生蓝色沉淀该反应的离子方程式为___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子数少1个 能级电子数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,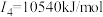 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为
的电子式为(2)
 元素的原子核外共有
元素的原子核外共有(3)某同学推断
 元素基态原子的核外电子轨道表示式为
元素基态原子的核外电子轨道表示式为 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中 时产生蓝色沉淀该反应的离子方程式为
时产生蓝色沉淀该反应的离子方程式为
您最近一年使用:0次
2 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。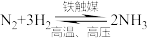
(1)基态氢原子中,核外电子的电子云轮廓图形状为_______
(2)自然界中的复元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为_______
② 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
分子中,与N原子相连的H显正电性。N、H电负性大小顺序为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、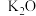 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是_______ 。
②比较 、
、 第一电高能的大小:
第一电高能的大小:_______
③表中的数据从上到下是纳、镁、铝逐级失去电子的电离能。
为什么原子的逐级电高能越来越大?______ ;结合数据说明为什么 的常见化合价为
的常见化合价为 价:请解释之:
价:请解释之:_______ 。
(4)目前合成氨通常采用的压强为 温度为
温度为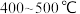 ,十分耗能。我国科研人员研制出了“
,十分耗能。我国科研人员研制出了“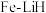 ”等催化剂,温度、压强分别降到了350℃、
”等催化剂,温度、压强分别降到了350℃、 ,这是近年来合成纸反应研究中的重要突破。
,这是近年来合成纸反应研究中的重要突破。
①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
②比较 与
与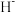 的半径大小关系:
的半径大小关系:
_______ 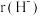 (填“>”或“<”)。
(填“>”或“<”)。
(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的复元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②
 分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
分子中,与N原子相连的H显正电性。N、H电负性大小顺序为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、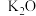 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较
 、
、 第一电高能的大小:
第一电高能的大小:③表中的数据从上到下是纳、镁、铝逐级失去电子的电离能。
| 元素 |  |  |  |
电离能(kJ mol-1) mol-1) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
 的常见化合价为
的常见化合价为 价:请解释之:
价:请解释之:(4)目前合成氨通常采用的压强为
 温度为
温度为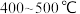 ,十分耗能。我国科研人员研制出了“
,十分耗能。我国科研人员研制出了“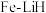 ”等催化剂,温度、压强分别降到了350℃、
”等催化剂,温度、压强分别降到了350℃、 ,这是近年来合成纸反应研究中的重要突破。
,这是近年来合成纸反应研究中的重要突破。①基态
 原子的核外电子排布式为
原子的核外电子排布式为②比较
 与
与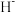 的半径大小关系:
的半径大小关系:
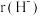 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
2021-01-24更新
|
364次组卷
|
4卷引用:专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)
(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修2)2月刊 (同步课堂必刷题)(已下线)1.2 原子结构与元素的性质(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)北京市朝阳区2020-2021学年高二上学期期末质量检测化学试题



