名校
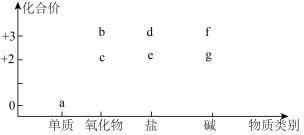
1 . 铁及其化合物在生活、生产中应用非常广泛,铁的“价-类”二维图如图所示,请回答下列问题:___________ 。
(2)写出检验某未知溶液中是否含有d的阳离子的操作及现象:___________ 。
(3)若d、e均为氯盐,则e中含有少量杂质d,可用___________ (填试剂名称)来除杂,发生反应的离子方程式为___________ 。
(4)若e为硫酸盐,则向e的溶液中滴加NaOH溶液,可观察到的现象为___________ 。g在潮湿的空气中生成f的化学方程式为___________ 。
(5)利用铝热反应制备a,该反应中,铝作___________ (填“氧化剂”“还原剂”或“催化剂”),下列过程中,与该反应的能量变化相符的是___________ (填标号)。
A.甲烷的燃烧 B.石灰石在高温下煅烧
C.盐酸中加入镁粉 D.水分子的H—O键断裂
(6)常温下,可用a制得的容器盛放浓硫酸,原因是___________ 。
(2)写出检验某未知溶液中是否含有d的阳离子的操作及现象:
(3)若d、e均为氯盐,则e中含有少量杂质d,可用
(4)若e为硫酸盐,则向e的溶液中滴加NaOH溶液,可观察到的现象为
(5)利用铝热反应制备a,该反应中,铝作
A.甲烷的燃烧 B.石灰石在高温下煅烧
C.盐酸中加入镁粉 D.水分子的H—O键断裂
(6)常温下,可用a制得的容器盛放浓硫酸,原因是
您最近一年使用:0次
2024-08-14更新
|
97次组卷
|
4卷引用:3.1.2 铁的重要化合物(提高)
名校
解题方法
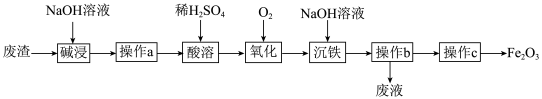
2 . 某研究小组以工厂废渣Fe3O4、Al2O3为原料制取Fe2O3工艺流程如下图。回答下列问题:___________ 。
(2)“操作a”中用到的玻璃仪器有烧杯、___________ 、___________ 。
(3)“氧化”的目的是___________ 。
(4)“氧化”时反应的离子方程式为___________ 。若用H2O2代替O2,其离子方程式为___________ 。
(5)“操作c”发生反应的化学方程式为___________ 。
(2)“操作a”中用到的玻璃仪器有烧杯、
(3)“氧化”的目的是
(4)“氧化”时反应的离子方程式为
(5)“操作c”发生反应的化学方程式为
您最近一年使用:0次
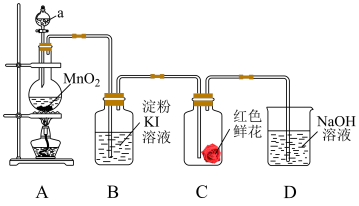
3 . 下图是二氧化锰和浓盐酸反应制取氯气、并验证其部分化学性质的实验装置,请回答下列问题:_____ 色气体。
(2)装置 中,仪器
中,仪器 中盛装的试剂是
中盛装的试剂是_____ (填“浓硫酸”或“浓盐酸”)。
(3)当有少量氯气通过后,可观察到装置 中溶液变成
中溶液变成____ 色。
(4)当氯气持续通过时,装置 中红色鲜花颜色
中红色鲜花颜色______ 。
(5)装置 的作用是
的作用是_____ 。
(2)装置
 中,仪器
中,仪器 中盛装的试剂是
中盛装的试剂是(3)当有少量氯气通过后,可观察到装置
 中溶液变成
中溶液变成(4)当氯气持续通过时,装置
 中红色鲜花颜色
中红色鲜花颜色(5)装置
 的作用是
的作用是
您最近一年使用:0次
解题方法
4 . 实验室用右图装置,制备并收集纯净、干燥的Cl2,其反应原理是: MnO2 + 4HCl(浓) MnCl2 + C12↑ + 2H2O,
MnCl2 + C12↑ + 2H2O,
(1)装置中,盛放MnO2的仪器名称是__________ ;盛放浓盐酸的仪器名称是__________ 。
(2)制得的Cl2中可能会混有的杂质气体有________ ,饱和食盐水的作用是________________ 、浓硫酸的作用是________________ ;NaOH溶液的作用是__________ 。
 MnCl2 + C12↑ + 2H2O,
MnCl2 + C12↑ + 2H2O, 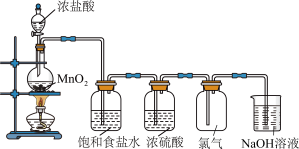
(1)装置中,盛放MnO2的仪器名称是
(2)制得的Cl2中可能会混有的杂质气体有
您最近一年使用:0次
2024-06-25更新
|
212次组卷
|
2卷引用:2.2.2 氯气的实验室制法(基础)
解题方法
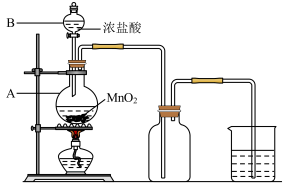
5 . 氯气的实验室制备、收集及尾气处理装置如下图所示,请回答下列问题:____________ 。如转移电子物质的量是 则被氧化的
则被氧化的 的物质的量是
的物质的量是_________  。
。
(2)图中仪器A的名称是__________ ;仪器B的名称是__________ 。
(3)氯气是一种__________ 色、有毒的气体。
(4)用向上排空气法收集氯气的原因是:氯气的密度比空气的密度__________ (选填“大”或“小”)。
(5)氯气的水溶液呈__________ (选填“酸”或“碱”)性。
(6)氯气有毒,烧杯中的溶液可用于吸收氯气,该尾气处理的离子方程式为______________ 。
 则被氧化的
则被氧化的 的物质的量是
的物质的量是 。
。(2)图中仪器A的名称是
(3)氯气是一种
(4)用向上排空气法收集氯气的原因是:氯气的密度比空气的密度
(5)氯气的水溶液呈
(6)氯气有毒,烧杯中的溶液可用于吸收氯气,该尾气处理的离子方程式为
您最近一年使用:0次
2024-06-25更新
|
115次组卷
|
2卷引用:2.2.2 氯气的实验室制法(提高)
解题方法
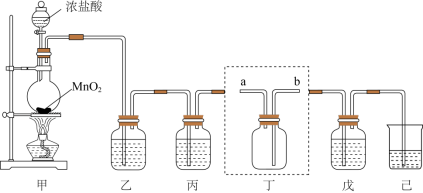
6 . 氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:___________ ,盛装浓盐酸的仪器的名称为____________ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为______________ (填a或b);装置乙和丙盛装的试剂分别是____________ 。(填名称)
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的化学方程式为____________ ,有同学认为装置己还有一个作用,该作用为______ ,发挥该作用进___________ (填“能”或“不能”)用澄清石灰水代替。
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为_____________ ;漂白粉长时间暴露在空气中容易发生变质的原因为_____________ (结合化学方程式说明)。
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的化学方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
您最近一年使用:0次
2024-06-22更新
|
99次组卷
|
2卷引用:2.2.2 氯气的实验室制法(提高)
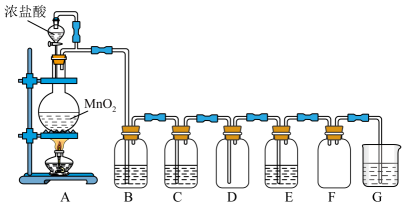
7 . 二氧化锰与浓盐酸混合加热可得到氯气,如图是制取氯气并探究化学性质的装置图。___________ 。
(2)若要得到纯净干燥的气体,则装置B盛放的试剂是___________ ;作用是___________ ;装置C盛放的试剂是___________ ;作用是___________ 。
(3)E中若装有淀粉碘化钾溶液,能观察到的实验现象是:___________ 。
(4)氯气可用___________ 法收集,请说明理由:___________ 。
(5)F装置的作用是___________ ;
(6)G中发生的化学反应方程式为:___________ 。
(2)若要得到纯净干燥的气体,则装置B盛放的试剂是
(3)E中若装有淀粉碘化钾溶液,能观察到的实验现象是:
(4)氯气可用
(5)F装置的作用是
(6)G中发生的化学反应方程式为:
您最近一年使用:0次
2024-06-20更新
|
177次组卷
|
3卷引用:2.2.2 氯气的实验室制法(提高)
名校
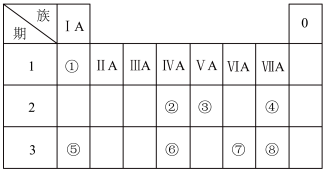
8 . 下表是元素周期表的一部分,表中所列的每个序号分别代表某一元素。___________ 。⑨元素的原子结构示意图为___________ 。
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是___________ (填元素符号);这五种元素分别形成的简单离子中离子半径最小的是___________ (填离子符号)。
(3)手机、电脑、电视屏幕使用的都是含铟(In)的导电玻璃。已知In元素与元素⑥同主族,下列关于In的说法中正确的是___________ (填字母)。
a.最外层有5个电子
b.最高价氧化物对应的水化物碱性比⑥强
c.失电子能力比⑥弱
d.可与稀硫酸反应产生氢气
(4)元素①和⑧的单质化合形成的化合物中①元素的化合价为___________ ;该化合物能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为___________ 。
(5)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
(6)元素④和⑥相比,金属性较强的是___________ (填元素符号),下列能证明这一事实的有___________ (填字母)。
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低

(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是
(3)手机、电脑、电视屏幕使用的都是含铟(In)的导电玻璃。已知In元素与元素⑥同主族,下列关于In的说法中正确的是
a.最外层有5个电子
b.最高价氧化物对应的水化物碱性比⑥强
c.失电子能力比⑥弱
d.可与稀硫酸反应产生氢气
(4)元素①和⑧的单质化合形成的化合物中①元素的化合价为
(5)表中元素⑦和⑩的最高价氧化物对应水化物的酸性最强的是
(6)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低
B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强
D.④单质的熔点比⑥单质的低
您最近一年使用:0次
2024-06-18更新
|
66次组卷
|
2卷引用:4.2.2 元素周期表和元素周期律的应用(巩固)
名校
解题方法
9 . 元素周期表的一部分如图,表中每一序号分别代表一种元素。回答下列问题。
(1)⑧元素的简单离子的结构示意图为___________ ,⑨元素在周期表中的位置为___________ 。
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为___________ 。
(3)⑤元素的焰色为___________ 色,⑤元素最高价氧化物对应的水化物溶液与⑥元素形成的单质反应的离子方程式为___________ 。
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为___________ (填化学式);②元素、③元素、④元素的最简单氢化物稳定性由强到弱的顺序为___________ 。
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为___________ (填化学式)。
| ① | ||||||||||
| ② | ③ | ④ | ||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||||
| ⑨ | …… | |||||||||
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为
(3)⑤元素的焰色为
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为
您最近一年使用:0次
2024-06-11更新
|
70次组卷
|
2卷引用:4.2.2 元素周期表和元素周期律的应用(提高)
名校
解题方法
10 . 下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①~⑧号元素回答下列问题。________ ,它的沸点比PH3高,原因是________________ ;
(2)测定文物年代需要利用元素②的一种中子数为8的核素,该核素符号可表示为________ ;
(3)元素①和氧元素形成的18电子化合物的名称是:________ ,该化合物中含有的化学键有________ (填“离子键、极性键、非极性键”);
(4)元素④、⑤、⑧中,原子半径最大的是________ (填元素符号),离子半径最大的是________ (填化学式)。
(5)可以证明元素⑧比元素⑦非金属性强的一个化学反应方程式是:________ 。
(2)测定文物年代需要利用元素②的一种中子数为8的核素,该核素符号可表示为
(3)元素①和氧元素形成的18电子化合物的名称是:
(4)元素④、⑤、⑧中,原子半径最大的是
(5)可以证明元素⑧比元素⑦非金属性强的一个化学反应方程式是:
您最近一年使用:0次
2024-04-24更新
|
94次组卷
|
2卷引用:4.3.2 共价键(提高)



