名校
解题方法
1 . 根据元素周期律回答下列问题:
(1)B(硼元素)在元素周期表中与 同主族,已知:
同主族,已知: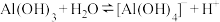 ,则
,则 的电离方程式为
的电离方程式为___________________________________ 。酸性:
__________  (填“>”或“<”)
(填“>”或“<”)
(2) 和镁粉混合点燃可得单质B,该反应的化学方程式为
和镁粉混合点燃可得单质B,该反应的化学方程式为_________________ 。
(3) 可用于生产储氢材料
可用于生产储氢材料 。
。 具有强还原性。在碱性条件下,
具有强还原性。在碱性条件下, 与
与 溶液反应可得
溶液反应可得 和
和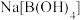 ,其中H元素由
,其中H元素由 价升高为
价升高为 价。
价。
①写出基态 核外电子排布式
核外电子排布式______________ ; 基态核外电子排布图
基态核外电子排布图_________________
②基态B原子中能量最高的是__________ 电子,其电子云在空间呈现____________ 形
③写出碱性条件下, 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:__________________
(1)B(硼元素)在元素周期表中与
 同主族,已知:
同主族,已知: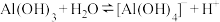 ,则
,则 的电离方程式为
的电离方程式为
 (填“>”或“<”)
(填“>”或“<”)(2)
 和镁粉混合点燃可得单质B,该反应的化学方程式为
和镁粉混合点燃可得单质B,该反应的化学方程式为(3)
 可用于生产储氢材料
可用于生产储氢材料 。
。 具有强还原性。在碱性条件下,
具有强还原性。在碱性条件下, 与
与 溶液反应可得
溶液反应可得 和
和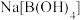 ,其中H元素由
,其中H元素由 价升高为
价升高为 价。
价。①写出基态
 核外电子排布式
核外电子排布式 基态核外电子排布图
基态核外电子排布图②基态B原子中能量最高的是
③写出碱性条件下,
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近半年使用:0次
名校
解题方法
2 . 现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要肥料。
(1)A的原子最外层共有___ 种不同运动状态的电子,该原子共有___ 种不同能量的电子,能量最高的电子占有___ 个轨道,其电子云形状为____ 。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:_____ 。
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式____ 。
(4)元素A与元素D相比,非金属性较强的是____ (用元素符号表示),下列表述中能表明这一事实的是____ 。
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因_____ 。
(5)C原子的原子结构示意图:_____ ,C的氢化物固态时属于____ 晶体。
(1)A的原子最外层共有
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式
(4)元素A与元素D相比,非金属性较强的是
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因
(5)C原子的原子结构示意图:
您最近半年使用:0次
解题方法
3 . 现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要的肥料。
(1)A的原子最外层共有__________ 种不同运动状态的电子,该层电子亚层有__________ 种。描述集气瓶中足量的A的氢化物与其低价态氧化物混合后,充分反应的实验现象:_____________________ 。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,其化学式是_______ 。写出该化合物在实验室制备乙酸乙酯时所起的作用:________________ 。
(3)B与C元素形成带一个单位正电荷的离子,写成该微粒的电子式_____ 。写出实验室检验溶液中该离子的简单实验方案:_______________ 。
(4)元素A与元素D相比,非金属性较强的是____________ (用元素符号表示),下列表述中能表明这一事实的是______
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
(5)C的氢化物固态时属于__________ 晶体,该氢化物与A的最高价氧化物水化物反应的化学方程式是_______________ 。
(1)A的原子最外层共有
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,其化学式是
(3)B与C元素形成带一个单位正电荷的离子,写成该微粒的电子式
(4)元素A与元素D相比,非金属性较强的是
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
(5)C的氢化物固态时属于
您最近半年使用:0次



