1 . 下列对电子排布式或轨道表示式书写的评价错误的是
| A.若Mn元素的基态原子核外电子排布式为1s22s22p63s23p63d7 ,则违反了构造原理 |
B.若基态硫原子的价层电子轨道表示式为 ,则违反了泡利原理 ,则违反了泡利原理 |
C.基态氮原子的核外电子轨道表示式为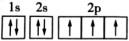 ,符合洪特规则和泡利原理 ,符合洪特规则和泡利原理 |
D.电子排布式(   )违反了洪特规则 )违反了洪特规则 |
您最近一年使用:0次
解题方法
2 . 下列有关原子核外电子排布的说法错误的是
A. 的电子排布式写成 的电子排布式写成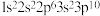 ,违反了能量最低原理 ,违反了能量最低原理 |
B.基态: 的电子排布式写成 的电子排布式写成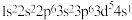 ,是正确的 ,是正确的 |
C.O原子的电子轨道表示式写成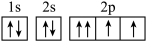 ,违反了泡利不相容原理 ,违反了泡利不相容原理 |
D.Si原子的价电子轨道表示式写成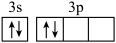 ,违反了洪特规则 ,违反了洪特规则 |
您最近一年使用:0次
3 . 某同学将氧原子的核外电子轨道表示式写成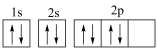 ,他违背了
,他违背了
| A.洪特规则 | B.泡利不相容原理 |
| C.能量守恒原理 | D.能量最低原理 |
您最近一年使用:0次
2024-03-23更新
|
328次组卷
|
3卷引用:河北省邢台市五岳联盟2023-2024学年高二下学期3月份月考化学试题
4 . 同一轨道最多容纳2个自旋方向____ 的电子(填:相同或相反)。
您最近一年使用:0次
5 . 泡利原理
在一个原子轨道里最多只能容纳_______ 个电子,而且它们的自旋状态_______ ,这个原理称为泡利原理。
在一个原子轨道里最多只能容纳
您最近一年使用:0次
6 . 若将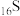 原子的电子排布式写成
原子的电子排布式写成 ,则违背了
,则违背了
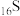 原子的电子排布式写成
原子的电子排布式写成 ,则违背了
,则违背了| A.能量守恒原理 | B.泡利不相容原理 | C.能量最低原理 | D.洪特规则 |
您最近一年使用:0次
2024-02-13更新
|
352次组卷
|
2卷引用:贵州省黔东南州2023-2024学年高二上学期 期末化学试题
23-24高二·全国·假期作业
7 . 每个电子层上最多容纳2n2个电子是由泡利不相容原理决定的。( )
您最近一年使用:0次
8 . 基态原子的核外电子排布规律
原则一:能量最低原理
基态原子核外电子总是尽可能先排布在能量___________ 的轨道上,然后___________ 依次排布在能量较高的轨道上。也可以说,核外电子遵循的排布规则使整个原子的能量处于___________ 状态。
原则二:泡利不相容原理
一个原子轨道中最多只能容纳___________ 电子,且这两个电子的自旋状态___________ 。
【方法指导】核外电子排布式的表示方法
(1)电子排布式:对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同,使体系的总能量达到最低。
基态锂原子电子排布式:___________ ;
基态氯原子电子排布式:___________ ;
(2)轨道表示式:用方框表示一个原子轨道,用箭头“↑”或“↓”来区别自旋状态不同的电子。
基态锂原子轨道表示式:___________ ;
基态氯原子轨道表示式:___________ ;
原则三:洪特规则
对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能_________ 并且_________ 相同,使体系的总能量达到___________ 。
【迁移应用】分别写出1~18号元素基态原子的电子排布式和轨道表示式。
【归纳总结】构造原理
随着原子序数的递增,基态原子的“外层电子”按顺序依次排布在___________ 等原子轨道上。
原则一:能量最低原理
基态原子核外电子总是尽可能先排布在能量
原则二:泡利不相容原理
一个原子轨道中最多只能容纳
【方法指导】核外电子排布式的表示方法
(1)电子排布式:对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同,使体系的总能量达到最低。
基态锂原子电子排布式:
基态氯原子电子排布式:
(2)轨道表示式:用方框表示一个原子轨道,用箭头“↑”或“↓”来区别自旋状态不同的电子。
基态锂原子轨道表示式:
基态氯原子轨道表示式:
原则三:洪特规则
对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能
【迁移应用】分别写出1~18号元素基态原子的电子排布式和轨道表示式。
【归纳总结】构造原理
随着原子序数的递增,基态原子的“外层电子”按顺序依次排布在
您最近一年使用:0次
9 . 在d轨道中电子排布成 ,而不排成
,而不排成 ,其直接的根据是
,其直接的根据是
 ,而不排成
,而不排成 ,其直接的根据是
,其直接的根据是| A.能量最低原理 | B.泡利不相容原理 |
| C.原子轨道能量顺序 | D.洪特规则 |
您最近一年使用:0次
10 . 泡利不相容原理
每个原子轨道上最多容纳___________ 个自旋状态不同的电子。
每个原子轨道上最多容纳
您最近一年使用:0次



