名校
解题方法
1 . 如图所示,NaCl是一种重要的化工原料,可以制备一系列物质。以下是钠法(液氨法)制备NaN3的工艺流程:

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:____ 。
(2)用电子式表示NH3分子的形成过程____ 。
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式____ 。
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为____ ( 被氧化为N2)。
被氧化为N2)。
(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。
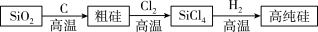
①硅元素位于周期表第____ 周期____ 族。
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于____ 晶体,SiCl4晶体微粒间的作用力为____ 。

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:
(2)用电子式表示NH3分子的形成过程
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为
 被氧化为N2)。
被氧化为N2)。(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。

①硅元素位于周期表第
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于
您最近一年使用:0次



