1 . 硫酸制备是工业重要课题
I.历史上曾用绿矾(FeSO4·H2O)制备硫酸。高温条件下FeSO4发生如下分解反应:2FeSO4 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
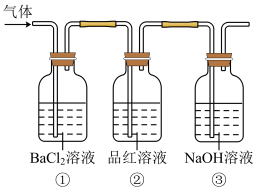
(1)装置①能检验出的气体产物是_______ ,装置②能检验出的气体产物是_______ 。
(2)如果把①和②互换位置对该实验是否有影响:_______ (填是或否)。
II.现代硫酸工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:

(3)接触室中的发生化学方程式_______ ,吸收环节中使用_______ 吸收SO3。
III.某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下实验。取标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。试回答:
(4)通过足量溴水的离子方程式为:_______ 。
(5)计算该空气样品中二氧化硫的体积分数是_______ 。
I.历史上曾用绿矾(FeSO4·H2O)制备硫酸。高温条件下FeSO4发生如下分解反应:2FeSO4
 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的气体产物,进行如下实验:将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
(1)装置①能检验出的气体产物是
(2)如果把①和②互换位置对该实验是否有影响:
II.现代硫酸工业上用黄铁矿(FeS2)为原料制备硫酸的流程如图:

(3)接触室中的发生化学方程式
III.某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下实验。取标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。试回答:
(4)通过足量溴水的离子方程式为:
(5)计算该空气样品中二氧化硫的体积分数是
您最近一年使用:0次
2022-09-01更新
|
358次组卷
|
3卷引用:新疆石河子第一中学2021-2022学年高一下学期4月月考化学试题



