解题方法
1 . 某小组探究铜与浓硝酸的反应。
【实验】
(1)铜与浓硝酸反应的化学方程式是_______ ,氢氧化钠溶液的作用是_______ 。
小组同学继续探究溶液呈鲜草绿色的原因。
甲同学提出猜想:因为气体溶解后,溶液颜色和气体颜色叠加形成鲜草绿色,设计实1-1及1-2进行验证。
实验1-1:取 反应后混合液于一支试管内,按一定的气体流速将
反应后混合液于一支试管内,按一定的气体流速将 和
和 混合气体通入,有大量红棕色气体逸出,约
混合气体通入,有大量红棕色气体逸出,约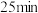 后溶液转为蓝色。
后溶液转为蓝色。
实验1-2:取 反应后混合液于另一支试管内,按与实验1-1中相同的气体流速将空气通入,有大量红棕色气体逸出,约
反应后混合液于另一支试管内,按与实验1-1中相同的气体流速将空气通入,有大量红棕色气体逸出,约 后溶液转为蓝色
后溶液转为蓝色
(2)乙同学根据以上2个实验的现象证明甲同学的猜想不成立,依据的现象是_______ 。
【查阅资料】
i.铜与浓硝酸反应,开始生成的 溶于水生成
溶于水生成 ,
, 与Cu2+反应生成绿色的化合物;
与Cu2+反应生成绿色的化合物;
ii.一定条件下,Cu2+既可以表现氧化性,又可以表现还原性;
iii.尿素 具有温和的抗氧化性;
具有温和的抗氧化性;
iv.金属和浓硝酸反应过程中有 生成,可大大加快金属与浓硝酸反应的速率。
生成,可大大加快金属与浓硝酸反应的速率。
其原理为:
第一步: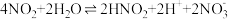
第二步: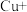 …
…
第三步:
【设计实验】
分别向四支试管内依次加入下列试剂后,同时插入铜丝并记录实验现象。
(3)补全iv中原理的第二步反应:_______ 。
(4)实验2-3中没有绿色出现的原因是_______ 。
(5)因为发生化学反应:_______ 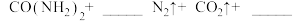 ,因此实验2-4中反应速率较慢。
,因此实验2-4中反应速率较慢。
(6)解释实验1-1和1-2的现象差异原因_______ 。
【实验】
| 实验装置(夹特仪器略) | 实验现象 |
 | 铜片溶解,最初反应较慢,随后加快,有大量红棕色气体放出,反应后试管中溶液呈现鲜草绿色 |
小组同学继续探究溶液呈鲜草绿色的原因。
甲同学提出猜想:因为气体溶解后,溶液颜色和气体颜色叠加形成鲜草绿色,设计实1-1及1-2进行验证。
实验1-1:取
 反应后混合液于一支试管内,按一定的气体流速将
反应后混合液于一支试管内,按一定的气体流速将 和
和 混合气体通入,有大量红棕色气体逸出,约
混合气体通入,有大量红棕色气体逸出,约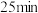 后溶液转为蓝色。
后溶液转为蓝色。实验1-2:取
 反应后混合液于另一支试管内,按与实验1-1中相同的气体流速将空气通入,有大量红棕色气体逸出,约
反应后混合液于另一支试管内,按与实验1-1中相同的气体流速将空气通入,有大量红棕色气体逸出,约 后溶液转为蓝色
后溶液转为蓝色(2)乙同学根据以上2个实验的现象证明甲同学的猜想不成立,依据的现象是
【查阅资料】
i.铜与浓硝酸反应,开始生成的
 溶于水生成
溶于水生成 ,
, 与Cu2+反应生成绿色的化合物;
与Cu2+反应生成绿色的化合物;ii.一定条件下,Cu2+既可以表现氧化性,又可以表现还原性;
iii.尿素
 具有温和的抗氧化性;
具有温和的抗氧化性;iv.金属和浓硝酸反应过程中有
 生成,可大大加快金属与浓硝酸反应的速率。
生成,可大大加快金属与浓硝酸反应的速率。其原理为:
第一步:
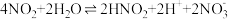
第二步:
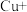 …
…第三步:

【设计实验】
分别向四支试管内依次加入下列试剂后,同时插入铜丝并记录实验现象。
| 编号 | 浓硝酸 | 蒸馏水/滴 | 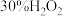 /滴 /滴 |  尿素溶液/滴 尿素溶液/滴 | 现象 |
| 2-1 | 1 | 0 | 0 | 0 | 快速反应,异常剧烈,溶液为鲜草绿色 |
| 2-2 | 1 | 3 | 0 | 0 | 快速反应,异常剧烈,溶液为鲜草绿色 |
| 2-3 | 1 | 0 | 3 | 0 | 反应较慢,溶液为蓝色,没有绿色出现 |
| 2-4 | 1 | 0 | 0 | 3 | 反应较慢,溶液为蓝色,没有绿色出现 |
(4)实验2-3中没有绿色出现的原因是
(5)因为发生化学反应:
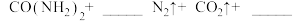 ,因此实验2-4中反应速率较慢。
,因此实验2-4中反应速率较慢。(6)解释实验1-1和1-2的现象差异原因
您最近一年使用:0次
名校
解题方法
2 . 某小组探究 溶液对氯水漂白性的影响,装置如下图所示。
溶液对氯水漂白性的影响,装置如下图所示。
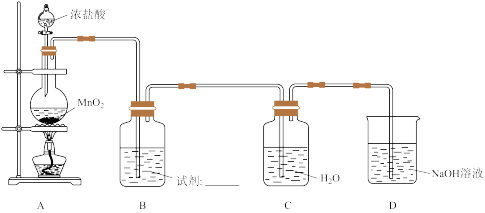
(1)A中反应的离子方程式是_______ 。
(2)B中试剂是_______ 。
(3)用化学方程式表示D中 溶液的作用
溶液的作用_______ 。
(4)取C中氯水,进行实验:向溶液a中加入 氯水。
氯水。
Ⅱ中品红褪色慢,推测可能发生了 ,导致Ⅱ中
,导致Ⅱ中 减少。分析沉淀中含
减少。分析沉淀中含 ,探究如下:将沉淀滤出、洗涤。向沉淀中加入盐酸,产生黄绿色气体。
,探究如下:将沉淀滤出、洗涤。向沉淀中加入盐酸,产生黄绿色气体。
①说明 具有
具有_______ 性。
②产生黄绿色气体的化学方程式是_______ 。
③实验发现,沉淀经几次洗涤后,加入盐酸,不再产生黄绿色气体。
(5)Ⅱ中溶液仍具有漂白性,可能是所加 溶液不足量。
溶液不足量。
①取Ⅱ中上层清液,_______ ,证实所加 溶液过量。
溶液过量。
②Ⅱ中溶液仍具有漂白性的原因是_______ 。
(6)进一步证实Ⅱ中所得沉淀中含 :向沉淀中加入饱和
:向沉淀中加入饱和 溶液,静置、过滤,滤渣、滤液备用。
溶液,静置、过滤,滤渣、滤液备用。
资料: 在一定条件下可转化为
在一定条件下可转化为
①实验证实滤渣中无 。
。
②取滤液,_______ 。
以上实验说明,所得沉淀中含 。
。
 溶液对氯水漂白性的影响,装置如下图所示。
溶液对氯水漂白性的影响,装置如下图所示。
(1)A中反应的离子方程式是
(2)B中试剂是
(3)用化学方程式表示D中
 溶液的作用
溶液的作用(4)取C中氯水,进行实验:向溶液a中加入
 氯水。
氯水。| 序号 | 溶液a | 现象 |
| Ⅰ | 1滴品红 | 几秒后品红褪色 |
| Ⅱ | 1滴品红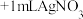 溶液 溶液 | 几分钟后品红褪色,产生白色沉淀 |
 ,导致Ⅱ中
,导致Ⅱ中 减少。分析沉淀中含
减少。分析沉淀中含 ,探究如下:将沉淀滤出、洗涤。向沉淀中加入盐酸,产生黄绿色气体。
,探究如下:将沉淀滤出、洗涤。向沉淀中加入盐酸,产生黄绿色气体。①说明
 具有
具有②产生黄绿色气体的化学方程式是
③实验发现,沉淀经几次洗涤后,加入盐酸,不再产生黄绿色气体。
(5)Ⅱ中溶液仍具有漂白性,可能是所加
 溶液不足量。
溶液不足量。①取Ⅱ中上层清液,
 溶液过量。
溶液过量。②Ⅱ中溶液仍具有漂白性的原因是
(6)进一步证实Ⅱ中所得沉淀中含
 :向沉淀中加入饱和
:向沉淀中加入饱和 溶液,静置、过滤,滤渣、滤液备用。
溶液,静置、过滤,滤渣、滤液备用。资料:
 在一定条件下可转化为
在一定条件下可转化为
①实验证实滤渣中无
 。
。②取滤液,
以上实验说明,所得沉淀中含
 。
。
您最近一年使用:0次
2023-01-05更新
|
751次组卷
|
2卷引用:北京市铁路第二中学2023-2024学年高一上学期期中考试化学试题
3 . 某同学看到“利用零价铁还原 脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与
脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与 溶液的反应。实验过程如下:
溶液的反应。实验过程如下:

i.打开弹簧夹,缓慢通入 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行;
氛围中进行;
ii.加入pH 已调至2.5 的
 酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在 、
、 和
和 。
。
(1)通入 并保持后续反应均在
并保持后续反应均在 氛围中进行的实验目的是
氛围中进行的实验目的是_________ 。
(2)白色物质是_________ ,用化学方程式解释其变为红褐色的原因:_________ 。
(3)用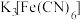 检验滤液中
检验滤液中 的实验方案是
的实验方案是_________ 。
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是_________ 。
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳。他用上述 溶液继续设计如下实验,探究碳粉的作用。
溶液继续设计如下实验,探究碳粉的作用。
实验操作①处填:_______ ,现象及结论②处填________ 。
关于碳粉的作用,还可以提出的假设是_______ 。
 脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与
脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与 溶液的反应。实验过程如下:
溶液的反应。实验过程如下:
i.打开弹簧夹,缓慢通入
 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行;
氛围中进行;ii.加入pH 已调至2.5 的

 酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在
 、
、 和
和 。
。(1)通入
 并保持后续反应均在
并保持后续反应均在 氛围中进行的实验目的是
氛围中进行的实验目的是(2)白色物质是
(3)用
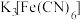 检验滤液中
检验滤液中 的实验方案是
的实验方案是(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳。他用上述
 溶液继续设计如下实验,探究碳粉的作用。
溶液继续设计如下实验,探究碳粉的作用。| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原 剂,脱除硝酸盐 | 向烧杯中加入___①____,一段 时间后,测定烧杯中  的 的浓度 |  浓度无明显变化,说 浓度无明显变化,说明假设1不成立 |
| 假设2:碳粉、铁粉形成 无数个微小的原电池,促 进了硝酸盐的脱除 | 按下图所示组装实验装置,一 段时间后,测定  浓度 浓度 | ____②____,说明假设2 成立 |
关于碳粉的作用,还可以提出的假设是
您最近一年使用:0次
4 . 某小组同学为比较酸性条件下NO3-、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
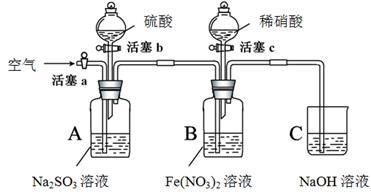
实验记录如下:
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2++ NO [Fe(NO)]2+
[Fe(NO)]2+
用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。

实验记录如下:
| 实验操作 | 实验现象 | |
| I | 打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c | B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II | 用注射器取出少量B装置中的溶液,加入KSCN溶液 | 溶液变为红色。 |
| III | 打开活塞b,向A装置中加入足量硫酸,关闭活塞b | A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV | 一段时间后,用注射器取出少量B装置中的溶液,…… | …… |
| V | 打开活塞a,通入一段时间空气 | ———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2++ NO
 [Fe(NO)]2+
[Fe(NO)]2+用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
您最近一年使用:0次
2016-12-09更新
|
724次组卷
|
2卷引用:2016届北京一五六中学上学期高三期中考试化学试卷



