16. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式
________.
(2)小明认为根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量。镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是
________(3)小红按图1装置改进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
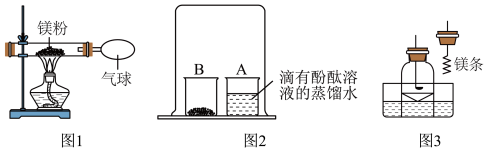
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体。
②镁条能在氮气中燃烧生成黄色的氮化镁(Mg
3N
2)固体。
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【做出猜想】黄色固体为Mg
3N
2【实验探究】按照图2所示,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B。观察到
________现象,得出结论是燃烧产物中含Mg
3N
2。
【反思与交流】空气中N
2的含量远大于O
2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg
3N
2,请给出合理的解释
________。
【拓展延伸】
为了证明镁可在氮气中燃烧生成氮化镁,小红又设计了如下方案进行验证.
步骤①:用盛水的水槽,无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配如图3所示的装置;另准备一只有一根铜丝穿过的橡皮塞,铜丝末端固定一根镁条。
步骤②:引燃燃烧匙中足量的红磷,塞好橡皮塞;待充分冷却,观察到广口瓶内水面上升。
步骤③:往水槽中加水使广口瓶内外水面相平;点燃镁条,迅速更换橡皮塞,镁条在广口瓶内继续燃烧,放出热量;待冷却后广口瓶内水位继续上升。
①步骤②的目的是
________。
②写出镁在氮气中燃烧生成氮化镁的化学方程式:
________。
③2.40g镁条在空气中完全燃烧,所得全部固体质量不可能是
________。
A 3.33g
B 4.00g
C 3.90g
D 3.96g