30. 在生活生产中,铁的应用非常广泛。
(一)认识铁元素及含铁物质
(1)人体缺铁会导致
_____(选填序号)。
A 佝偻病
B 贫血症
C 甲状腺疾病
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到
_____(选填序号)。
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(3)冬季取暖人们常用到暖宝宝,其热量来源于铁的缓慢氧化。已知暖宝宝的主要成分为铁粉、炭粉和少量氯化钠,暖宝宝反应的主要原理是铁粉与氧气、水共同作用生成氢氧化铁,写出反应的化学方程式:
_____;氯化钠的作用是
_____。
(二)制备硫酸亚铁铵晶体的探究
硫酸亚铁铵晶体【(NH
4)
aFe
b(SO
4)
c·xH
2O】(俗称摩尔盐晶体)是一种重要的化工原料,用途十分广泛。某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成的流程如下:
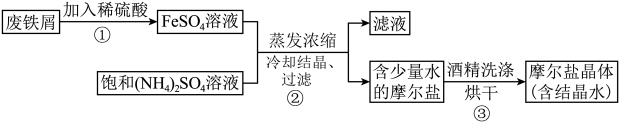
资料:硫酸亚铁铵晶体易溶于水,不溶于乙醇;
(4)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍,碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH
_____7(填“>”、“=”、“<”)
(5)操作③中使用乙醇汽油洗涤可以快速晾干。这样做的优点是
_____;
A 避免用水洗涤所造成的晶体损耗
B 酒精易挥发,可低温晾干晶体
C 防止硫酸亚铁被氧化
(三)硫酸亚铁铵晶体分解的定性探究
硫酸亚铁铵晶体受热分解可得到氧化铁。兴趣小组在科研人员指导下设计实验探究硫酸亚铁铵晶体受热分解的产物。
(6)甲组同学设计了如图1所示实验装置:
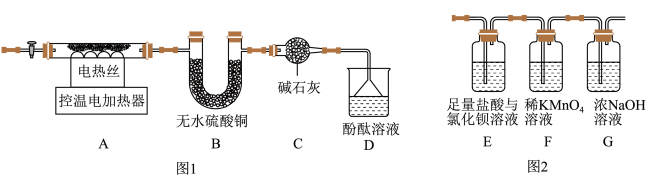
①实验中,装置B中观察到的现象是
_____;
②装置D中观察到酚酞溶液变红色,由此可知分解的产物中有
_____(写化学式)。
(7)乙组同学认为硫酸亚铁铵晶体受热分解的产物中还有SO
2、SO
3。为进行验证,用甲组实验中的装置A和上图2所示装置连接进行实验。观察到装置E中有白色沉淀生成,证明了有SO
3生成,写出该反应的化学方程式
_____;而F装置中
_____、表明生成了SO
2。
(四)硫酸亚铁铵晶体成分的定量探究
【实验步骤】:取3份质量均为7.84g的(NH
4)
aFe
b(SO
4)
c·xH
2O晶体,分别进行实验。①向一份中加入过量的NaOH溶液,充分反应后得到0.68gNH3②向另一份中加入过量的BaCl
2溶液,充分反应后过滤、洗涤、干燥得到9.32g沉淀③加热第三份晶体使其分解,剩余固体质量与温度的关系如图所示

回答下列问题:
资料:硫酸亚铁铵晶体受热时,在200℃以下只失去结晶水。
(8)实验中加入过量BaCl
2溶液的目的
_____;
(9)根据实验数据,计算硫酸亚铁铵晶体的化学式
_____;写出A点到B点发生反应的化学方程式
_____。