1. 用含钴废料(主要成分为Co,含有一定量的Ni、Al
2O
3、Fe、SiO
2等)制备草酸钴晶体(CoC
2O
4·2H
2O)的工业流程如图。已知:①草酸钴晶体难溶于水;②RH为有机物(难电离)。
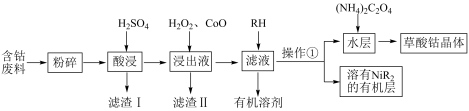
(1)H
2O
2是一种绿色氧化剂,写出加入H
2O
2后发生反应的离子方程式:
_________________。
(2)加入氧化钴的目的是
_______________________________。
(3)草酸钴晶体分解后可以得到多种钴的氧化物(其中Co的化合价为+2、+3),取一定量钴的氧化物,用280mL5mol·L
-1盐酸恰好完全溶解,并得到CoCl
2溶液和2.24L(标准状况)黄绿色气体,由此可确定该钴氧化物中Co、O的物质的量之比为
________。
(4)实验室可以用酸性KMnO
4标准液滴定草酸根离子(C
2O
42-),测定溶液中

的浓度,写出此反应的离子方程式:
_______________________________________;KMnO
4标准溶液常用硫酸酸化,若用盐酸酸化,会使测定结果
________(填“偏高”“偏低”或“无影响”)。