38. 空气中氧气含量测定的再认识。
Ⅰ【经典赏析】教材介绍了拉瓦锡用定量的方法研究了空气的成分,实验装置及资料如下。
| 汞(有毒) | 氧化汞 | 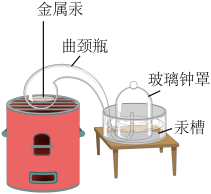 |
| 密度 | 13.546g/cm3 | 密度 | 11.14g/cm3 |
| 沸点 | 356.58°C | 不能溶于汞 |
| 加热至沸与氧气反应,12天 | 分解温度 | 500°C |
① 写出汞与氧气反应的化学方程式
__________。
②拉瓦锡在实验中选择使用“汞”的优点如下:
A 液态的汞在汞槽中既起到液封的作用,又能直接用来测见反应器内空间体积的变化。
B 汞加热后只跟氧气反应,且生成的氧化汞易加热分解又得到原先质量的汞和氧气,把得到的氧气加到剩下的4/5体积的气体中,结果所得气体跟空气的性质完全相同
C 氧化汞的密度小于汞,且不溶于汞,因此易与汞分离。
D 汞的沸点低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽。
但现在实验室的模仿研究却不用“汞”的原因有:
__________。
③加热红色氧化汞粉末得到汞和氧气的微观过程如下:
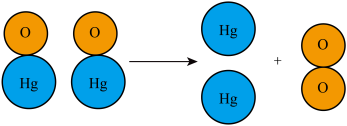
根据图示获得的信息是
__________。
A 可说明分子质量大,原子质量小
B 可说明原子也能保持物质的化学性质
C 氧化汞由一个汞原子和一个氧原子构成
D 所得氧气与原空气中的氧气化学性质相同
Ⅱ【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量,写出红磷燃烧的化学方程式:
__________。
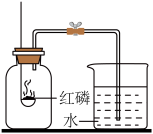
兴趣小组在老师的指导下,分别用红磷、白磷进行该实验,用测气体压强的传感器测得反应后装置内气体压强减小分别为12.15%、17.79%。
用燃烧磷的方法测出的氧气含量常常远低于21%。
【提出问题】用红磷燃烧的方法测出的氧气含量为什么常常远远偏低?
【进行猜想】可能的原因有①装置漏气;②
__________,装置内氧气有剩余;等……。
Ⅲ【实验探究1】小明根据铁在空气中易生锈(铁锈的主要成分为氧化铁)的原理,探究能否用铁来准确测定空气中氧气的含量。于是进行了以下实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
【交流与反思】查阅资料得知白磷剧毒、磷燃烧产生的白烟接触水后也有毒。与用红磷、白磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是
______________,缺点是
_______________。
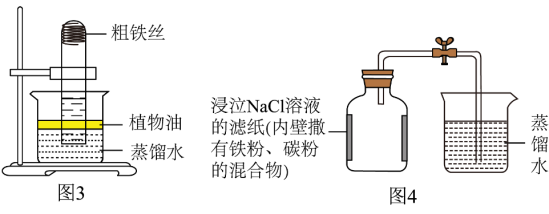
Ⅳ【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如表所示。
| 实验前的体积/mL | 实验后的体积/mL |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 130 | 90.0 | 63.7 |
请列式计算出空气中氧气含量为
_______________(计算结果保留一位小数)
【结论与反思】通过上述实验探究,同学们认为测定空气中氧气含量的最佳方案是选用铁粉、炭粉、氯化钠和蒸馏水进行实验,理由是
___________。