浙江省台州市临海市第五中学、东塍中学2023-2024学年九年级上学期期中联考科学试题
浙江
九年级
期中
2024-02-11
17次
整体难度:
适中
考查范围:
常见的物质、科学探究所需要的基本技能、物质的运动与相互作用、物质的结构、生物的新陈代谢
一、选择题 添加题型下试题
A. 石雕花窗 石雕花窗 | B. 烤海苔饼 烤海苔饼 |
C. 剪纸 剪纸 | D. 做草编 做草编 |
【知识点】 化学变化和物理变化的判别
A. 测溶液pH值 测溶液pH值 | B. 过滤 过滤 |
C. 稀释浓H2SO4 稀释浓H2SO4 | D. 倾倒液体 倾倒液体 |
【知识点】 常见实验操作 浓硫酸的性质及浓硫酸的稀释
| A.氧化钙、生石灰、CaO | B.碳酸钠、纯碱、Na2CO3 |
| C.氢氧化钙、熟石灰、CaCO3 | D.氯化钠、食盐、NaCl |
【知识点】 盐的性质及用途 氧化物、酸、碱和盐的概念

| A.食盐水 | B.白酒 | C.蔗糖水 | D.白醋 |
【知识点】 盐的性质及用途
 )可用于肉类食品的防腐,但应严格控制用量。亚硝酸钠中氮元素的化合价为( )
)可用于肉类食品的防腐,但应严格控制用量。亚硝酸钠中氮元素的化合价为( )| A.0 | B.-3 |
| C.+5 | D.+3 |
【知识点】 有关元素化合价的计算

A.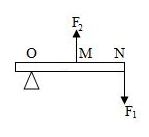 | B.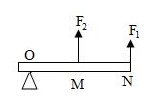 | C.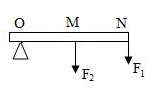 | D.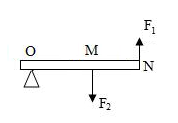 |
【知识点】 杠杆的分类

| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
【知识点】 分解反应及其应用 识别化学反应基本类型

| A.上坡时,大货车的重力势能增大 |
| B.下坡路段刹车失灵的大货车动能越来越大 |
| C.以相同速度行驶时,大货车比小轿车的动能大 |
| D.大货车冲上避险车道时,动能全部转化为重力势能 |
【知识点】 动能和势能的转化与守恒
| A.金属表面除锈 | B.实验室与块状大理石制取CO2 |
| C.除去NaCl中的少量NaOH | D.制造药物氯化锌 |
【知识点】 酸的化学性质
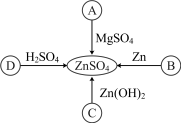
| A.A----Zn(OH)2 | B.B----CuSO4 |
| C.C----H2SO4 | D.D----ZnO |
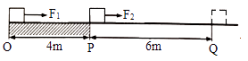
| A.W1>W2 | B.W1<W2 | C.P1>P2 | D.P1<P2 |
| A.加熟石灰混合研磨,区分硝酸铵和氯化钾两种化肥 |
| B.用灼烧闻气味的方法可鉴别羊毛和合成纤维 |
| C.用氯化钡溶液区分稀盐酸和稀硫酸 |
| D.用氢氧化钠中和酸性土壤 |
序号 | 实验目的 | 实验过程 |
A | 证明变质 | 取少量溶液,滴加盐酸,将生成的气体通入石灰水 |
B | 确定成分 | 取少量溶液,向滤液中滴加酚酞试液 |
C | 测定纯度 | 取一定量溶液,加入浓盐酸,用氢氧化钠固体吸收气体,称量 |
D | 除去杂质 | 取溶液,滴加氯化钡溶液恰好完全反应,过滤 |
| A.A | B.B | C.C | D.D |
二、填空题 添加题型下试题
(1)下列属于混合物的是
①金属铁 ②白酒 ③洁净的空气 ④玫瑰香醋 ⑤蒸馏水
(2)下列物品是由有机合成材料制成的是
A. 羊毛衫 B. 玻璃杯 C. 不锈钢餐具 D. 塑料雨衣
(3)铜也会生锈,下图是某化学实验小组借鉴课本“铁钉锈蚀条件的探究”实验,设计了“铜片锈蚀条件的探究”实验。实验较长时间后,发现A试管中铜片最先生锈,则铜锈蚀的条件是

【知识点】 金属锈蚀的条件及其防护 合成塑料 常见物质的分类
(1)下列化肥中,属于氮肥的是
A.碳酸氢铵[NH4HCO3] B.草木灰(主要成分[K2CO3] ) C.磷矿粉[Ca3(PO4)2]
(2)涌泉一些果农种植大棚早熟蜜柑时,常向大棚中补充气体肥料CO2,目的是促进其光合作用。此过程实现的能量转化为
【知识点】 光合作用的原理 盐与化肥 能量的转化与转移的方向性
(1)用毛笔蘸取稀硫酸在竹片上画花,然后烘干,水洗,在竹片上就得到一幅精美的呈黑色或褐色的竹片画。在烘干的过程中稀硫酸变为浓硫酸,制作竹片画时就利用了浓硫酸的
(2)在加热的条件下浓硫酸与铜反应的化学方程式是Cu+2H2SO4(浓)
 CuSO4+SO2↑+2X,则X的化学式是
CuSO4+SO2↑+2X,则X的化学式是(3)常温下铁遇到浓硫酸在表面会形成一层 致密的氧化膜,因此工业上浓硫酸用铁罐来储存。装过浓硫酸的铁罐在用水清洗时会产生气泡,该反应的微观示意图如图所示,其中“〇”表示的离子是

【知识点】 酸的化学性质
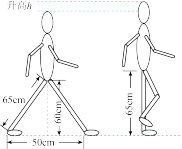
(1)小华测出自己的步距为0.5m,他从教学楼的一端走到另一端,共走了84步,用时35s,则他的步行速度为
(2)小华根据自己的腿长和步距画出了如图所示的步行示意图,对步行时重心的变化进行了分析,当两脚一前一后着地时重心降低,而单脚着地迈步时重心升高,因此每走一步都要克服重力做功。则小华每走一步克服重力所做的功为
三、探究题 添加题型下试题
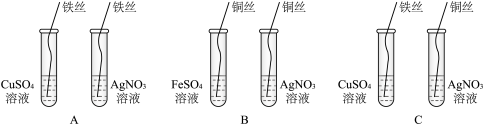
(1)三种实验方案中不能达到实验目的的是:
(2)将铁丝放入CuSO4溶液中能观察到的实验现象是:
【知识点】 金属活动性顺序及其应用 金属的化学性质
四、填空题 添加题型下试题
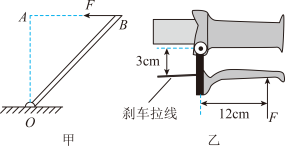
【知识点】 杠杆的平衡条件
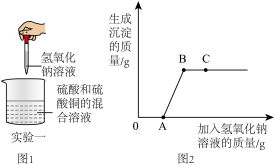
(1)OA段没有沉淀的原因是
(2)B点处溶液的溶质是
(3)C点处溶液呈
【知识点】 碱的化学性质
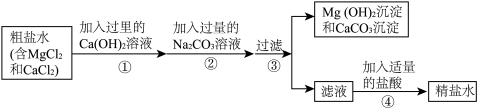
(1)步骤①反应的化学方程式为
(2)步骤②中,加入过量的Na2CO3可以除去
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有
五、探究题 添加题型下试题
[提出问题]反应后溶液中的溶质是什么呢?
[假设猜想]同学们做出猜想如下:
猜想一:只有Na2SO4
猜想二:有Na2SO4和NaOH
猜想三:有Na2SO4和H2SO4
猜想四:有Na2SO4、H2SO4和NaOH
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量反应后的溶液于洁净试管中,滴加 | 溶液不变红 | 猜想二不成立 |
| 步骤2:另取少量反应后的溶液于另一洁净试管中,滴加Na2CO3溶液 | | 猜想一不成立 |
(2)【实验探究】
[结论]猜想三成立。
[拓展]要完成实验探究中的步骤2,下列提供的试剂还可以选用的有
A.银粉 B.生锈的铁钉 C.氯化钡溶液 D.氢氧化铁
【知识点】 中和反应及其应用
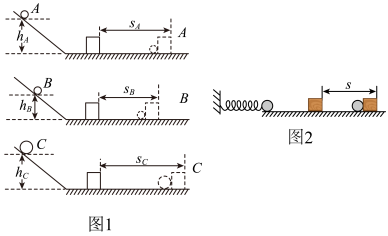
(1)实验中,探究的动能是指
A.小球在斜面上的动能 B.小球撞击木块时的动能
C.小球撞击木块后的动能 D.木块被小球撞击的动能
(2)使质量相同的小球从斜面上不同高度处自由滚下,是为了研究动能大小与
(3)小华同学通过比较图1中B、C两图,得出“质量大的物体动能大”,小丽认为小华的这一比较过程存在错误,你知道错误是什么吗?
(4)小明同学尝试改用如图2所示装置探究“物体动能大小与哪些因素有关”,设计了以下两个实验方案:
方案一:用同一钢球将同一弹簧压缩至不同程度,静止释放,撞击同一木块,比较木块被撞击的距离;
方案二:用质量不同的钢球将同一弹簧压缩相同程度后静止释放,撞击同一木块,比较木块被撞击的距离。
关于他的实验方案
A.只有方案一可行 B.只有方案二可行
C.两个方案均可行 D.两个方案均不可行
【知识点】 动能的影响因素
【问题一】镁条与碳酸钠溶液反应产生的气体是什么?
【作出猜想】猜想1:可能是二氧化碳; 猜想2:可能是氢气。
【问题二】镁条与碳酸钠溶液反应产生的白色不溶物是什么?
【查阅资料】
①Mg(OH)2难溶于水,MgCO3微溶于水,它们受热都会分解成两种氧化物;
②白色的无水硫酸铜遇水变蓝色。
【作出猜想】甲同学猜想:是Mg(OH)2;
乙同学猜想:是MgCO3;
丙同学猜想:是Mg(OH)2和MgCO3的混合物。
【进行实验】取白色不溶物放入试管中,滴加足量的稀盐酸,观察到有气泡产生,得出甲同学的猜想不正确。小明通过进一步实验得出丙同学的猜想正确。他的实验操作及现象是
【问题三】镁条与碳酸钠溶液反应快速产生大量气泡的原因是什么?
【查阅资料】Na2CO3溶液中除Na+、CO32-外,还有OH—;镁条与水能缓慢反应生成H2。
【作出猜想】可能是Na+、CO32-、OH-中的某一种离子促进了镁与水的反应。
【进行实验】按如图所示方案进行实验。发现只有A中产生气泡较快,而B、C中产生气泡很缓慢。

(1)试剂X是
(2)该实验说明是
【查阅资料】
杆秤是我国古老的质量称量工具(如图甲),刻度是均匀的。使用时先把被测物体挂在秤钩处,提起秤纽,移动秤砣,当秤杆在水平位置平衡时,秤砣悬挂点对应的数值即物体的质量。
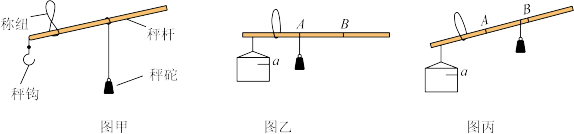
【产品制作】
器材:木棒、塑料杯、细线、刻度尺、金属块(代替秤砣)。
步骤:①模仿杆秤结构,用杯子代替秤钩,先自制一根无刻度“密度秤”
②杯中不加液体,提起秤纽,移动秤砣,当秤杆在水平位置平衡时(如图乙),将此时秤砣的悬挂点A标记为“0”刻度。
③杯中加水至a处,提起秤纽,移动秤砣,当秤杆在水平位置平衡时,将此时秤砣的悬挂点B标记为某刻度(单位:g/cm3)。
④以AB两点之间长度的
 为标准,在整根秤杆上均匀地标上刻度。
为标准,在整根秤杆上均匀地标上刻度。【产品检验】
在杯中倒入“等量”的密度已知的液体,移动秤砣使“密度秤”在水平位置平衡,读出该液体的密度,与其密度值比对。用多种密度已知的液体,重复上述操作,进行检验。
(1)在制作过程中,秤杆出现左低右高现象,如图丙,要将秤杆调至水平位置平衡,秤砣应往
(2)步骤③中,秤砣悬挂点B标记的刻度值应为
(3)产品检验时在杯中倒入“等量”密度已知的液体,“等量”指加入液体的
(4)【产品升级】为了制作出精确度更高的“密度秤”,下列改进措施可行的是
A.把秤纽位置往远离杯子一侧移动 B.减小秤砣的质量
C.减少加入杯中的液体体积 D.换用更细的秤杆
【知识点】 杠杆的平衡条件
【实验验证】
| 步骤 | 现象 | 结论 |
| 取少量该粉末加入足量蒸馏水,充分搅拌 | 得到无色澄清溶液 | 杂质中一定没有氯化铜 |
| 取上述无色溶液少许于试管中,滴加氯化钡溶液 | 有白色沉淀生成 | 杂质中一定没有硝酸钙 |
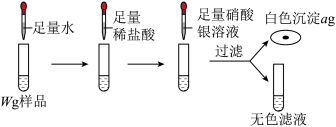
| 另称取14.9g粉末于烧杯中,加入蒸馏水溶解,再加入足量硝酸银溶液和稀硝酸,过滤,将滤渣洗涤烘干并称量 | 生成白色沉淀,测得沉淀质量为28.7g | 杂质中一定有 |
【实验拓展】为了确定样品中氯元素的质量分数,小组同学设计了如下实验继续探究:
(1)小文认为上述实验测定样品中的氯元素质量分数会比实际的大,理由是:
(2)为了准确测定样品中氯元素的质量分数,小科对上述实验过程进行改进,改进的措施为:

(1)如图1,取5gNaOH溶液于烧杯中,滴入酚酞溶液,再逐滴加入稀盐酸至过量。在实验过程中能说明氢氧化钠与盐酸发生反应的现象为
(2)利用图2装置,向氢氧化钠溶液中匀速加入溶质质量分数为7.3%且初温相同的稀盐酸,利用温度传感器测定得到温度变化曲线如图3所示。
①氢氧化钠和盐酸反应是
②当加入盐酸为
③图2装置中的NaOH溶液中溶质的质量是多少克?
【知识点】 中和反应及其应用
六、解答题 添加题型下试题
(1)压路机能将路面压实,是因为力能使物体
(2)该压路机辗压路面时,与路面的接触面积为1.5m2,则它对水平路面的压强为
(3)该压路机发动机以额定功率正常工作时,在水平路面上匀速行驶500s,前进了2000m,发动机做了多少功

七、探究题 添加题型下试题
(1)取少量“银粉”于试管中,滴加适量盐酸,观察到有
(2)为了进一步确定“银粉”是铝还是锌,小王通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图象。在绘制锌的图象时,a点所对应的锌的质量m为多少?
(3)取1.8克“银粉”(杂质忽略不计)加入到50克稀盐酸中,恰好完全反应,生成氢气0.2克。根据图可知,“银粉”是

【知识点】 金属的化学性质
八、解答题 添加题型下试题
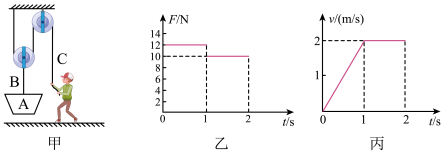
(1)动滑轮的重力为多少?
(2)第2s内拉力F的功率为多少?
(3)此装置最多能匀速运载多重的货物?

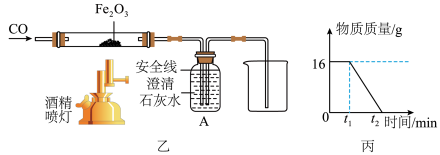
(1)《千里江山图》色彩艳丽,璀璨夺目,这与所用矿石颜料赭石(主要成分为Fe2O3) 有关。我国早在春秋战国时就开始利用赭石炼铁,主要反应原理是:Fe2O3+3CO
 2Fe+3CO2 ,其中属于还原剂的是
2Fe+3CO2 ,其中属于还原剂的是(2)实验室可用如图乙所示的装置模拟炼铁,A装置的功能有
(3)丙图是玻璃管中氧化铁的质量随时间变化的趋势图,请画出生成铁的质量随时间变化的图像和坐标。

【知识点】 金属的冶炼
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化和物理变化的判别 | |
| 2 | 0.94 | 常见实验操作 浓硫酸的性质及浓硫酸的稀释 | |
| 3 | 0.85 | 力是否做功的判断 | |
| 4 | 0.94 | 盐的性质及用途 氧化物、酸、碱和盐的概念 | |
| 5 | 0.85 | 盐的性质及用途 | |
| 6 | 0.85 | 杠杆的分类 | |
| 7 | 0.94 | 有关元素化合价的计算 | |
| 8 | 0.85 | 杠杆的分类 | |
| 9 | 0.85 | 分解反应及其应用 识别化学反应基本类型 | |
| 10 | 0.85 | 动能和势能的转化与守恒 | |
| 11 | 0.85 | 酸的化学性质 | |
| 12 | 0.85 | 酸的化学性质 盐的性质及用途 | |
| 13 | 0.85 | 功率计算公式的应用 功的计算公式的应用 | |
| 14 | 0.85 | 中和反应及其应用 盐与化肥 | |
| 15 | 0.85 | 碱的化学性质 盐的性质及用途 常见物质的鉴定 | |
| 二、填空题 | |||
| 16 | 0.65 | 金属锈蚀的条件及其防护 合成塑料 常见物质的分类 | |
| 17 | 0.85 | 光合作用的原理 盐与化肥 能量的转化与转移的方向性 | |
| 18 | 0.85 | 酸的化学性质 | |
| 19 | 0.65 | 速度公式及其应用 功的计算公式的应用 | |
| 21 | 0.65 | 杠杆的平衡条件 | |
| 22 | 0.85 | 碱的化学性质 | |
| 23 | 0.65 | 酸的化学性质 碱的化学性质 盐的性质及用途 物质除杂或净化 | |
| 三、探究题 | |||
| 20 | 0.85 | 金属活动性顺序及其应用 金属的化学性质 | |
| 24 | 0.65 | 中和反应及其应用 | |
| 25 | 0.65 | 动能的影响因素 | |
| 26 | 0.65 | 盐的性质及用途 常见物质的鉴定 | |
| 27 | 0.65 | 杠杆的平衡条件 | |
| 28 | 0.65 | 盐的性质及用途 常见物质的鉴定 | |
| 29 | 0.65 | 中和反应及其应用 | |
| 31 | 0.85 | 金属的化学性质 | |
| 四、解答题 | |||
| 30 | 0.65 | 二力平衡条件的应用 压强的大小及其计算 功率计算公式的应用 功的计算公式的应用 | |
| 32 | 0.65 | 滑轮组及其工作特点 滑轮组绳子拉力的计算 功率计算公式的应用 功的计算公式的应用 | |
| 33 | 0.85 | 金属的冶炼 | |


 核桃夹
核桃夹 羊角锤
羊角锤 镊子
镊子 起子
起子

