24. 某兴趣小组对实验室氯酸钾和二氧化锰反应进行如下探究。
【提出问题】如何在明二氧化锰是氯酸钾分解反应的催化剂?
【查阅资料】①氯化钾可溶于水,二氧化锰不溶于水。
②氯酸钾、二氧化锰、氯化钾的熔点分别为356℃、535℃、770℃。
③氧气传感器测量范围(%):0~30(体积分数)
【设计并完成实验】
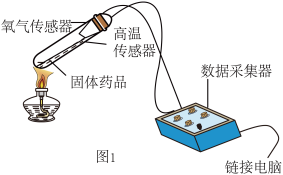
①将4.0g氯酸钾放在试管中,用图Ⅰ装置(省略夹持仪器)进行实验。
②将4.0g氯酸钾与2.0g二氧化锰粉末混合均匀后放在试管中,用图1装置进行实验。
③将4.0g氯酸钾与1.0g二氧化锰粉末混合均匀后放在试管中,用图1装置进行实验。
④将实验②、③反应后的固体分别加水溶解、操作X、洗涤、干燥、称量,分别得到2.0g、1.0g黑色粉末。
⑤将实验④得到的2.0g、l.0g黑色粉末再分别和4g氯酸钾混合,用图1装置重复实验,到的结果分别与实验②、③相同。
【实验数据】实验①②③数据见图2和图3。
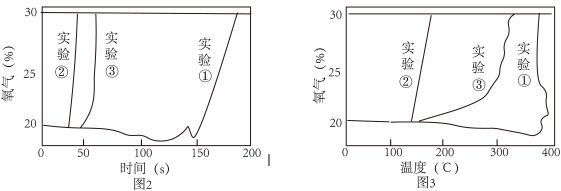

【实验分析】
(1)二氧化锰可
______(填“加快”或“减慢”)氮酸钾分解反应的速率。
(2)操作X为
______。
(3)实验④与⑤的目的是证明二氧化锰的
______和
______在该化学反应前后都没有发生改变。
【实验结论】
(4)二氧化锰可作氯酸钾分解反应的催化剂,该反应的化学方程式为
______。
【实验反思】
(5)图1装置中,试管口向上倾斜,请说明这样放置的原因:
______。
(6)二氧化锰粒径大小对氯酸钾分解催化效果有没有影响?
取2份4.0g氯酸钾与2.0g二氧化锰、粒径大小不同的二氧化锰,加热,用传感器测得固体残留率(反应剩余固体质量与反应前固体质量之比)如图4所示。
分析图像,对氯酸钾分解的催化效果更好的为粒径
______(选填“1~2mm”或“0.002mm”)的二氧化锰。
(7)结合图2、3、4提供的信息,对于同种能化剂。还有哪些因素可能影响其催化效果?请写出一种可能因素:
______。
【实验拓展】
(8)实验①,若反应一段时间后,停止实验,此时可推测试管内固体中一定含物质A,则A是
______(填化学式),固体中可能含氯酸钾。
(9)利用图5溶解度曲线信息,可确定反应后试管内固体的成分。

①30℃时,氯酸钾的溶解度是
______。
②冷至室温,取反应后试管内固体3g(假设固体成分混合均匀),放入30℃时10g水中,充分溶解后,若看到
______现象时,则固体一定是氯酸钾和物质A的混合物,且氯酸钾的质量范围是
______。(用m表示氯酸钾质量)