安徽省皖豫名校联盟 安徽卓越县中联盟2024届高三下学期5月联考化学试卷
安徽
高三
模拟预测
2024-05-14
227次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础、认识化学科学
安徽省皖豫名校联盟 安徽卓越县中联盟2024届高三下学期5月联考化学试卷
安徽
高三
模拟预测
2024-05-14
227次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础、认识化学科学
一、单选题 添加题型下试题
单选题
|
容易(0.94)
解题方法
1. 品安徽名茶,秀淡雅人生。茶器是茶文化的一部分,下列茶器的主要成分是硅酸盐的是
选项 | A | B | C | D |
茶器 |
|
|
|
|
名称 | 清“寿字”高盅 | 龙首银茶壶 | 都篮 | 象牙茶则 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
2. 化学与生活联系密切。下列叙述错误的是
| A.紫外线灯可用于衣物的消毒杀菌 |
| B.石膏常用于制作模型和医疗石膏绷带 |
| C.葡萄糖在酶的催化下水解为乙醇,可用作燃料 |
| D.将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
3. 近日,《国家科学评论》在线发表了南京师范大学陈旭东教授课题组和清华大学李隽教授课题组的合作研究成果,该研究团队完成了具有二十面体结构的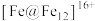 铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
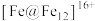 铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
铁团簇(如图所示)的合成与计算化学研究。下列说法正确的是
A. 比 比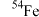 多2个电子 多2个电子 | B.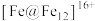 具有还原性 具有还原性 |
| C.Fe位于元素周期表第10纵列 | D.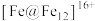 中铁与铁之间存在离子键 中铁与铁之间存在离子键 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
4. 实验是进行科学探究的重要方式。下列叙述正确的是
| A.过滤适用于过滤胶状氢氧化物类沉淀 |
| B.用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 |
| C.某些强氧化剂(如高锰酸钾)与葡萄糖的混合物不能研磨,否则可能引起爆炸 |
| D.除去碱式滴定管胶管内的气泡时,将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
5. 根据下列实验事实能得出相应结论的是
选项 | 实验事实 | 结论 |
A | 向0.1 mol·L  溶液中滴加双氧水,溶液褪色 溶液中滴加双氧水,溶液褪色 |  具有漂白性 具有漂白性 |
B | 分别加热 和 和 固体,试管内壁均有水珠 固体,试管内壁均有水珠 | 两种物质均受热分解 |
C | 向水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色 溶液,呈棕黄色;煮沸,溶液变红褐色 | 升温能促进 水解 水解 |
D | 向0.1 mol·L  溶液中滴加等浓度的醋酸溶液,无明显现象 溶液中滴加等浓度的醋酸溶液,无明显现象 | 酸性: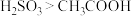 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 有机物M是一种重要的亲电试剂,常用于有机合成,其结构如图所示,其中X、Y、Z、W为原子序数依次增大的短周期元素,X是空气中含量最高的元素,Y、W同主族。
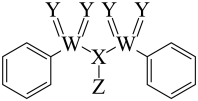
| A.电负性:Z>W>Y |
B.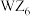 属于非极性分子 属于非极性分子 |
| C.简单氢化物的沸点:Z>X,与化学键的键能有关 |
| D.最高价氧化物对应水化物的酸性:Z>W |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。 作为配体可提供孤电子对,回收定影液时
作为配体可提供孤电子对,回收定影液时 溶液能溶解AgBr形成
溶液能溶解AgBr形成 。下列叙述正确的是
。下列叙述正确的是
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。 作为配体可提供孤电子对,回收定影液时
作为配体可提供孤电子对,回收定影液时 溶液能溶解AgBr形成
溶液能溶解AgBr形成 。下列叙述正确的是
。下列叙述正确的是A.从结构分析, 中两个硫原子均显+2价 中两个硫原子均显+2价 |
B.键角: 大于 大于 |
C.1个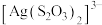 中含有8个σ键 中含有8个σ键 |
D. 中提供孤电子对的是中心硫原子 中提供孤电子对的是中心硫原子 |
【知识点】 共价键的形成及主要类型解读 简单配合物的成键解读
您最近一年使用:0次
单选题
|
较难(0.4)
8.  作为配体可提供孤电子对,回收定影液时
作为配体可提供孤电子对,回收定影液时 溶液能溶解AgBr形成
溶液能溶解AgBr形成 。一种制备
。一种制备 的方法为向
的方法为向 与
与 的混合溶液中通入
的混合溶液中通入 气体,同时生成
气体,同时生成 。下列离子方程式书写错误的是
。下列离子方程式书写错误的是
 作为配体可提供孤电子对,回收定影液时
作为配体可提供孤电子对,回收定影液时 溶液能溶解AgBr形成
溶液能溶解AgBr形成 。一种制备
。一种制备 的方法为向
的方法为向 与
与 的混合溶液中通入
的混合溶液中通入 气体,同时生成
气体,同时生成 。下列离子方程式书写错误的是
。下列离子方程式书写错误的是A. 在稀硫酸中不稳定: 在稀硫酸中不稳定: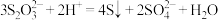 |
B.制备 的总反应: 的总反应: |
C. 溶液溶解AgBr: 溶液溶解AgBr: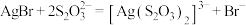 |
D.向 溶液中滴加过量氯水: 溶液中滴加过量氯水: |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 一定温度下,向2.0 L恒容密闭容器中充入一定量的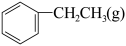 ,在催化剂作用下发生脱氢反应:
,在催化剂作用下发生脱氢反应: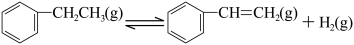
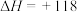 kJ·mol
kJ·mol ,测得乙苯脱氢反应时间与容器中气体总压强的关系如图所示:
,测得乙苯脱氢反应时间与容器中气体总压强的关系如图所示:

| A.乙苯脱氢反应在相对较高温度下能自发进行 |
B.0~4h内平均反应速率可用压强变化表示为v( ) )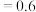 kPa⋅h kPa⋅h |
| C.若向平衡体系中再通入适量的乙苯气体,平衡正向移动 |
| D.若在平衡时扩大容器的容积使体系压强恢复至起始压强,再次达到平衡时乙苯的体积分数减小 |
您最近一年使用:0次
10. 三维骨架结构的KFeC2O4F材料具有优异的储钾性能,且该材料成本低廉、合成简单、热稳定性良好,可用于钾离子全电池的正极材料。一种钾离子全电池放电时的工作原理如图所示: 。下列有关说法正确的是
。下列有关说法正确的是
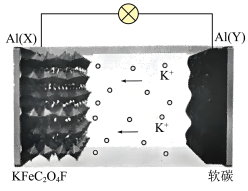
 。下列有关说法正确的是
。下列有关说法正确的是| A.放电时,电流流向:Al(X)→电解液→Al(Y) |
B.放电时,Al(X)电极的电极反应式: |
| C.充电时,Al(X)电极的电势低于Al(Y)电极的电势 |
D.充电时,外电路中每转移1 mol电子,有39 g 从正极材料中脱出 从正极材料中脱出 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 有机物X可用作除氧剂,能发生如图所示的变化。下列说法错误的是
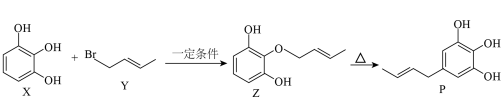
A.X可以与 反应 反应 |
| B.X和Y均能发生聚合反应 |
| C.P分子中所有碳原子可能共平面 |
D.1 mol Z与含1 mol 的水溶液反应,最多能得到2种产物 的水溶液反应,最多能得到2种产物 |
【知识点】 含有酚羟基的物质性质的推断解读
您最近一年使用:0次
12. 某同学按图示装置进行实验(夹持以及尾气处理装置省略),其中能达到相应实验目的的是
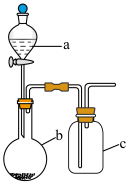
选项 | 实验目的 | a中的物质 | b中的物质 | c中的物质 |
A | 验证SO2的漂白性 | 浓硫酸 | Na2SO3 | 品红溶液 |
B | 验证非金属性:Cl>C>Si | 稀盐酸 | Na2CO3 | Na2SiO3溶液 |
C | 制备Fe(OH)2 | 浓氨水 | 碱石灰 | FeCl2溶液 |
D | 探究干燥Cl2是否具有漂白性 | 浓盐酸 | 漂白粉 | 新鲜花朵 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
13. 近日,清华大学某课题组报道了一种在碳纳米管上负载金属钴酞菁的分子催化剂(CoPc/CNT),实现了一步电化学乙烯( )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示:
 )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示: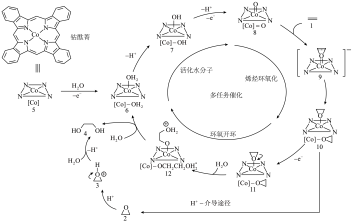
已知: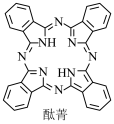 为平面形分子。
为平面形分子。
A.酞菁分子中氮原子的杂化类型为 、 、 |
| B.步骤“5→6”中钴元素被还原 |
| C.上述反应过程中没有极性键的形成 |
D.步骤“2→3→4”的总反应为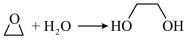 |
您最近一年使用:0次
单选题
|
较难(0.4)
14. 已知:HA为一元弱酸;
 、
、
 。常温下,向
。常温下,向 和
和 的混合溶液中滴加NaA溶液,溶液中
的混合溶液中滴加NaA溶液,溶液中 [
[ 、
、 或
或 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是

 、
、
 。常温下,向
。常温下,向 和
和 的混合溶液中滴加NaA溶液,溶液中
的混合溶液中滴加NaA溶液,溶液中 [
[ 、
、 或
或 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是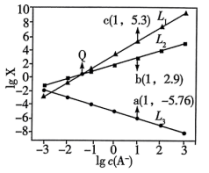
A. 代表 代表 与 与 的关系 的关系 |
B.常温下, |
C. 的K为 的K为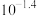 |
D.Q点溶液中 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
15. 3-硝基苯甲酰氯(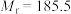 )能用于制染料和有机合成,一种实验室制备原理如图所示:
)能用于制染料和有机合成,一种实验室制备原理如图所示: 、
、 的沸点分别为80℃、78.6℃;②
的沸点分别为80℃、78.6℃;② 和3-硝基苯甲酰氯均易与水反应。
和3-硝基苯甲酰氯均易与水反应。
实验步骤:
ⅰ.在三颈烧瓶中加入3-硝基苯甲酸26.72g( )、50 mL
)、50 mL (0.42 mol)和200 mL无水苯;
(0.42 mol)和200 mL无水苯;
ⅱ.加热至80~85℃搅拌回流5h;
ⅲ.反应完毕,减压回收 和
和 ,冷却,析出黄色晶体;
,冷却,析出黄色晶体;
ⅳ.抽滤、洗涤、干燥、提纯,得22.26g产品。
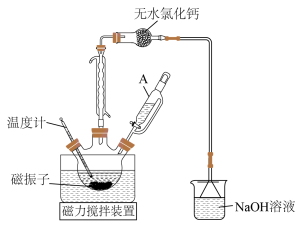
(1)三颈烧瓶洗涤干净后,组装仪器前必须进行的操作是____________ ;相对普通分液漏斗,仪器A的主要优点是____________ 。
(2)本实验中,需要加入一定量的苯,其目的是____________ 。
(3)无水氯化钙______ (填“能”或“不能”)用碱石灰代替,其原因是____________ 。
(4)磁振子起到的两个作用是____________ 。
(5)抽滤装置如图所示,抽滤的先后操作顺序为a→c→b→d→g→______ (填字母)。
e.取下抽滤瓶上的橡皮管f.关闭抽气泵g.洗涤h.确认抽干
(6)本实验3-硝基苯甲酰氯的产率为______ %。
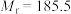 )能用于制染料和有机合成,一种实验室制备原理如图所示:
)能用于制染料和有机合成,一种实验室制备原理如图所示: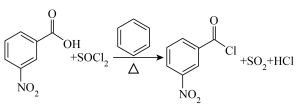
 、
、 的沸点分别为80℃、78.6℃;②
的沸点分别为80℃、78.6℃;② 和3-硝基苯甲酰氯均易与水反应。
和3-硝基苯甲酰氯均易与水反应。实验步骤:
ⅰ.在三颈烧瓶中加入3-硝基苯甲酸26.72g(
 )、50 mL
)、50 mL (0.42 mol)和200 mL无水苯;
(0.42 mol)和200 mL无水苯;ⅱ.加热至80~85℃搅拌回流5h;
ⅲ.反应完毕,减压回收
 和
和 ,冷却,析出黄色晶体;
,冷却,析出黄色晶体;ⅳ.抽滤、洗涤、干燥、提纯,得22.26g产品。
(1)三颈烧瓶洗涤干净后,组装仪器前必须进行的操作是
(2)本实验中,需要加入一定量的苯,其目的是
(3)无水氯化钙
(4)磁振子起到的两个作用是
(5)抽滤装置如图所示,抽滤的先后操作顺序为a→c→b→d→g→
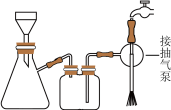
e.取下抽滤瓶上的橡皮管f.关闭抽气泵g.洗涤h.确认抽干
(6)本实验3-硝基苯甲酰氯的产率为
您最近一年使用:0次
16. 硝酸镍、硝酸钠在陶瓷、玻璃工业应用广泛。以废弃镍板(含有少量的氧化铝杂质)生产硝酸镍、硝酸钠的工艺流程如图所示: 难溶于水。
难溶于水。
②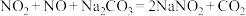 ,
,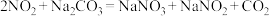 。
。
请回答下列问题:
(1)工业生产普通玻璃的主要原料有石英砂、______ 。
(2)“反应器”中需控制反应温度为:50∼60℃的原因是____________ 。
(3)假若Ni与浓硝酸反应产生的混合气体中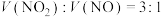 ,该反应的离子方程式为
,该反应的离子方程式为____________ 。
(4)为了除去 ,向“浸取液”中加入
,向“浸取液”中加入 调节pH至5~6。写出除去
调节pH至5~6。写出除去 并生成
并生成 的离子方程式:
的离子方程式:____________ 。
(5)补充完成操作③____________ 。
(6)向“转化器”中加入稀硝酸的目的是____________ 。
(7)若进入“吸收塔”的混合气体中NO为a mol、 为b mol、空气中含
为b mol、空气中含 为d mol,
为d mol, 溶液中含
溶液中含 为c mol,“转化器”中加入的稀硝酸中含e mol
为c mol,“转化器”中加入的稀硝酸中含e mol  ,则
,则
______ (用含e、d的代数式表示,不考虑流程中钠、氮元素的损失)。

 难溶于水。
难溶于水。②
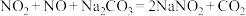 ,
,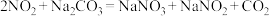 。
。请回答下列问题:
(1)工业生产普通玻璃的主要原料有石英砂、
(2)“反应器”中需控制反应温度为:50∼60℃的原因是
(3)假若Ni与浓硝酸反应产生的混合气体中
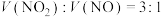 ,该反应的离子方程式为
,该反应的离子方程式为(4)为了除去
 ,向“浸取液”中加入
,向“浸取液”中加入 调节pH至5~6。写出除去
调节pH至5~6。写出除去 并生成
并生成 的离子方程式:
的离子方程式:(5)补充完成操作③
(6)向“转化器”中加入稀硝酸的目的是
(7)若进入“吸收塔”的混合气体中NO为a mol、
 为b mol、空气中含
为b mol、空气中含 为d mol,
为d mol, 溶液中含
溶液中含 为c mol,“转化器”中加入的稀硝酸中含e mol
为c mol,“转化器”中加入的稀硝酸中含e mol  ,则
,则
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
17. 安徽铜陵素有“中国古铜都、当代铜基地”之称,铜产品畅销世界各地。
(1)工业常用火法炼铜,相关反应如下:
反应ⅰ: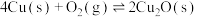

反应ⅱ: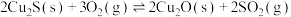
 kJ⋅mol
kJ⋅mol
反应ⅲ:
 kJ⋅mol
kJ⋅mol
反应ⅳ: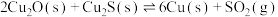
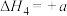 kJ⋅mol
kJ⋅mol
则
______ 。
(2)已知铜离子在浓氨水中以配合物的形式存在。某研究小组以粗铜、纯铜为电极,以浓氨水为电解质溶液,进行粗铜精炼模拟实验。电解过程中, 向阴极移动,一开始阴极表面有气体逸出,一段时间后阴极表面析出红色固体。阴极先后发生的电极反应式为
向阴极移动,一开始阴极表面有气体逸出,一段时间后阴极表面析出红色固体。阴极先后发生的电极反应式为____________ 、____________ 。
(3)T℃下,在体积可变的真空密闭容器中充入1 mol 和足量的
和足量的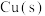 ,发生反应ⅰ,达到平衡后,
,发生反应ⅰ,达到平衡后, min时保持温度不变,将体积压缩至原来的四分之一并保持体积不变(A点状态),再次达到平衡,A点可能向
min时保持温度不变,将体积压缩至原来的四分之一并保持体积不变(A点状态),再次达到平衡,A点可能向______ (填“B”“C”或“D”)点移动,判断依据是____________ 。 和1 mol
和1 mol 发生(1)中反应,达到平衡时测得混合气体的平均摩尔质量为56 g⋅mol
发生(1)中反应,达到平衡时测得混合气体的平均摩尔质量为56 g⋅mol 。该温度下,反应ⅱ的物质的量分数平衡常数
。该温度下,反应ⅱ的物质的量分数平衡常数
______ [反应 的物质的量分数平衡常数
的物质的量分数平衡常数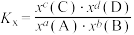 ,其中x(A)、x(B)、x(C)、x(D)为各组分的物质的量分数]。
,其中x(A)、x(B)、x(C)、x(D)为各组分的物质的量分数]。
(5)磷青铜主要用作耐磨零件等,其立方晶胞结构如图所示,用 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。______ 种空间运动状态。
②该晶体中距离Sn原子最近的Cu原子有x个,距离P原子最近的P原子有y个,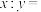
______ 。
③若该晶体的密度为ρ g⋅cm ,最近的Cu原子核间距为
,最近的Cu原子核间距为______ pm(用含ρ、 的代数式表示)。
的代数式表示)。
(1)工业常用火法炼铜,相关反应如下:
反应ⅰ:
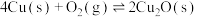

反应ⅱ:
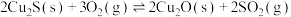
 kJ⋅mol
kJ⋅mol
反应ⅲ:

 kJ⋅mol
kJ⋅mol
反应ⅳ:
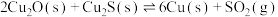
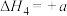 kJ⋅mol
kJ⋅mol
则

(2)已知铜离子在浓氨水中以配合物的形式存在。某研究小组以粗铜、纯铜为电极,以浓氨水为电解质溶液,进行粗铜精炼模拟实验。电解过程中,
 向阴极移动,一开始阴极表面有气体逸出,一段时间后阴极表面析出红色固体。阴极先后发生的电极反应式为
向阴极移动,一开始阴极表面有气体逸出,一段时间后阴极表面析出红色固体。阴极先后发生的电极反应式为(3)T℃下,在体积可变的真空密闭容器中充入1 mol
 和足量的
和足量的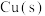 ,发生反应ⅰ,达到平衡后,
,发生反应ⅰ,达到平衡后, min时保持温度不变,将体积压缩至原来的四分之一并保持体积不变(A点状态),再次达到平衡,A点可能向
min时保持温度不变,将体积压缩至原来的四分之一并保持体积不变(A点状态),再次达到平衡,A点可能向
 和1 mol
和1 mol 发生(1)中反应,达到平衡时测得混合气体的平均摩尔质量为56 g⋅mol
发生(1)中反应,达到平衡时测得混合气体的平均摩尔质量为56 g⋅mol 。该温度下,反应ⅱ的物质的量分数平衡常数
。该温度下,反应ⅱ的物质的量分数平衡常数
 的物质的量分数平衡常数
的物质的量分数平衡常数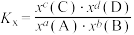 ,其中x(A)、x(B)、x(C)、x(D)为各组分的物质的量分数]。
,其中x(A)、x(B)、x(C)、x(D)为各组分的物质的量分数]。(5)磷青铜主要用作耐磨零件等,其立方晶胞结构如图所示,用
 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。
②该晶体中距离Sn原子最近的Cu原子有x个,距离P原子最近的P原子有y个,
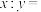
③若该晶体的密度为ρ g⋅cm
 ,最近的Cu原子核间距为
,最近的Cu原子核间距为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
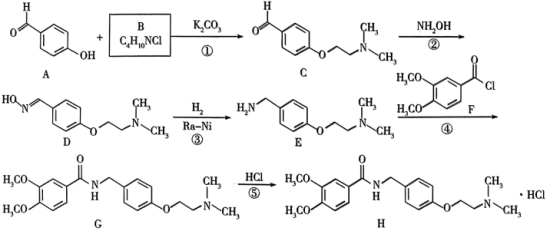
18. 有机化合物H是一种用于治疗功能性消化不良的药物。一种合成H的合成路线如图所示(加料顺序、反应条件略)。
(1)化合物A的名称为______ ;B的结构简式为______ 。
(2)G中含氧官能团的名称为______ 。
(3)化合物M为F的同分异构体,M同时具有如下结构和性质,则M的结构有______ 种(不考虑立体异构)。
a.苯环上有两个取代基b.与 溶液发生显色反应c.酸式水解产物可发生银镜反应
溶液发生显色反应c.酸式水解产物可发生银镜反应
其中核磁共振氢谱上有6组峰的结构简式为______ (填一种)。
(4)参考上述合成路线中②、③和④,无机试剂任选,以 和
和 为含碳原料合成
为含碳原料合成 。已知第一步反应为取代反应,基于你的合成路线回答下列问题:
。已知第一步反应为取代反应,基于你的合成路线回答下列问题:
①第一步反应的化学方程式为____________ 。
②第二步反应生成的有机物的结构简式为____________ 。
③第三步反应的反应类型为______ 。
(1)化合物A的名称为
(2)G中含氧官能团的名称为
(3)化合物M为F的同分异构体,M同时具有如下结构和性质,则M的结构有
a.苯环上有两个取代基b.与
 溶液发生显色反应c.酸式水解产物可发生银镜反应
溶液发生显色反应c.酸式水解产物可发生银镜反应其中核磁共振氢谱上有6组峰的结构简式为
(4)参考上述合成路线中②、③和④,无机试剂任选,以
 和
和 为含碳原料合成
为含碳原料合成 。已知第一步反应为取代反应,基于你的合成路线回答下列问题:
。已知第一步反应为取代反应,基于你的合成路线回答下列问题:①第一步反应的化学方程式为
②第二步反应生成的有机物的结构简式为
③第三步反应的反应类型为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础、认识化学科学
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 硅酸盐工业 淀粉和纤维素组成与结构 化学科学对人类文明发展的意义 常见合金的组成 | |
| 2 | 0.94 | 常见硫酸盐的性质 葡萄糖和果糖 蛋白质的变性 化学科学对人类文明发展的意义 | |
| 3 | 0.85 | 铁 氢氧化亚铁的还原性 元素、核素、同位素 | |
| 4 | 0.65 | 酸碱中和滴定实验基本操作及步骤 乙酸乙酯制备实验的装置及操作 仪器使用与实验安全 过滤 | |
| 5 | 0.85 | 碳酸钠与碳酸氢钠性质的比较 盐类水解规律理解及应用 物质性质实验方案的设计 | |
| 6 | 0.65 | 元素性质与电负性的关系 利用杂化轨道理论判断分子的空间构型 极性分子和非极性分子 | |
| 7 | 0.65 | 共价键的形成及主要类型 简单配合物的成键 | |
| 8 | 0.4 | 离子方程式的正误判断 含硫化合物之间的转化 简单配合物的成键 硫及其化合物综合 | |
| 9 | 0.65 | 化学反应速率计算 化学平衡的移动及其影响因素 压强对化学平衡移动的影响 | |
| 10 | 0.65 | 原电池电子流向判断及应用 原电池、电解池综合考查 电解池电极反应式及化学方程式的书写与判断 利用电子守恒法进行多池串联相关计算 | |
| 11 | 0.65 | 含有酚羟基的物质性质的推断 | |
| 12 | 0.65 | 氯气的化学性质 二氧化硫的漂白性 氢氧化亚铁的制备 元素非金属性强弱的比较方法 | |
| 13 | 0.65 | 氧化还原反应的规律 共价键的形成及主要类型 利用杂化轨道理论判断化学键杂化类型 | |
| 14 | 0.4 | 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 15 | 0.65 | 根据n=m/M的相关计算 取代反应 常见有机物的制备 综合实验设计与评价 | 实验探究题 |
| 16 | 0.65 | 氮氧化物的危害及无害化处理方法 硝酸的强氧化性 硅酸盐工业 盐类水解在生活、生产中的应用 | 工业流程题 |
| 17 | 0.4 | 盖斯定律与热化学方程式 化学平衡常数的有关计算 电解池电极反应式及化学方程式的书写与判断 晶胞的有关计算 | 原理综合题 |
| 18 | 0.65 | 根据要求书写同分异构体 根据题给物质选择合适合成路线 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |







