河北省深州中学2016-2017学年高一下学期期末考试化学试题
河北
高一
期末
2017-09-18
423次
整体难度:
容易
考查范围:
化学实验基础、认识化学科学、常见无机物及其应用、物质结构与性质、化学反应原理、化学与STSE
一、单选题 添加题型下试题
| A.实验剩余的药品不能放回原试剂瓶 |
| B.可燃性气体的验纯 |
| C.气体实验装置在实验前进行气密性检查 |
| D.滴管不能交叉使用 |
A.1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为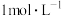 |
B.从1L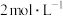 的 的 溶液中取出0.5L,该溶液的浓度为 溶液中取出0.5L,该溶液的浓度为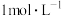 |
C.配制480mL 的 的 溶液,需称量62.5g胆矾 溶液,需称量62.5g胆矾 |
D.中和100mL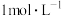 的 的 溶液,需要4g NaOH 溶液,需要4g NaOH |
| A.水玻璃、漂白粉、胆矾均为混合物 |
| B.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| C.能电离出H+的物质属于酸 |
| D.酸性氧化物一定不能与酸起反应 |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.使PH试纸变红的溶液 HCO3﹣、SO42﹣、 Na+、NH4+ |
| B.使石蕊试液变蓝色的溶液:K+、Na+、AlO2-、S2O32- |
| C.能与Al反应生成H2的溶液:NH4+、K+、NO3-、I- |
| D.能与K3[Fe(CN)6]产生蓝色沉淀的溶液:MnO4-、H+、Na+、SO42- |
【知识点】 限定条件下的离子共存解读
| A.还原性:H2O> H2S | B.属于置换反应 |
| C.氧化性:O2> S | D.酸性:H2S> H2O |
【知识点】 氧化还原反应基本概念 氧化性、还原性强弱的比较解读
| A.铝粉与氧化镁共热可制取金属镁 |
| B.足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气 |
| C.在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化 |
| D.工业上用电解熔融Al2O3的方法冶炼铝 |
| A.CO2溶于水形成碳酸,SiO2难溶于水 |
| B.高温下SiO2与碳酸盐反应生成CO2 |
| C.HCl通可溶性碳酸盐溶液中放出气体,通可溶性硅酸盐溶液中生成沉淀 |
| D.CO2通入可溶性硅酸盐中析出硅酸沉淀 |
A.NH4Br的电子式: |
B.HClO的电子式: |
C.中子数为117、质子数为116的Lv原子: 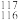 Lv Lv |
D.HCl的电子式: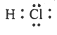 |
【知识点】 化学用语综合判断
| A.第三周期第0族 | B.第四周期第ⅠA族 |
| C.第三周期第ⅠA族 | D.第三周期第ⅦA族 |
| A.热稳定性:HCl> HI | B.原子半径:Na> Mg |
| C.酸性:H2SO3>H2SO4。 | D.结合质子能力:S2-> Cl- |
| A.Na2O2和NaOH | B.CH3COONa和NaOH |
| C.CCl4和H2O | D.CO2和H2O2 |
【知识点】 分子结构与性质
②N2(g)+3H2(g)
 2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是 ( )
A.反应②中的能量变化如图所示: 则ΔH2=E1-E3 |
| B.H2的燃烧热为241.8 kJ·mol-1 |
| C.氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+ 6H2O(g) ΔH=+906 kJ·mol-1 |
| D.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,最终反应放出的热量小于92.4 kJ, |
【知识点】 化学反应热的计算 盖斯定律与热化学方程式解读

| A.该实验研究的是金属的吸氧腐蚀 |
| B.铁表面的反应为Fe-3e-= Fe3+ |
| C.红色首先在食盐水滴的中心出现 |
| D.食盐水中有气泡逸出 |
| A.lmol FeI2与足量氯气反应时转移的电子数为2NA |
| B.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| C.18gD2O和18gH2O中含有的质子数均为10NA |
| D.1 mol Na2O2固体中含离子总数为4NA |
【知识点】 阿伏加德罗常数的求算解读
| A.稀醋酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1 |
| B.已知2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则可知C的燃烧热为110.5 kJ·mol-1 |
| C.氢气的燃烧热为285.5 kJ·mol-1,则水电解的热化学方程式为:2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
| D.甲烷的标准燃烧热为△H=-890.3kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1 |
【知识点】 中和热 燃烧热 热化学方程式书写及正误判断解读
 C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+234.14 kJ/mol,
CO2(g)+2Fe(s) ΔH=+234.14 kJ/mol, C(s)+O2(g)=CO2(g) ΔH= -393.5 kJ/mol,
则2Fe(s)+
 O2(g)=Fe2O3(s)的ΔH是( )
O2(g)=Fe2O3(s)的ΔH是( )| A.-824.39 kJ/mol | B.-627.6 kJ/mol | C.-744.7 kJ/mol | D.-169.4 kJ/mol |
【知识点】 盖斯定律及其有关计算
A.用FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水) Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| B.FeCl3溶液中滴加过量的氨水:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ |
C.用铜电极电解硫酸铜溶液:2Cu2++ 2H2O  2Cu↓ +O2↑ +4H+ 2Cu↓ +O2↑ +4H+ |
| D.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液。当Pb(CH3COO)2溶液中通入H2S气体时有黑色沉淀生成:Pb(CH3COO)2+H2S=PbS↓+ 2 CH3COOH |
【知识点】 离子方程式的正误判断解读
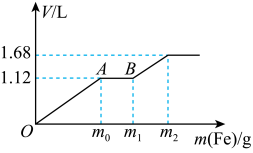
| A.开始时产生的气体为H2 |
| B.AB段产生的反应为置换反应 |
| C.所用混合溶液中c(HNO3)=0.5mol·L-1 |
| D.参加反应铁粉的总质量m2=5.6g |
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氢氧化钡溶液 | 生成白色沉淀 | Al(OH)3不溶于氢氧化钡溶液 |
| C | 向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 | 溶液先不显红色,加入氯水后变红色 | 该溶液中含有Fe2+ |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验方案的设计与评价
| A.第二周期元素的最高正价和负价的绝对值之和等于8 |
| B.ⅦA族元素一定是同周期中非金属性最强的元素 |
| C.氮的非金属性比磷强,所以氮气的性质比白磷活泼 |
| D.Na+半径大于Cl-半径 |
【知识点】 元素周期律的应用

| A.Pt极上有64 g Cu析出时,b极产生22.4 L气体 |
| B.a极的电极反应是2Cl--2e-= Cl2↑ |
| C.电解过程中CuSO4溶液的pH逐渐增大 |
| D.X极是电源负极,Y极是电源正极 |
【知识点】 原电池、电解池综合考查解读

| A.若X为锌片,开关K置于M处,可减缓铁的腐蚀 |
| B.当K置于N处时,可减缓铁的腐蚀 |
| C.若X为碳棒,开关K置于M处,可减缓铁的腐蚀 |
| D.铁被腐蚀过程实质是金属铁失电子发生了还原反应 |
【知识点】 金属的电化学腐蚀与防护
A.已知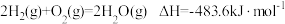 ;则氢气的燃烧热为 ;则氢气的燃烧热为 |
B.已知 ;则金刚石比石墨稳定 ;则金刚石比石墨稳定 |
C.已知 ;则含 ;则含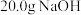 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出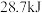 的热量 的热量 |
D.已知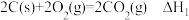 , ,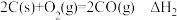 ;则 ;则 |
 溶液。下列叙述中正确的是
溶液。下列叙述中正确的是
A.甲烧杯中溶液的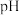 逐渐减小 逐渐减小 | B.乙烧杯中发生还原反应 |
C.外电路的电流方向是从 到 到 | D.电池工作时,盐桥中的 移向甲烧杯 移向甲烧杯 |
【知识点】 原电池原理 原电池原理的应用 原电池电子流向判断及应用解读

A.a极的电极反应式为:2 H+ + 2 e H2 ↑ H2 ↑ |
| B.D口导出的是NaOH溶液 |
| C.C口导出的是NaOH和NaCl的混合溶液 |
| D.浓盐水从A口注入 |

| A.该电池能在高温下正常工作 |
| B.电池工作时,H+向正极移动 |
| C.电池工作时,正极周围溶液的PH将不断变小 |
| D.该电池的总反应式为: 该电池的总反应式为Mg+H2O2+H2SO4=MgSO4+2H2O |
| A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法 |
| B.海水中元素种类很多,总储量很大,如金元素总储量约为5×107 t |
| C.海带提碘过程,将干海带剪碎,酒精润湿,灼烧,加蒸馏水溶解,过滤,滤液滴加稀硫酸,最后滴加几滴淀粉溶液,溶液变蓝 |
| D.海水提溴有两步涉及氯气氧化溴离子的反应,两次目的不同 |
【知识点】 海水资源综合利用
A.2AlCl3(熔融) 2Al+ 3Cl2↑ 2Al+ 3Cl2↑ | B.Fe2O3+ 2Al  Fe+Al 2O3 Fe+Al 2O3 |
C.Cu2S+O2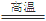 2Cu+SO2 2Cu+SO2 | D.Ag2O 2Ag+O2↑ 2Ag+O2↑ |
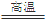 Cu2S+2FeS+SO2,下列说法正确的是
Cu2S+2FeS+SO2,下列说法正确的是| A.SO2仅为氧化产物 | B.CuFeS2仅作还原剂,硫元素被氧化 |
| C.每转移6mol电子,有1mol硫被氧化 | D.每生成0.5molCu2S,有2mol硫被氧化 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
二、解答题 添加题型下试题
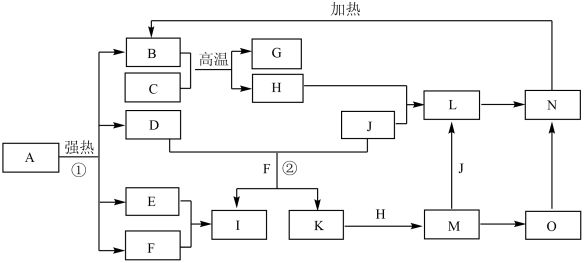
请按要求回答:
⑴写出G、L的化学式G:
⑵反应②的离子方程式
⑶反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为
1∶1∶1∶14,则该反应的化学方程式为
⑷将A直接溶于水(未加稀硫酸酸化)得到的溶液,敞口久置,变质过程中涉及的离子方程式为
三、填空题 添加题型下试题
| 乙 | 丙 | 丁 | |
| 甲 | 戊 |
(1)乙在元素周期表中的位置是
(2)原子半径:戊
(3)乙与戊组成化合物的电子式为
(4)元素的非金属性:甲
A.丙的氢化物稳定,甲的氢化物不稳定
B.丙的最高价氧化物对应的水化物是强酸,甲的是弱酸
C.丙的最高价氧化物对应的水化物易溶于水,甲的难溶
(5)工业上制取甲(粗品)的化学方程式为
【知识点】 元素周期律、元素周期表的推断
四、解答题 添加题型下试题
2NH3+3CuO
 N2+3Cu+3H2O,试回答:
N2+3Cu+3H2O,试回答:(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。

① 仪器连接的顺序(用字母编号表示,仪器可重复使用 )
②列出计算Cu的相对原子质量的表达式
③下列情况将使测定结果偏大的是
A.CuO未全部还原为Cu B.CuO受潮 C.CuO中混有Cu
(2)如果仍采用上述仪器装置,其他方案可选用测定的物理量有
A.m (Cu)和m(CuO) B. m (N2)和m (H2O)
C.m (Cu)和m(H2O) D.m(NH3)和m (H2O)
【知识点】 探究物质组成或测量物质的含量解读 综合实验设计与评价解读
五、填空题 添加题型下试题

(1)图一是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。Cu极的电极反应式是
盐桥中是含有琼胶的KCl饱和溶液,电池工作时K+向
(2)图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是
当铜电极的质量减轻3.2 g时,消耗的CH4在标准状况下的体积为
(1)CH3OH、H2燃烧热分别为:△H=-725.5 kJ/mol、△H=-285.8 kJ/mol ,写出工业上以CO2、H2合成CH3OH的热化学方程式:
(2)已知:2H2(g)+O2(g)=2H2O(g) △H=-483 kJ·mol -1
N2(g)+2O2(g)=2NO2(g) △H=+68kJ·mol -1
则H2还原NO2生成水蒸气的热化学方程式为
(3)在25℃、101 kPa 时,7.80 g C6H6(l)燃烧生成CO2(g)和H2O(1),放出 326.04 kJ的热量,则表示C6H6的燃烧热的热化学方程式为
【知识点】 热化学方程式书写及正误判断解读 盖斯定律的应用解读
试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 仪器使用与实验安全 实验安全 | |
| 2 | 0.85 | 物质的量浓度计算-溶液配制有关计算 一定物质的量浓度的溶液的配制 配制一定物质的量浓度溶液的综合考查 | |
| 3 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 4 | 0.65 | 限定条件下的离子共存 | |
| 5 | 0.85 | 氧化还原反应基本概念 氧化性、还原性强弱的比较 | |
| 6 | 0.65 | 铝 铝与强碱溶液反应 铝的钝化 电解法制取铝 | |
| 7 | 0.65 | 二氧化硅与二氧化碳结构与性质的比较 硅酸的化学性质 硅酸钠与二氧化碳反应 | |
| 8 | 0.65 | 化学用语综合判断 | |
| 9 | 0.94 | 元素周期表提供的元素信息 原子序数与元素在周期表中的位置的关系分析及利用 | |
| 10 | 0.85 | 同周期元素性质递变规律 同主族元素性质递变规律 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |
| 11 | 0.64 | 分子结构与性质 | |
| 12 | 0.65 | 化学反应热的计算 盖斯定律与热化学方程式 | |
| 13 | 0.85 | 探究铁的吸氧腐蚀 | |
| 14 | 0.65 | 阿伏加德罗常数的求算 | |
| 15 | 0.65 | 中和热 燃烧热 热化学方程式书写及正误判断 | |
| 16 | 0.65 | 盖斯定律及其有关计算 | |
| 17 | 0.65 | 离子方程式的正误判断 | |
| 18 | 0.85 | 铁与强氧化性酸的反应 铁与非氧化性酸的反应 铁与铁离子反应 | |
| 19 | 0.65 | 化学实验方案的设计与评价 | |
| 20 | 0.65 | 溶液的酸碱性与pH 盐类水解的应用 | |
| 21 | 0.65 | 元素周期律的应用 | |
| 22 | 0.65 | 原电池、电解池综合考查 | |
| 23 | 0.65 | 金属的电化学腐蚀与防护 | |
| 24 | 0.65 | 化学能与物质稳定性之间的关系 中和热概念 表示燃烧热的热化学方程式书写 反应热大小比较 | |
| 25 | 0.65 | 原电池原理 原电池原理的应用 原电池电子流向判断及应用 | |
| 26 | 0.65 | 氯碱工业 | |
| 27 | 0.65 | 新型电池 | |
| 28 | 0.65 | 海水资源综合利用 | |
| 29 | 0.85 | 常见金属的冶炼 | |
| 30 | 0.65 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 二、解答题 | |||
| 31 | 0.65 | 无机综合推断 铝与强碱溶液反应 铁的其他化合物 | 无机推断题 |
| 33 | 0.65 | 探究物质组成或测量物质的含量 综合实验设计与评价 | 实验探究题 |
| 三、填空题 | |||
| 32 | 0.65 | 元素周期律、元素周期表的推断 | |
| 34 | 0.65 | 原电池原理 电解原理的应用 | |
| 35 | 0.65 | 热化学方程式书写及正误判断 盖斯定律的应用 | |



