回答下列问题:
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是_____ 。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式_____ 。
②每生成1molFeO 转移
转移_____ 个电子。
(3) 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为_____ 。
Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为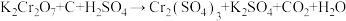 。
。
(4)配平该反应方程式:_____ 。
(5)此反应的氧化产物为_____ 。
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:_____ 。
(7)某条件下, 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为_____ 。
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式
②每生成1molFeO
 转移
转移(3)
 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为
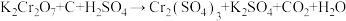 。
。(4)配平该反应方程式:
(5)此反应的氧化产物为
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:
(7)某条件下,
 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为
更新时间:2024-01-31 21:55:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请写出以下化学反应的离子方程式。
(1)实验室制备氢氧化铁胶体________
(2)食醋除水垢(主要成分为碳酸钙)________
(3)稀硫酸除铁锈________
(4)氨水吸收烟气中的二氧化硫________
(5)胃舒平(有效成分为氢氧化铝)治疗胃酸过多________
(1)实验室制备氢氧化铁胶体
(2)食醋除水垢(主要成分为碳酸钙)
(3)稀硫酸除铁锈
(4)氨水吸收烟气中的二氧化硫
(5)胃舒平(有效成分为氢氧化铝)治疗胃酸过多
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某校化学小组同学将氯气通入NaOH溶液中,制得一种消毒液,运用下列实验,检测该消毒液的性质:
①将少量消毒液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测消毒液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向消毒液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。请回答以下问题:
(1)用离子方程式表示制备该消毒液的原理___________ 。
(2)该消毒液中大量存在的阴离子有OH-、___________ 、___________ 。
(3)实验①表现出该消毒液具有___________ 性。
(4)实验②用pH试纸检测消毒液的操作是___________ 。
(5)实验③中涉及反应的离子方程式为___________ 。
①将少量消毒液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测消毒液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向消毒液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。请回答以下问题:
(1)用离子方程式表示制备该消毒液的原理
(2)该消毒液中大量存在的阴离子有OH-、
(3)实验①表现出该消毒液具有
(4)实验②用pH试纸检测消毒液的操作是
(5)实验③中涉及反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】胆矾(CuSO4·5H2O)又名蓝矾,是化学工业、医药领域中的常见物质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加_______ 至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;
③另取少量①所得溶液,加入足量的_______ 溶液,出现白色沉淀;
④取③中所得上层清液,加入_______ 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=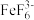 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6
请回答:步骤①中,加入足量NaF溶液的可能原因是_______ ,若不加NaF溶液,可导致最终的测量值_______ (填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为_______ ; 若Na2S2O3标准溶液的平均用量为10.00 mL,则产品中胆矾的质量分数为_______ 。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加
③另取少量①所得溶液,加入足量的
④取③中所得上层清液,加入
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=
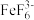 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6请回答:步骤①中,加入足量NaF溶液的可能原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,易溶于水且不与水反应。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。
(1)该反应中氧化剂的化学式是____ 。
(2)用双线桥标出上述反应的电子转移情况____ 。
(3)标准状况下44.8 mL的ClO2恰好能与50 mL 0.1 mol·L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为____ ,此过程说明ClO2具有____ (填“氧化”或“还原”)性。
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的____ 倍。
(5)新制备的ClO2中常含有少量Cl2,检验其中是否含有Cl2的实验方法是____ 。
(1)该反应中氧化剂的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)标准状况下44.8 mL的ClO2恰好能与50 mL 0.1 mol·L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(4)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同时的电镀废水,所需Cl2的物质的量是ClO2的
(5)新制备的ClO2中常含有少量Cl2,检验其中是否含有Cl2的实验方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列10种物质:①Fe ②干冰 ③冰醋酸 ④熔融的Na2CO3 ⑤KAl(SO4)2·12H2O ⑥Cl2 ⑦盐酸 ⑧漂白粉 ⑨NaHSO4 ⑩固体SiHCl3
(1)上述物质中属于电解质的有___________ (填序号),能导电的物质有___________ (填序 号)。
(2)NaHSO4 在水溶液中的电离方程式为___________ 。
(3)SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种物质X,物质X名称为___________ 。
(4)将少量②的气体通入⑧的溶液中反应的离子方程式为___________ 。
(5)写出高温条件下①和水反应的化学方程式为___________ ,氧化剂是___________ (填化学式)。
(6)向Na2CO3溶液中滴入少量醋酸(CH3COOH)溶液,___________ (填“能”或“不能”)立即产生气体。
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和CO ,该反应离子方程式中氧化剂与还原剂的系数比为
,该反应离子方程式中氧化剂与还原剂的系数比为___________ 。
(1)上述物质中属于电解质的有
(2)NaHSO4 在水溶液中的电离方程式为
(3)SiHCl3 遇水剧烈反应生成H2SiO3、HCl 和另一种物质X,物质X名称为
(4)将少量②的气体通入⑧的溶液中反应的离子方程式为
(5)写出高温条件下①和水反应的化学方程式为
(6)向Na2CO3溶液中滴入少量醋酸(CH3COOH)溶液,
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和CO
 ,该反应离子方程式中氧化剂与还原剂的系数比为
,该反应离子方程式中氧化剂与还原剂的系数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: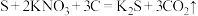 +________,
+________,_______ (完善方程式,填化学式,下同);在该反应中氧化剂是_______ ;方程式中所涉及的物质,哪些是氧化物_______ ,哪些是电解质_______ 。
(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。
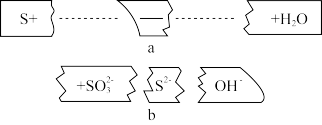
写出并配平该反应的离子方程式:_______ 。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的
 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:
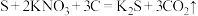 +________,
+________,(3)把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。

写出并配平该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.现有下列十种物质:①H2 ②铝 ③Na2O ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)其中,属于混合物的是_________ ,属于氧化物的是__________ ,属于单质的是____ 。(本小题均用序号作答)
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH- H2O,该离子反应对应的化学方程式为
H2O,该离子反应对应的化学方程式为____________________________________________________ 。
II.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。

(1)从物质分类标准看,“铜绿”属于________ (填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:_____________ 。
(3)请写出铜绿与盐酸反应的化学方程式:_______________________ 。
(4)上述转化过程中属于化合反应的是_____________ ,属于置换反应的是____________ 。
(1)其中,属于混合物的是
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-
 H2O,该离子反应对应的化学方程式为
H2O,该离子反应对应的化学方程式为II.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。

(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:
(3)请写出铜绿与盐酸反应的化学方程式:
(4)上述转化过程中属于化合反应的是
您最近一年使用:0次
【推荐3】对于4NH3+5O2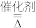 4NO+6H2O反应。
4NO+6H2O反应。
(1)被氧化的元素是________ ,被还原的元素是________ 。
(2)发生氧化反应的物质是________ ,发生还原反应的物质是________ ,还原产物是________ ,氧化产物是________ 。
(3)该反应是置换反应吗?________ (选填“是”或“不是”)。
(4)当生成30 g NO时,转移电子数为________ 。
(5)从单线桥表示电子转移的方向和数目________ 。
(6)查阅资料可知:铜和浓硫酸共热,发生反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为________ ,其中H2SO4在反应中体现____________________ 作用。
(7)请配平下列反应方程式:
_____ K2Cr2O7+____ HCl
_______ KCl+_____ CrCl3+_____ Cl2↑+______ H2O
 4NO+6H2O反应。
4NO+6H2O反应。(1)被氧化的元素是
(2)发生氧化反应的物质是
(3)该反应是置换反应吗?
(4)当生成30 g NO时,转移电子数为
(5)从单线桥表示电子转移的方向和数目
(6)查阅资料可知:铜和浓硫酸共热,发生反应Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为(7)请配平下列反应方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按照要求回答问题。
(1) 的电子式为
的电子式为_______ ,写出其用于呼吸面具做供氧剂的化学方程式:_______ 。
(2)实验室用NaOH浓溶液配制0.1 mol·L NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液_______ mL(保留一位小数),该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管、烧杯之外,还有_______ 。
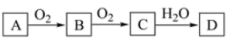
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则C→D的化学方程式:
,则C→D的化学方程式:_______ 。
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):_______ 。
(5)高铁酸钠( )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为_______ mol。
(1)
 的电子式为
的电子式为(2)实验室用NaOH浓溶液配制0.1 mol·L
 NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则C→D的化学方程式:
,则C→D的化学方程式:
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
(5)高铁酸钠(
 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3+KNO3+KOH=K2FeO4+KNO2+H2O(未配平)
方法二:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O
(1)配平方法一的化学方程式,并用双线桥标明电子转移的方向和数目:_____
Fe2O3+____KNO3+______KOH=______K2FeO4+______KNO2+______H2O
(2)方法二中的还原产物为___________ (写化学式),将方法二的化学方程式改写为离子方程式___________ ,根据反应方程式判断,氧化性:KClO___________ K2FeO4(填“>”、“<”或“=”);
(3)利用方法二制备K2FeO4,若有0.5molK2FeO4生成,转移的电子数为___________ ;
(4)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,③Br2+K2S=2KBr+S。下列说法正确的是___________。
方法一:Fe2O3+KNO3+KOH=K2FeO4+KNO2+H2O(未配平)
方法二:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O
(1)配平方法一的化学方程式,并用双线桥标明电子转移的方向和数目:
Fe2O3+____KNO3+______KOH=______K2FeO4+______KNO2+______H2O
(2)方法二中的还原产物为
(3)利用方法二制备K2FeO4,若有0.5molK2FeO4生成,转移的电子数为
(4)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,③Br2+K2S=2KBr+S。下列说法正确的是___________。
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S |
| C.反应②中氧化剂与还原剂的物质的量之比为1:8 |
| D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.现有以下物质:① 溶液;②液氨;③
溶液;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦稀硫酸;⑧
胶体;⑥铜;⑦稀硫酸;⑧ ;⑨蔗糖;
;⑨蔗糖;
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号):以上纯净物中能导电的是_______ (填序号)。
(2)⑤与⑦反应的离子方程式_______ 。
(3)制备物质⑤的方法_______ 。
Ⅱ.虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。
(4)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_______ (填字母)。

(5)下列反应方程式: 中若反应中发生氧化反应的
中若反应中发生氧化反应的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为_______ 。
 溶液;②液氨;③
溶液;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦稀硫酸;⑧
胶体;⑥铜;⑦稀硫酸;⑧ ;⑨蔗糖;
;⑨蔗糖;(1)以上物质中属于混合物的是
(2)⑤与⑦反应的离子方程式
(3)制备物质⑤的方法
Ⅱ.虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。
(4)如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(5)下列反应方程式:
 中若反应中发生氧化反应的
中若反应中发生氧化反应的 个数为12,则反应中转移的电子数为
个数为12,则反应中转移的电子数为
您最近一年使用:0次

 还原,则元素X在还原产物中的化合价是
还原,则元素X在还原产物中的化合价是

