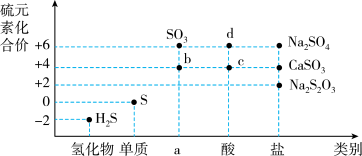
物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据图正确回答下列含硫物质有关问题。
(1)a对应物质的类别是___________ ;
(2)图中 b、c、d 这三种物质中属于弱电解质的是_______________ (填化学式)。
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。
①是检验SO2的___________ 。
②中的现象褪色,体现了SO2的___________ 。
③中产生淡黄色浑浊,体现了SO2的___________ 。
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
产生沉淀的化学式是:①___________ ,②___________ 。
(6)写出SO2与氢氧化钠溶液反应的化学方程式______________ 。
(1)a对应物质的类别是
(2)图中 b、c、d 这三种物质中属于弱电解质的是
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
| A.Na2S+S | B.Na2SO3+S |
| C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。

①是检验SO2的
②中的现象褪色,体现了SO2的
③中产生淡黄色浑浊,体现了SO2的
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
| 加入的物质 | H2O2 | 氨水 |
| 沉淀的化学式 | ① | ② |
(6)写出SO2与氢氧化钠溶液反应的化学方程式
更新时间:2024-04-24 08:41:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人野兽”(即能与盐酸反应的物质或者水溶液),盐酸必须避开它们,否则就无法通过。
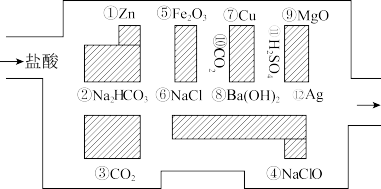
请回答下列问题:
(1)请你帮助它走出迷宫(用图中物质的序号按先后顺序连接起来表示所走的路线)___________ 。
(2) 俗称
俗称___________ ,其水溶液显___________ 性(填“酸”“碱”或“中”);除去碳酸钠固体中碳酸氢钠的反应的化学方程式为___________ 。
(3)化学工业为疫情防控提供了强有力的物质支撑,“84消毒液”是一种以次氯酸钠为主要成分的含氯消毒剂,主要用于物体表面和环境等的消毒,可有效灭活新冠病毒,这是利用了 的强
的强___________ 性(填“氧化”或“还原”);洁厕灵(主要成分是盐酸)和84消毒液不能混用,否则产生有毒氯气,其离子方程式为___________ 。
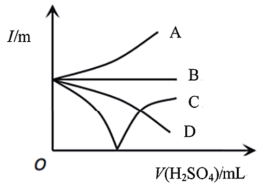
(4)向 溶液中缓缓加入
溶液中缓缓加入 直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的
直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的___________ (填字母)曲线表示。

请回答下列问题:
(1)请你帮助它走出迷宫(用图中物质的序号按先后顺序连接起来表示所走的路线)
(2)
 俗称
俗称(3)化学工业为疫情防控提供了强有力的物质支撑,“84消毒液”是一种以次氯酸钠为主要成分的含氯消毒剂,主要用于物体表面和环境等的消毒,可有效灭活新冠病毒,这是利用了
 的强
的强(4)向
 溶液中缓缓加入
溶液中缓缓加入 直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的
直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。回答下列问题。
(1)按照物质的分类方法,FeCl3应属于_________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为______________ ;判断胶体制备是否成功可利用胶体的____________ ;某同学在实验中没有使用蒸馏水,而是用自来水,结果生成了红褐色沉淀,原因是________________ 。
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。 其中孔雀石颜料属于_________ (填“纯净物”或"混合物”),请写出Cu(OH)2·CuCO3与盐酸反应的化学方程式________________ 。
(1)按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。 其中孔雀石颜料属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】N、Cu及其相关化合物用途非常广泛。回答下列问题:
(1)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3)。某些汽车安全气囊中装有叠氮化钠。
①叠氮酸在水溶液中解离出H+和_____________ (填化学符号)。
②叠氮酸与NaOH溶液的反应属于___________ (填反应类型)。
③叠氮化钠受热分解时产生两种单质,该反应的化学方程式为___________ 。
(2)孔雀石主要成分的化学式为Cu2(OH)2CO3[也可写作Cu(OH)2·CuCO3];蓝铜矿主要成分的化学式为Cu(OH)2·2CuCO3。
①孔雀石在树木燃烧的熊熊烈火中灼烧时,出现了“绿→黑→ 红”的颜色变化,我们的祖先在燃烧后的灰烬中发现了Cu。请用两个化学方程式说明颜色变化的原因:____________________ 、_______________ (提示:两个反应的反应类型分别为分解反应和置换反应)。
②用一定量的铁与足量稀H2SO4及足量CuO也可制单质铜,有人设计以下两种方案。
方案I :Fe H2
H2 Cu
Cu
方案II:CuO CuSO4
CuSO4 Cu
Cu
若实验过程中,根据一般的实验方法和实验操作规则进行操作,则两者制得单质铜的量为方案I_________ 方案 II(填“>”、“<”或“=”)。
③宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料,青色来自蓝铜矿颜料。下列说法错误的是_________ (填序号)。
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料耐酸耐碱
C.孔雀石、蓝铜矿颜料不易被空气氧化
D. Cu(OH)2·CuCO3中铜的质量分数高于Cu(OH)2·2CuCO3
(1)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3)。某些汽车安全气囊中装有叠氮化钠。
①叠氮酸在水溶液中解离出H+和
②叠氮酸与NaOH溶液的反应属于
③叠氮化钠受热分解时产生两种单质,该反应的化学方程式为
(2)孔雀石主要成分的化学式为Cu2(OH)2CO3[也可写作Cu(OH)2·CuCO3];蓝铜矿主要成分的化学式为Cu(OH)2·2CuCO3。
①孔雀石在树木燃烧的熊熊烈火中灼烧时,出现了“绿→黑→ 红”的颜色变化,我们的祖先在燃烧后的灰烬中发现了Cu。请用两个化学方程式说明颜色变化的原因:
②用一定量的铁与足量稀H2SO4及足量CuO也可制单质铜,有人设计以下两种方案。
方案I :Fe
 H2
H2 Cu
Cu方案II:CuO
 CuSO4
CuSO4 Cu
Cu若实验过程中,根据一般的实验方法和实验操作规则进行操作,则两者制得单质铜的量为方案I
③宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料,青色来自蓝铜矿颜料。下列说法错误的是
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料耐酸耐碱
C.孔雀石、蓝铜矿颜料不易被空气氧化
D. Cu(OH)2·CuCO3中铜的质量分数高于Cu(OH)2·2CuCO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】若以I2(l)为溶剂,下列四个反应中何者为歧化、反歧化、溶剂合、复分解:
(1)KI+IBr=KBr+I2_______
(2)NaCN+I2=NaI+ICN_______
(3)KI+I2=KI3_______
(4)PbC12+2KI=PbI2+2KCl_______
(1)KI+IBr=KBr+I2
(2)NaCN+I2=NaI+ICN
(3)KI+I2=KI3
(4)PbC12+2KI=PbI2+2KCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被_______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
①上表所列铜化合物中,推断铜的质量百分含量最高的是_______ 。
②CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有_______ 。
③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是_______ 。
④Cu2(OH)2 CO3与稀硫酸反应的化学方程式为_______ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu2S | Cu2(OH)2CO3 |
①上表所列铜化合物中,推断铜的质量百分含量最高的是
②CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2
 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2
 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是④Cu2(OH)2 CO3与稀硫酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知反应:①KClO3 + HCl-----Cl2↑+ KCl + H2O
②Cl2+2KI═2KCl+I2
③I2+5Cl2+6H2O═2HIO3+10HCl
回答下列问题:
(1)反应③中氧化产物是__________ (填化学式)
(2)配平反应①并用单线桥法表示该反应中电子转移的方向和数目___KClO3 + ___HCl=_____Cl2↑+____ KCl + ____H2O,______________ 。
(3)下列说法正确的是______ 。
A. 反应③中氧化剂和还原剂的物质的量之比为1:5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl-> I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(4)实验室用反应①可以制取Cl2,若反应消耗24.5g KClO3,则至少需用________ mL 6mol/LNaOH溶液吸收产生的氯气。写出吸收氯气的离子方程式:______________ 。
②Cl2+2KI═2KCl+I2
③I2+5Cl2+6H2O═2HIO3+10HCl
回答下列问题:
(1)反应③中氧化产物是
(2)配平反应①并用单线桥法表示该反应中电子转移的方向和数目___KClO3 + ___HCl=_____Cl2↑+____ KCl + ____H2O,
(3)下列说法正确的是
A. 反应③中氧化剂和还原剂的物质的量之比为1:5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl-> I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(4)实验室用反应①可以制取Cl2,若反应消耗24.5g KClO3,则至少需用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
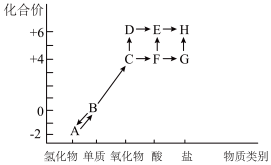
【推荐1】研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。
(1)G是一种由四种元素组成的钠盐,它的电离方程式是___________ 。
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是___________ 。
(3)检验H中阴离子的实验操作及现象是_____________ 。
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式___________ 。
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
(5)实验i选择的试剂是①和___________ (填序号),证明实现转化的现象是___________ ,该转化利用了Na2SO3的___________ 性。
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为_____________ 。
I.以下是硫元素形成物质的“价—类”二维图及含硫物质相互转化的部分信息。

(1)G是一种由四种元素组成的钠盐,它的电离方程式是
(2)C有毒,实验室可以用过量的NaOH溶液吸收,反应的离子方程式是
(3)检验H中阴离子的实验操作及现象是
(4)C→F→E是造成酸雨的可能途径,请写出其中的化学方程式
II.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液②浓硫酸③Na2S溶液④稀硫酸⑤酸性KMnO4溶液⑥品红溶液⑦铜片
| 实验序号 | 预期转化 | 选择试剂(填序号) | 证明实现转化的现象 |
| i |  → → | ||
| ii | ①、③、④ | 淡黄色沉淀 | |
| iii |  → → | ②、⑦、⑥ |
(5)实验i选择的试剂是①和
(6)实验ii实现了-2价S向0价S的转化,相应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学物质在生活、生产中扮演着非常重要的角色。现有下列物质:①硅胶、②浓硫酸、③稀 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,按要求填空。
,按要求填空。
(1)上面物质可用作食品干燥剂的是______ ,“84”消毒液的有效成分是______ ,能使蔗糖变黑的是______ 。(填序号)
(2)硫酸具有A酸性、B吸水性、C脱水性、D强氧化性,以下过程主要表现了浓硫酸的哪些性质,请将选项字母 填在下列各小题的横线上:
①浓硫酸使蓝色硫酸铜晶体变白色______ ,②热的浓硫酸与铜片反应______ 。(填选项字母)
(3)稀 和Cu反应的离子方程式为
和Cu反应的离子方程式为____________ 。
(4)工业上用石英砂(主要为 )和焦炭制取粗硅,其反应的化学方程式为
)和焦炭制取粗硅,其反应的化学方程式为____________ 。盛装NaOH等碱性溶液的试剂瓶应使用橡胶塞,不用玻璃塞,其原因是____________ (用化学方程式表示)。
(5)实验室利用含 的溶液吸收
的溶液吸收 ,从而实现
,从而实现 的回收利用。写出
的回收利用。写出 与
与 在水溶液中发生反应的离子方程式:
在水溶液中发生反应的离子方程式:____________ 。
 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,按要求填空。
,按要求填空。(1)上面物质可用作食品干燥剂的是
(2)硫酸具有A酸性、B吸水性、C脱水性、D强氧化性,以下过程主要表现了浓硫酸的哪些性质,请将
①浓硫酸使蓝色硫酸铜晶体变白色
(3)稀
 和Cu反应的离子方程式为
和Cu反应的离子方程式为(4)工业上用石英砂(主要为
 )和焦炭制取粗硅,其反应的化学方程式为
)和焦炭制取粗硅,其反应的化学方程式为(5)实验室利用含
 的溶液吸收
的溶液吸收 ,从而实现
,从而实现 的回收利用。写出
的回收利用。写出 与
与 在水溶液中发生反应的离子方程式:
在水溶液中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)SO2使橙色溴水褪色的化学方程式:___________
(2)铜与浓硫酸加热制SO2的化学方程式:________
(3)草酸(弱酸H2C2O4)使酸性高锰酸钾褪色放出CO2气体的离子方程式:___________
(4)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
①______ +________ →________ +________ +________ +H2O
②反应物中发生氧化反应的物质是________ ,被还原的元素是________ 。
③反应中1 mol氧化剂________ (填“得到”或“失去”)________ mol电子。
④请将反应物的化学式及配平后的系数填入下列相应的位置中:
________ +________ →
(5)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH-=Fe3O4+S4O
+O2+xOH-=Fe3O4+S4O +2H2O。请回答下列问题。
+2H2O。请回答下列问题。
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是____ 。
②反应的化学方程式中x=________ 。
③每生成1 mol Fe3O4,反应转移的电子为________ mol,被Fe2+还原的O2的物质的量为________ mol。
(2)铜与浓硫酸加热制SO2的化学方程式:
(3)草酸(弱酸H2C2O4)使酸性高锰酸钾褪色放出CO2气体的离子方程式:
(4)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
①
②反应物中发生氧化反应的物质是
③反应中1 mol氧化剂
④请将反应物的化学式及配平后的系数填入下列相应的位置中:
(5)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O
 +O2+xOH-=Fe3O4+S4O
+O2+xOH-=Fe3O4+S4O +2H2O。请回答下列问题。
+2H2O。请回答下列问题。①水热法制备Fe3O4纳米颗粒的反应中,还原剂是
②反应的化学方程式中x=
③每生成1 mol Fe3O4,反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某学生对SO2与漂粉精的反应进行实验探究:
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为_______ 。
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是_______ (选填编号)。
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)_______ ;_______ 。
(4)现象ii中,黄绿色气体是_______ (写化学式)。资料显示,漂粉精在酸性条件下可发生反应并生成黄绿色气体,写出反应的离子方程式:_______ 。
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是_______ (写化学式)。
| 操作 | 现象 |
| 取 4g 漂粉精固体,加入 100mL 水 | 部分固体溶解,溶液略有颜色。 |
| 过滤,测漂粉精溶液的pH | pH 试纸:先变蓝(pH约为12),后褪色。 |
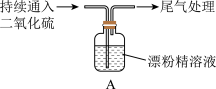 | i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去。 |
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)
(4)现象ii中,黄绿色气体是
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质类别与元素化合价是研究物质性质的两个视角,下列是硫元素及其化合物的“价类二维图”。
I.根据要求回答下列问题:
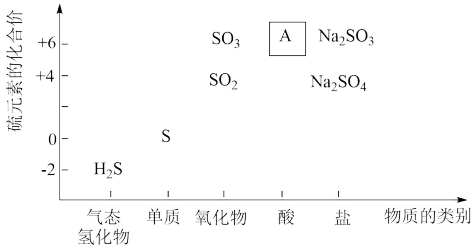
(1)写出图中A的化学式_______ 。
(2)SO2属于_______ (填“酸性”或“碱性”)氧化物,因此可与CaO、_______ (写出与CaO不同类别的一个具体物质)等反应。请写出CaO除去燃煤产生的SO2的化学方程式_______ (两个方程式)。
(3)重庆八中小王同学预测SO2具有还原性,其理论依据是_______ ,将SO2通入酸性高锰酸钾溶液中,下列实验事实能够证实SO2具有还原性的是_______ (填序号)。
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
II.硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生Cu(NO3)2以外,还产生了NO与NO2两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):
(4)反应产生的混合气体中,产生NO气体的体积为_______ L(标准状况下测定)。
(5)反应后, 的物质的量浓度为
的物质的量浓度为_______ mol/L。
I.根据要求回答下列问题:

(1)写出图中A的化学式
(2)SO2属于
(3)重庆八中小王同学预测SO2具有还原性,其理论依据是
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
II.硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生Cu(NO3)2以外,还产生了NO与NO2两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):
(4)反应产生的混合气体中,产生NO气体的体积为
(5)反应后,
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒(Se),有抗癌、抗衰老等重要功能。请回答下列问题。
(1)34Se的原子结构示意图为___________ ,其在周期表中的位置为______ 。
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是___________ (填标号)。
A.还原性:S2->Se2-
B.浓硒酸不可能具有强氧化性、吸水性
C.稳定性:H2Se>H2S>H2O
D.氧化性:O2>Se
②SO2通入SeO2的水溶液中会生成不溶于水的Se,该反应的化学方程式为___________ ;Se能与浓硫酸反应生成SO2和SeO2,则浓硫酸、SO2和SeO2三者中,氧化性最弱的为___________ 。
(1)34Se的原子结构示意图为
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是
A.还原性:S2->Se2-
B.浓硒酸不可能具有强氧化性、吸水性
C.稳定性:H2Se>H2S>H2O
D.氧化性:O2>Se
②SO2通入SeO2的水溶液中会生成不溶于水的Se,该反应的化学方程式为
您最近一年使用:0次



