一种利用废铜渣(主要成分为 ,及少量的
,及少量的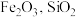 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
 ,及少量的
,及少量的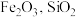 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
A.“酸浸”所得滤渣的主要成分为 |
B.向“沉铁”后的滤液中加入乙醇,析出的深蓝色晶体为 |
C.“沉铜”过程中发生了氧化还原反应, 是还原剂 是还原剂 |
D.“转化”后的滤液中含有的阳离子为 和 和 |
更新时间:2024-05-26 00:04:20
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某兴趣小组对化合物M开展探究实验。
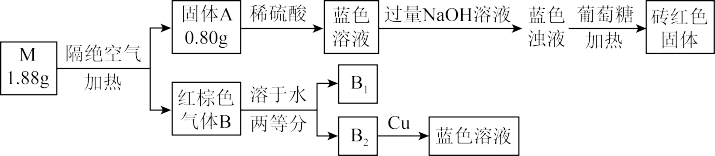
已知:①M是强酸盐,由三种元素组成;两种元素组成的固体A是纯净物,气体B是混合物。
②酚酞溶液作指示剂,用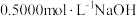 溶液滴定
溶液滴定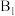 ,消耗20.00mLNaOH溶液。
,消耗20.00mLNaOH溶液。
下列推断正确的是

已知:①M是强酸盐,由三种元素组成;两种元素组成的固体A是纯净物,气体B是混合物。
②酚酞溶液作指示剂,用
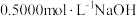 溶液滴定
溶液滴定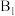 ,消耗20.00mLNaOH溶液。
,消耗20.00mLNaOH溶液。下列推断正确的是
| A.砖红色固体和固体A的成分相同 |
| B.气体B溶于水的反应原子利用率为100% |
C.M是 ,物质的量为0.2mol ,物质的量为0.2mol |
| D.上述转化中包括5个氧化还原反应 |
您最近一年使用:0次
【推荐2】工业上以铬铁矿(主要成分为 )、碳酸钠、氧气、硫酸为原料生产重铬酸钠
)、碳酸钠、氧气、硫酸为原料生产重铬酸钠 ,其主要反应为:(1)高温下发生反应:
,其主要反应为:(1)高温下发生反应: (未配平)
(未配平)
(2) ;下列说法正确的是
;下列说法正确的是
 )、碳酸钠、氧气、硫酸为原料生产重铬酸钠
)、碳酸钠、氧气、硫酸为原料生产重铬酸钠 ,其主要反应为:(1)高温下发生反应:
,其主要反应为:(1)高温下发生反应: (未配平)
(未配平)(2)
 ;下列说法正确的是
;下列说法正确的是| A.反应(1)和(2)均为氧化还原反应 |
B.反应(1)中每生成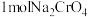 时电子转移 时电子转移 |
C.高温下, 的氧化性强于 的氧化性强于 ,弱于 ,弱于 |
D.反应(1)中参加反应的 与生成的 与生成的 物质的量之比 物质的量之比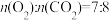 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
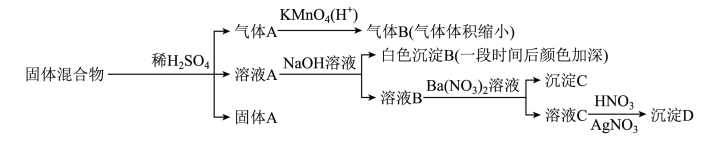

| A.气体A中一定含有H2 |
| B.该固体混合物中Fe2O3和Fe至少有其中一种 |
| C.固体A中可能含有BaSO4 |
| D.该固体混合物一定含有Na2CO3、Na2SO3、BaCl2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】以废旧电路板为原料制备硫酸铜可以变废为宝。下图是某科研小组设计的工艺流程(流程中 RH 为萃取剂),下列说法不正确的是


| A.“粉碎”可以增大反应的接触面积,提高浸取速率和铜的浸取率 |
| B.“浸取”发生的离子反应为 Cu+H2O2+2NH3 +2NH4+=Cu(NH3)42++2H2O |
| C.工艺流程中循环使用的物质有 NH3、NH4Cl、RH 和有机溶剂 |
| D.从硫酸铜溶液获得纯净的硫酸铜晶体的操作是:加入适量乙醇,蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】已知:室温时,饱和 溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5;
溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5; 不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是

 溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5;
溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5; 不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
| A.将浓硫酸稀释为25%稀硫酸,所需玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、容量瓶 |
B.操作Ⅱ中用硫酸酸化至pH=2的主要目的是抑制 的水解 的水解 |
C.操作Ⅱ中,通入 至饱和的目的是使 至饱和的目的是使 转化为SnS沉淀并防止 转化为SnS沉淀并防止 被氧化 被氧化 |
| D.操作Ⅳ中所得的晶体可用乙醇洗去晶体表面附着的水 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】氧杂环丁基叠氮聚合物制备反应原理如图:





下列说法错误的是





下列说法错误的是
| A.反应①属于开环聚合反应 | B.反应①的催化剂中含有配位键 |
| C.可用红外光谱仪检测叠氮聚合物的生成 | D.生成1mol叠氮聚合物需要消耗2molNaN3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】 溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
 溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓
溶于一定量水中得a溶液,呈浅棕黄色;a溶液加入少量浓 得溶液 b,溶液b较溶液 a黄色加深。已知:
得溶液 b,溶液b较溶液 a黄色加深。已知: (黄色);浓度较小时
(黄色);浓度较小时  (用
(用 表示)几乎无色。取溶液进行如下实验,对现象分析错误的是
表示)几乎无色。取溶液进行如下实验,对现象分析错误的是A.测溶液 a的  约为1.3,证明 约为1.3,证明  发生了水解 发生了水解 |
B.向 b中加入  后,会产生白色沉淀 后,会产生白色沉淀 |
C.向 b中滴入  溶液变血红色,说明 溶液变血红色,说明  的配位键稳定性大于 的配位键稳定性大于  |
D.将溶液 a稀释,颜色变浅,主要是因为  浓度降低导致 浓度降低导致 |
您最近一年使用:0次
单选题
|
较难
(0.4)
真题
【推荐1】一种以锰尘(主要成分为 ,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯
,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯 的清洁生产新工艺流程如下:
的清洁生产新工艺流程如下: 如下表。
如下表。
下列说法错误的是
 ,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯
,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯 的清洁生产新工艺流程如下:
的清洁生产新工艺流程如下: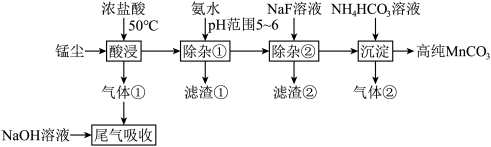
 如下表。
如下表。 |  |  |  |  |  |  |  |
 |  |  | 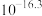 |  |  | 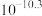 | 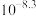 |
| A.酸浸工序中产生的气体①为氯气 |
B.滤渣①主要成分为 和 和 |
C.除杂②工序中逐渐加入 溶液时,若 溶液时,若 浓度接近,则 浓度接近,则 先析出 先析出 |
D.沉淀工序中发生反应的离子方程式为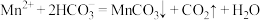 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】铋(Bi)及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等) 为原料,采用湿法治金制备精铋工艺流程如下:
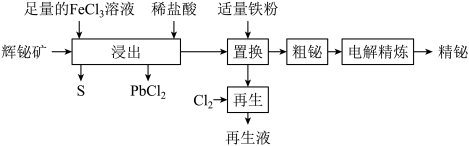
下列说法错误的是

下列说法错误的是
| A.“浸出”产生S 的主要离子反应为 6Fe3++Bi2S3=6Fe2++2Bi3++3S |
| B.“浸出”时使用稀盐酸主要目的是还原杂质 PbO2 |
| C.“电解精炼”时,粗铋应与电源的正极相连 |
| D.再生液可以加入“浸出”操作中循环利用 |
您最近一年使用:0次



 存在时,活性炭吸附脱除
存在时,活性炭吸附脱除 的反应方程式为
的反应方程式为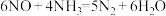 。研究发现:活性炭的表面含有羧基等含氧官能团,活性炭含氧官能团化学吸附
。研究发现:活性炭的表面含有羧基等含氧官能团,活性炭含氧官能团化学吸附
 原子与羧基中的
原子与羧基中的 原子发生作用
原子发生作用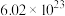 个
个 、
、 和
和 ,含少量的
,含少量的 )制备钼酸钠晶体(
)制备钼酸钠晶体( )的简化流程如图所示。下列说法错误的是
)的简化流程如图所示。下列说法错误的是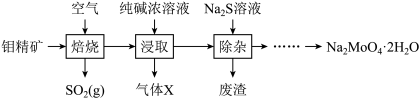
 和
和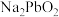 。
。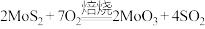
 ,可获得副产品亚硫酸钠
,可获得副产品亚硫酸钠

