解题方法
1 . 某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
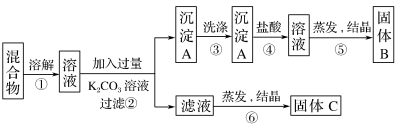
(1)操作①用玻璃棒搅拌的目的是___________ ;操作②所需的玻璃仪器有烧杯、玻璃棒、__________ 。
(2)B的化学式为___________ 。
(3)该方案的明显失误是因某一步设计不当而使分离的产物KCl不纯,该步骤是___________ (填序号),改进措施是往滤液中滴加过量___________ 以除去多余的杂质离子再结晶。
(4)写出④对应的化学反应方程式___________ 。

(1)操作①用玻璃棒搅拌的目的是
(2)B的化学式为
(3)该方案的明显失误是因某一步设计不当而使分离的产物KCl不纯,该步骤是
(4)写出④对应的化学反应方程式
您最近一年使用:0次
2 . 碳一化工指用CO、CH4等含有1个碳原子的物质合成含2个或多个碳原子的化学工艺。下列是碳一化工的一段生产过程:

回答下列问题:
(1)产物A中有多种物质,其中分子构型为正四面体形的电子式为___________ ,写出生成该物质的化学方程式___________ ,产物B的名称为___________ 。
(2)写出上述流程中制备CH3CH2OH的反应方程式___________ ,上述反应两种产物都能与钠反应,其中反应比较缓和的是___________ (写分子式)。
(3)CO可与CH3OH反应制备乙酸:
CO(g)+CH3OH(g) CH3COOH(g) ΔH=-137.9kJ·mol-1
CH3COOH(g) ΔH=-137.9kJ·mol-1
升高温度,生成CH3COOH速率___________ (填"增大"、“减小”或“不变”,下同),1mol CO与1mol CH3OH在上述条件下密闭容器中反应,放出的热量___________ 137.9kJ(填"大于"、“小于”或"等于"),生成的乙酸中常含有副产物CH3COOCH3,除去副产物的方法是___________ 。

回答下列问题:
(1)产物A中有多种物质,其中分子构型为正四面体形的电子式为
(2)写出上述流程中制备CH3CH2OH的反应方程式
(3)CO可与CH3OH反应制备乙酸:
CO(g)+CH3OH(g)
 CH3COOH(g) ΔH=-137.9kJ·mol-1
CH3COOH(g) ΔH=-137.9kJ·mol-1升高温度,生成CH3COOH速率
您最近一年使用:0次
3 . 工业上用氯化铁腐蚀铜箔制造电路板。某实验小组为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
(1)试剂a与腐蚀废液反应的离子方程式为_____________ 。
(2)试剂b是_____________ ,操作Ⅱ为_____________ 。滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为_____________ 。上述流程中操作Ⅲ包括在HCl气流中蒸发浓缩、_____________ 、过滤、洗涤。

回答下列问题:
(1)试剂a与腐蚀废液反应的离子方程式为
(2)试剂b是
您最近一年使用:0次
22-23高一上·山西朔州·期末
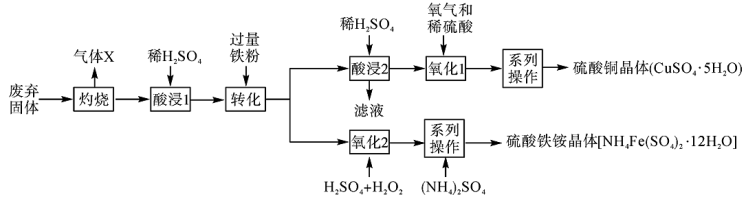
4 . 某实验小组同学利用某工业废弃矿石(主要成分为CuS和Fe2O3,其他成分不参与反应)制备硫酸铜晶体与硫酸铁铵晶体,工艺流程如下图所示:
已知: 。
。
回答下列问题:
(1)气体X的名称为_______ 。
(2)“酸浸1”过程中红色固体被溶解的化学方程式为_______ 。
(3)“酸浸2”得到的滤液为_______ (填主要物质的化学式)溶液,可以转移到_______ 操作工序中循环利用。
(4)“氧化2”过程发生反应的离子方程式为_______ ,实际操作时,所加 的量要比理论计算值多,可能原因是
的量要比理论计算值多,可能原因是_______ 。
(5)“系列操作”包括蒸发浓缩、_______ 、过滤、洗涤、干燥。
(6)若称取25.6 kg废弃矿石经过上述流程最终得到25kg硫酸铜晶体,则矿石中Cu元素的质量分数为_______ %。

已知:
 。
。回答下列问题:
(1)气体X的名称为
(2)“酸浸1”过程中红色固体被溶解的化学方程式为
(3)“酸浸2”得到的滤液为
(4)“氧化2”过程发生反应的离子方程式为
 的量要比理论计算值多,可能原因是
的量要比理论计算值多,可能原因是(5)“系列操作”包括蒸发浓缩、
(6)若称取25.6 kg废弃矿石经过上述流程最终得到25kg硫酸铜晶体,则矿石中Cu元素的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。
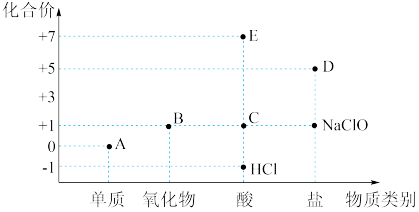
回答下列问题:
(1)已知D可用于实验室制 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是___________ (填化学式)。
(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为___________ 。
(3)取10mL某84消毒液(有效成分NaClO含量为14.9g/L),加水稀释,配制成100mL稀溶液。
①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、___________ 。
②稀释后的溶液中,NaClO的物质的量浓度为___________  。
。
(4)工业上“侯氏制碱法”以NaCl、 、
、 ,及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
,及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
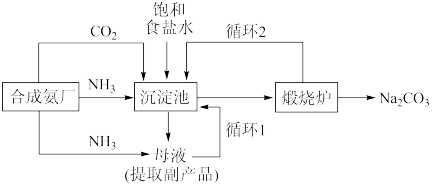
①实验室分离出沉淀的操作名称是___________ ;煅烧炉里进行的化学反应方程式为:___________ 。
②检验产品 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有___________ 。

回答下列问题:
(1)已知D可用于实验室制
 ,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是
,焰色试验时其火焰呈现紫色。A、B、C、D四种物质中,属于电解质的是(2)将E滴入碳酸氢钠溶液中,有大量气泡产生,该反应的离子方程式为
(3)取10mL某84消毒液(有效成分NaClO含量为14.9g/L),加水稀释,配制成100mL稀溶液。
①配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②稀释后的溶液中,NaClO的物质的量浓度为
 。
。(4)工业上“侯氏制碱法”以NaCl、
 、
、 ,及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
,及水等为原料制备纯碱,生产纯碱的工艺流程示意图如下:
①实验室分离出沉淀的操作名称是
②检验产品
 中是否含有氯离子,需要的试剂有
中是否含有氯离子,需要的试剂有
您最近一年使用:0次
6 . NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:

(1)写出上述实验过程中所用试剂:试剂①___________ ;试剂③___________ 。
(2)判断试剂①已过量的方法是:___________ 。
(3)用化学方程式表示加入试剂②的作用:___________ 。
(4)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉___________ (填“能”或“不能”,下同)透过半透膜;SO
___________ 透过半透膜。

(1)写出上述实验过程中所用试剂:试剂①
(2)判断试剂①已过量的方法是:
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉

您最近一年使用:0次
7 . 现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示。请回答下列问题:

(1)试剂X最好是_______ (填化学式)。
(2)写出步骤②的离子反应方程式_______ 。
(3)按此实验方案得到的溶液3中肯定含有_______ (填化学式)杂质;为了除这个杂质,可以向溶液3中加入过量的_______ 。
(4)为检验所得的NaNO3固体中是否含有NaCl和Na2SO4.取一定量的固体物质溶于水配成溶液:
①首先检验_______ 离子,应先加入过量的_______ ;
②将所得混合物过滤,然后在溶液中加入试剂_______ 检验另一离子。

(1)试剂X最好是
(2)写出步骤②的离子反应方程式
(3)按此实验方案得到的溶液3中肯定含有
(4)为检验所得的NaNO3固体中是否含有NaCl和Na2SO4.取一定量的固体物质溶于水配成溶液:
①首先检验
②将所得混合物过滤,然后在溶液中加入试剂
您最近一年使用:0次
11-12高二上·北京·期中
名校
解题方法
8 . 用铁、铝的混合物进行如下实验:
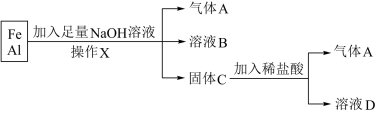
(1)操作X的名称是___________ 。
(2)气体A是___________ 。
(3)A与 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成___________ (填化学式),A在该反应中作为___________ (填“氧化剂”或“还原剂”)。
(4)溶液B中阴离子除 外还有
外还有___________ ,溶液D中存在的金属离子为___________ 。

(1)操作X的名称是
(2)气体A是
(3)A与
 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成(4)溶液B中阴离子除
 外还有
外还有
您最近一年使用:0次
2022-08-17更新
|
829次组卷
|
12卷引用:2011-2012学年北京市育园中学高二上学期期中考试化学(理)试卷
(已下线)2011-2012学年北京市育园中学高二上学期期中考试化学(理)试卷云南省盈江县民族完全中学2019-2020学年高二上学期期末考试化学试题福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题云南省丽江市宁蒗县第一中学2019—2020学年高一上学期期末考试化学试题云南省昭通市彝良县第二中学2019—2020学年高一上学期期末考试化学试题贵州省雷山县第四中学2019-2020学年高一上学期期末考试化学试题贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题第二节 金属材料 第1课时 合金黑龙江省哈尔滨市第六中学校2022—2023学年高一上学期期中考试化学试题云南省广南县第一中学校2021-2022学年高一下学期3月份考试化学试题作业(十九) 常见的合金及其应用
名校
解题方法
9 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量 Na+、Cu2+、 、Cl-、
、Cl-、 。
。
(1)下列离子中,能大量存在于该废水中的是___________(填标号)
(2)取100 mL该废水于烧杯,逐滴加入NaOH溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是Na+、___________ (用离子符号表示)。
(3)某化学社团小组成员欲除去废水样品中的Cu2+和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:

①试剂c为___________ (写化学式);溶液3所含溶质离子Cl-、___________ 。
②“分离操作”的名称是___________ 。
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为___________ 。
 、Cl-、
、Cl-、 。
。(1)下列离子中,能大量存在于该废水中的是___________(填标号)
| A.Ag+ | B.Mg2+ | C.OH- | D. |
(3)某化学社团小组成员欲除去废水样品中的Cu2+和
 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
①试剂c为
②“分离操作”的名称是
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 某试剂瓶中 溶液中含有少量
溶液中含有少量 和
和 ,请选择适当的试剂除去杂质,从而得到纯净的
,请选择适当的试剂除去杂质,从而得到纯净的 晶体和
晶体和 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。

实验室只提供如下试剂: 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液,稀
溶液,稀 ,稀
,稀 ,铁粉,铜粉,锌粒。请回答下列问题:
,铁粉,铜粉,锌粒。请回答下列问题:
(1)若沉淀A是 的混合物,试剂X的化学式为
的混合物,试剂X的化学式为_______ ,试剂a的化学式为_______ 。
(2)步骤④中涉及的操作是:_______ 、_______ 、过滤、洗涤、干燥。
(3)向溶液3中加入适量的_______ (填化学式),再结晶,从而获得 晶体。
晶体。
(4)通过过滤、洗涤得到溶液5,如何证明固体混合物已洗净_______ 。
(5)上述实验步骤③中加入过量 溶液的目的是
溶液的目的是_______ 。
 溶液中含有少量
溶液中含有少量 和
和 ,请选择适当的试剂除去杂质,从而得到纯净的
,请选择适当的试剂除去杂质,从而得到纯净的 晶体和
晶体和 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
实验室只提供如下试剂:
 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液,稀
溶液,稀 ,稀
,稀 ,铁粉,铜粉,锌粒。请回答下列问题:
,铁粉,铜粉,锌粒。请回答下列问题:(1)若沉淀A是
 的混合物,试剂X的化学式为
的混合物,试剂X的化学式为(2)步骤④中涉及的操作是:
(3)向溶液3中加入适量的
 晶体。
晶体。(4)通过过滤、洗涤得到溶液5,如何证明固体混合物已洗净
(5)上述实验步骤③中加入过量
 溶液的目的是
溶液的目的是
您最近一年使用:0次



