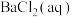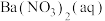1 . 某实验小组利用如图装置模拟古法制硫酸并进行 性质探究。
性质探究。
② 熔点
熔点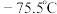 ,沸点
,沸点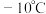 ;熔点
;熔点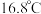 ,沸点
,沸点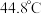 。
。
请回答下列问题:
Ⅰ.制取硫酸:实验开始前打开活塞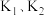 ,关闭活塞
,关闭活塞 ,通入一段时间
,通入一段时间 后,关闭活塞
后,关闭活塞 ,打开活塞
,打开活塞 ,用酒精喷灯高温加热绿矾。
,用酒精喷灯高温加热绿矾。
(1)绿矾的化学式为_________________ 。
(2)使用石英玻璃管而不使用普通玻璃管的原因是_________________ 。
(3) 装置的作用是
装置的作用是_________________ 和分离出_________________ (填化学式)。
Ⅱ.探究 的性质:在装置
的性质:在装置 中先后加入同浓度同体积不同的钡盐溶液,控制食用油油层厚度一致、通入
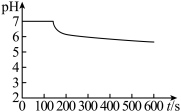
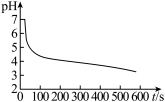
中先后加入同浓度同体积不同的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表
流速一致。四次实验分别得到如表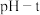 图:
图:
(4)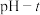 图中,用化学用语解释曲线①缓慢下降的原因
图中,用化学用语解释曲线①缓慢下降的原因_________________________________________ ;对比四组实验分析,④中发生反应_____________________________________________ (写反应的离子方程式)使溶液酸性增强, 化性增强,氧化
化性增强,氧化 的速率加快。
的速率加快。
(5)上述四次实验中有白色沉淀生成的是_________________ (填编号)。
 性质探究。
性质探究。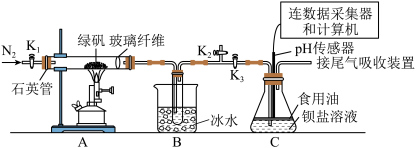
②
 熔点
熔点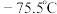 ,沸点
,沸点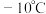 ;熔点
;熔点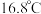 ,沸点
,沸点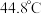 。
。请回答下列问题:
Ⅰ.制取硫酸:实验开始前打开活塞
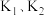 ,关闭活塞
,关闭活塞 ,通入一段时间
,通入一段时间 后,关闭活塞
后,关闭活塞 ,打开活塞
,打开活塞 ,用酒精喷灯高温加热绿矾。
,用酒精喷灯高温加热绿矾。(1)绿矾的化学式为
(2)使用石英玻璃管而不使用普通玻璃管的原因是
(3)
 装置的作用是
装置的作用是Ⅱ.探究
 的性质:在装置
的性质:在装置 中先后加入同浓度同体积不同的钡盐溶液,控制食用油油层厚度一致、通入
中先后加入同浓度同体积不同的钡盐溶液,控制食用油油层厚度一致、通入 流速一致。四次实验分别得到如表
流速一致。四次实验分别得到如表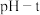 图:
图:①已煮沸的 | ②未煮沸的 |
|
|
③已煮沸的 | ④未煮沸的 |
|
|
(4)
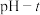 图中,用化学用语解释曲线①缓慢下降的原因
图中,用化学用语解释曲线①缓慢下降的原因 化性增强,氧化
化性增强,氧化 的速率加快。
的速率加快。(5)上述四次实验中有白色沉淀生成的是
您最近一年使用:0次
名校
2 . 根据实验操作及现象,下列结论中正确的是
| 实验操作及现象 | 结论 | |
A | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| 取一定量 样品,溶解后加入 样品,溶解后加入 溶液,产生白色沉淀。加入浓 溶液,产生白色沉淀。加入浓 ,仍有沉淀 ,仍有沉淀 | 此样品中含有 |
C | 向盛有 和 和 的试管中分别滴加浓盐酸,盛 的试管中分别滴加浓盐酸,盛 的试管中产生黄绿色气体 的试管中产生黄绿色气体 | 氧化性: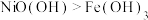 |
D | 向 溶液中通入 溶液中通入 气体,出现黑色沉淀 气体,出现黑色沉淀 | 酸性: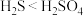 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 物质的性质决定用途。下列对应的两者关系正确的是
| A.浓硫酸具有很强的脱水性,可作气体干燥剂 |
B.氨气具有碱性,可用作烟气中 的脱除剂 的脱除剂 |
C. 溶于水后能电离出 溶于水后能电离出 ,常作烘焙糕点的膨松剂 ,常作烘焙糕点的膨松剂 |
D.常温下 在浓硝酸中钝化,可用铝质容器贮运浓硝酸 在浓硝酸中钝化,可用铝质容器贮运浓硝酸 |
您最近一年使用:0次
名校
解题方法
4 . 下列各组离子因发生氧化还原反应而不能大量共存的是
A. 、 、 、 、 | B. 、 、 、 、 |
C. 、 、 、 、 | D. 、 、 、 、 |
您最近一年使用:0次
5 . NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1 mol Cu与足量硫粉共热反应,转移的电子数为NA |
| B.1 mol Na2O2与二氧化碳充分反应,转移的电子数为2NA |
| C.浓硝酸受热分解生成NO2、N2O4共2.3g时,转移的电子数为0.5NA |
| D.100 mL 18.0 mol/L 的浓H2SO4与足量铜加热反应,可制备SO2的分子数为0.9NA |
您最近一年使用:0次
6 . 化学实验是研究和学习物质及其变化的基本方法,是科学探究的一种重要途径。下列实验操作、现象及得出的结论均正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向盛装某溶液的试管中加入NaOH溶液,加热,并将湿润的蓝色石蕊试纸靠近试管口 | 试纸未变红 | 该溶液中不存在 |
B | 用洁净的玻璃棒蘸取某溶液,在酒精灯外焰上灼烧 | 火焰呈黄色 | 该溶液中一定存在 |
C | 将稀硫酸滴入碳酸氢钠溶液中 | 产生无色无味的气体 | 非金属性:C<S |
D | 将质量、大小相同的铁片分别加入浓硝酸和稀硝酸中 | 稀硝酸中的铁片溶解并产生气泡,浓硝酸中的铁片无明显现象 | 氧化性:稀硝酸>浓硝酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-03更新
|
158次组卷
|
2卷引用:湖北省部分学校2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 近年来,“氮排放”逐渐引起人们的重视。氮及其化合物与生产生活及环境息息相关,请回答下列问题:
(1)下列环境问题与氮的氧化物排放无关的是___________。
(2)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式___________ 。
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择___________ 作为罐体材料。
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为___________ 。
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有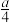 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为___________ 。
A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为___________ 。
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为___________ 。
(1)下列环境问题与氮的氧化物排放无关的是___________。
| A.酸雨 | B.光化学烟雾 | C.臭氧层空洞 | D.白色污染 |
(3)硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
①工业生产中为了盛装大量浓硝酸,可选择
A.Mg B.Al C.Fe D.Cu
②为避免硝酸生产尾气中的NO2污染环境,可以使用具有碱性的碳酸钠溶液吸收,发生反应的离子方程式为
③硝酸与金属反应会产生氮氧化物。在含有agHNO3的稀硝酸中,加入bg铁粉充分反应, 铁全部溶解并生成NO,有
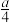 gHNO3被还原,则a:b可能为
gHNO3被还原,则a:b可能为A.2:1 B.3:1 C.4:1 D.8:3
(4)氮化硅(Si3N4)陶瓷材料可用于高温工程的部件、冶金工业等方面的高级耐火材料,可由石英与焦炭在高温的氮气流中制备,反应的化学方程式为
(5)氮的同族元素锑(Sb)可形成比纯硫酸更强的酸——氟锑酸(HSbF6),称为超酸。为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为:CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
您最近一年使用:0次
2024-04-30更新
|
112次组卷
|
2卷引用:湖北省新高考联考协作体2023-2024学年高一下学期期中考试化学试题(A)
名校
解题方法
8 . 下列离子方程式书写正确的是
A.过量的SO2通入NaClO溶液中:SO2+ClO-+H2O=HSO +HClO +HClO |
B.食醋除去少量水垢: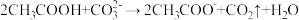 |
C.NaHCO3溶液与过量澄清石灰水混合:HCO +OH +OH +Ca2+=CaCO3 +Ca2+=CaCO3 +H2O +H2O |
D.Fe粉加入过量稀硝酸中:3Fe+8H++2NO =3Fe2++2NO =3Fe2++2NO +4H2O +4H2O |
您最近一年使用:0次
9 .  铜锌合金完全溶解于
铜锌合金完全溶解于 的浓硝酸(密度为
的浓硝酸(密度为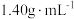 )中,得到
)中,得到 和
和 混合气体
混合气体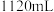 (换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入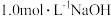 溶液,当金属离子刚好全部沉淀,得到
溶液,当金属离子刚好全部沉淀,得到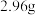 沉淀。下列说法正确的是
沉淀。下列说法正确的是
 铜锌合金完全溶解于
铜锌合金完全溶解于 的浓硝酸(密度为
的浓硝酸(密度为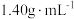 )中,得到
)中,得到 和
和 混合气体
混合气体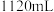 (换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入
(换算为标准状况),(忽略反应前后溶液体积变化)。向反应后的溶液中逐滴加入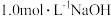 溶液,当金属离子刚好全部沉淀,得到
溶液,当金属离子刚好全部沉淀,得到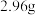 沉淀。下列说法正确的是
沉淀。下列说法正确的是A.该合金中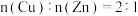 |
B.合金完全溶解时,溶液中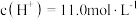 |
C. 和 和 的混合气体中, 的混合气体中, 的体积分数是 的体积分数是 |
D.刚好得到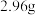 沉淀时,加入 沉淀时,加入 溶液的体积是 溶液的体积是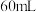 |
您最近一年使用:0次
名校
解题方法
10 . 氮、硫及其化合物的价类二维图如图所示,下列说法不正确的是
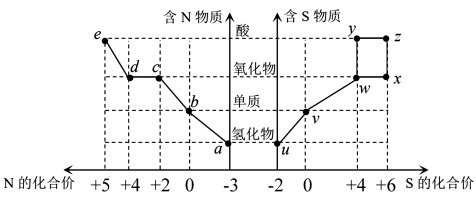
A. 和 和 与氧气反应只生成特定的氧化物 与氧气反应只生成特定的氧化物 |
B. 均能作还原剂 均能作还原剂 |
C. 均可与水反应生成酸,都属于酸性氧化物 均可与水反应生成酸,都属于酸性氧化物 |
D.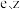 的浓溶液与铜反应分别生成氧化物 的浓溶液与铜反应分别生成氧化物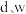 |
您最近一年使用:0次