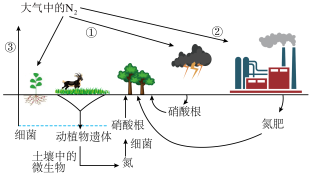
1 . 自然界的氮循环如图所示,回答下列问题。_____ 。
(2)如图为N2转化为HNO3的流程。
N2 NO
NO NO2
NO2 HNO3
HNO3
①上述物质颜色为红棕色的是_____ (用化学式表示)
②NO2转化为HNO3的反应中,NO2体现_____ 性。
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式_____ 。
(4)稀硝酸与铜反应的还原产物为_____ 。
(2)如图为N2转化为HNO3的流程。
N2
 NO
NO NO2
NO2 HNO3
HNO3①上述物质颜色为红棕色的是
②NO2转化为HNO3的反应中,NO2体现
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式
(4)稀硝酸与铜反应的还原产物为
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式不正确的是
A.铜与浓硝酸反应: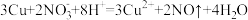 |
B.向CuCl2溶液中加入Na2S溶液: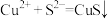 |
C.二氧化硅与氢氧化钠反应:SiO2+2OH-= +H2O +H2O |
D.SO2通入酸性KMnO4溶液中: |
您最近一年使用:0次
3 . A、B、C、D、E五种物质有如图所示的转化关系,根据信息回答下列问题:
(1)E为___________ (填名称),写出Cu与E的浓溶液反应的化学方程式___________ 。
(2)将C通入B的水溶液中,产生的现象为___________ ,体现了C的___________ 性(填“氧化”或“还原”)。
(3)将C通入酸性高锰酸钾溶液中,产生的现象为___________ ,体现了C的___________ 性(填“氧化”或“还原”)。
Ⅱ.若A为空气中含量最多的气体,完成下列问题
(4)写出B→C的化学方程式___________ 。
(5)D→E的过程中同时有C生成,标准状况下每生成22.4L的C转移___________ mol电子。写出Cu与E的浓溶液反应的化学方程式___________ 。

(1)E为
(2)将C通入B的水溶液中,产生的现象为
(3)将C通入酸性高锰酸钾溶液中,产生的现象为
Ⅱ.若A为空气中含量最多的气体,完成下列问题
(4)写出B→C的化学方程式
(5)D→E的过程中同时有C生成,标准状况下每生成22.4L的C转移
您最近一年使用:0次
名校
解题方法
4 . 常温下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶液褪色。
②甲、乙是两种酸
③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)M的化学式为___________
(2)甲的浓溶液需盛放在棕色试剂瓶中,其原因是___________ (用化学方程式表示)。
(3)在X与H2O的反应中,被氧化的X与被还原的X的物质的量之比是___________ 。
(4)欲除去Y中混有的W,下列试剂可供选用的是___________。
(5)写出M与乙的浓溶液在加热条件下反应的化学方程式:___________ 。
(6)工业上运输甲、乙两种浓溶液可选用___________ (金属名称)制运输罐,所选用的金属能做运输罐的理由是___________ 。
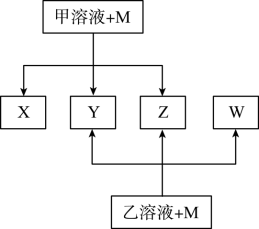
②甲、乙是两种酸
③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)M的化学式为
(2)甲的浓溶液需盛放在棕色试剂瓶中,其原因是
(3)在X与H2O的反应中,被氧化的X与被还原的X的物质的量之比是
(4)欲除去Y中混有的W,下列试剂可供选用的是___________。
| A.品红溶液 | B.酸性高锰酸钾溶液 | C.氢氧化钠溶液 | D.饱和 溶液 溶液 |
(6)工业上运输甲、乙两种浓溶液可选用
您最近一年使用:0次
名校
解题方法
5 . 常温下,下列各组离子在指定溶液中能大量共存的是
A. 氨水溶液: 氨水溶液: 、 、 、 、 、 、 |
B. 盐酸溶液: 盐酸溶液: 、 、 、 、 、 、 |
C. 酸性 酸性 溶液: 溶液: 、 、 、 、 、 、 |
D. 溶液: 溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-03-06更新
|
292次组卷
|
3卷引用:海南省海南中学2023-2024学年高一下学期合格考化学期中考试试题
名校
解题方法
6 . 某化学兴趣小组利用4份等质量的铝片(已打磨)、其他材料及电解质溶液设计了4组原电池,反应一段时间,观察并记录的部分实验结果如表所示。下列说法错误的是
| 实验编号 | ① | ② | ③ | ④ |
| 电极材料 | 铝、铜 | 铝、石墨 | 镁、铝 | 铝、铜 |
| 电解质溶液 | 稀硫酸 | 稀硫酸 | 氢氧化钠溶液 | 浓硝酸 |
| 电流表指针偏转方向 | 偏向铜 | 偏向镁 |
| A.④中电流表指针始终偏向铜 |
| B.②和③中,当生成等物质的量的气体时,外电路中转移电子的数目相等 |
| C.③中镁作正极,铝作负极 |
| D.由上述实验可知,在原电池中活泼性强的金属单质不一定作负极 |
您最近一年使用:0次
2024-02-19更新
|
165次组卷
|
3卷引用:海南省海口市海南中学2023-2024学年高一下学期4月期中考试化学试题
7 . 亚硝酰氯NOCl常用于合成洗涤剂及合成中间体,某学习小组在实验室利用2NO+Cl2 2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。

已知:①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应NOCl+H2O=HNO2+HCl。
回答下列问题:
(1)仪器a的名称是______ ,仪器a中反应的离子方程式为_____ 。
(2)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?______ (填“合理”或“不合理”),试说明原因:______ 。
(3)实验时,应先在三颈烧瓶内通入_____ (填“Cl2”或“NO”),另一种气体可以通入的标志是_____ 。
(4)实验中用NaOH溶液进行尾气处理。
①无水CaCl2的作用是______ 。
②尾气处理时,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与______ (填化学式)同时通入NaOH溶液中。
 2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
2NOCl反应制备NOCl,设计如图实验装置(夹持装置略去)。
已知:①NOCl为红褐色液体或黄色气体,熔点-64.5℃,沸点-5.5℃;
②NOCl遇水发生反应NOCl+H2O=HNO2+HCl。
回答下列问题:
(1)仪器a的名称是
(2)实验过程中,某同学发现铜与稀硝酸反应较慢,于是有同学提议用“浓硝酸”代替将A装置中的“稀硝酸”,该同学的观点是否合理?
(3)实验时,应先在三颈烧瓶内通入
(4)实验中用NaOH溶液进行尾气处理。
①无水CaCl2的作用是
②尾气处理时,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与
您最近一年使用:0次
2023-05-04更新
|
436次组卷
|
2卷引用:海南省文昌中学2023-2024学年高一下学期期中段考化学试题
名校
解题方法
8 . 常温下,下列各组离子一定能大量共存的是
A.pH=1的溶液:I-、Mg2+、 、 、 |
B.FeCl3溶液中:K+、Na+、 、 、 |
C.pH=12的溶液:K+、Na+、 、 、 |
| D.水电离出的c(H+)=10-12mol/L的溶液:Na+、K+、Cl-、HS- |
您最近一年使用:0次
名校
9 . 部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
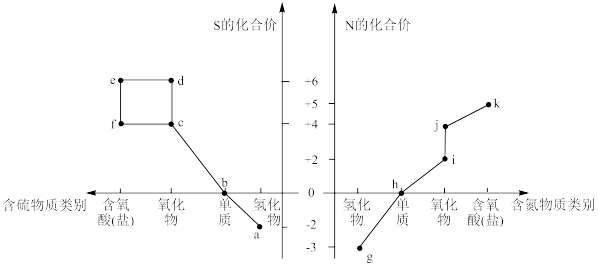
回答下列问题:
(1)h的电子式为_______ 。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是_______ (填序号)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将 的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是_______ 。
(4) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入 的
的 浓液中,可制得该物质:
浓液中,可制得该物质: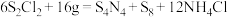 (已知
(已知 是硫单质中最稳定的)。
是硫单质中最稳定的)。
①上述制备反应中被氧化的元素是_______ (填元素符号),物质g体现的性质有_______ 。
② 在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是_______ 。

回答下列问题:
(1)h的电子式为
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将
 的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是(4)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入 的
的 浓液中,可制得该物质:
浓液中,可制得该物质: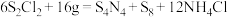 (已知
(已知 是硫单质中最稳定的)。
是硫单质中最稳定的)。①上述制备反应中被氧化的元素是
②
 在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
您最近一年使用:0次
2022-11-27更新
|
158次组卷
|
3卷引用:海南省琼海市嘉积中学2022-2023学年高三上学期期中检测化学试题
名校
10 . 含有实验装置类的试题,常常是围绕某一实验目的所进行的系统操作,解答时重在依据实验中各物质的性质与转化、装置的结构与功能、反应条件的控制等。
(1)某学习小组设计实验制备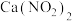 。实验装置如图1所示(夹持装置已略去)。
。实验装置如图1所示(夹持装置已略去)。
已知: ;
;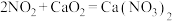 。
。

①向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的 ,目的是
,目的是_______ 。
②B中盛放的试剂是_______ 。
(2)硫代硫酸钠( )可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠:
)可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠: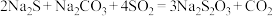 的装置如图2。
的装置如图2。
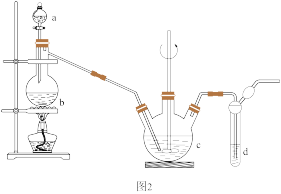
①a、b中试剂分别为 溶液和
溶液和 固体,c中试剂为
固体,c中试剂为_______ ,d中的试剂为_______ 。
②为了保证硫代硫酸钠的产量,实验中通入的 不能过量,原因是
不能过量,原因是_______ 。
(3)实验室用图3装置测定FeO和 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是FeO和
的质量,D装置的硬质双通玻璃管中的固体物质是FeO和 的混合物。
的混合物。

装置B的作用是_______ ;装置C中装的液体是_______ ;F所起的作用是_______ 。
(1)某学习小组设计实验制备
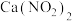 。实验装置如图1所示(夹持装置已略去)。
。实验装置如图1所示(夹持装置已略去)。已知:
 ;
;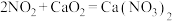 。
。
①向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的
 ,目的是
,目的是②B中盛放的试剂是
(2)硫代硫酸钠(
 )可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠:
)可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠: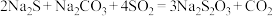 的装置如图2。
的装置如图2。
①a、b中试剂分别为
 溶液和
溶液和 固体,c中试剂为
固体,c中试剂为②为了保证硫代硫酸钠的产量,实验中通入的
 不能过量,原因是
不能过量,原因是(3)实验室用图3装置测定FeO和
 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是FeO和
的质量,D装置的硬质双通玻璃管中的固体物质是FeO和 的混合物。
的混合物。
装置B的作用是
您最近一年使用:0次



