水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
标注。
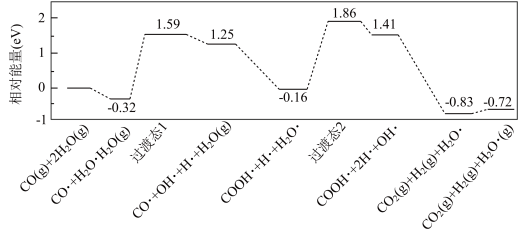
可知水煤气变换的ΔH________ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________ eV,写出该步骤的化学方程式_________ 。
 标注。
标注。
可知水煤气变换的ΔH
2020高三·全国·专题练习 查看更多[12]
(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训甘肃省白银市靖远县第四中学2021届高三上学期10月月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考向18 化学反应与能量变化-备战2022年高考化学一轮复习考点微专题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点05 化学反应中的能量变化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第1讲 化学能与热能
更新时间:2020-04-15 09:47:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】I.分别取40mL的0.50mol·L-1盐酸与40mL的0.55mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
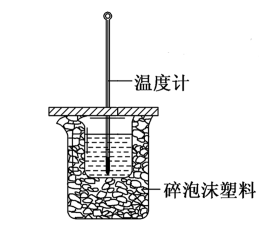
(1)反应过程中,NaOH稍过量的原因是___________ 。
(2)图中装置缺少的仪器是___________ 。
(3)假设盐酸和NaOH溶液的密度都是1g·cm-3,又知中和后生成溶液的比热容c=4.18J·g-1·℃-1,为了计算中和热,实验时还需测量的数据有(填字母)___________ 。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度
D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
Ⅱ.已知:①4g氢气在氧气中完全燃烧生成液态水时放出572 kJ的热量。
①CH4的燃烧热为ΔH=-890 kJ·mol-1。
请回答下列问题:
(4)写出H2燃烧热的热化学方程式___________ 。
(5)11.2 L H2和CH4的混合气体(标准状况下)完全燃烧生成CO2和液态水时放出369.5 kJ的热量,则混合气体中H2和CH4的物质的量之比是___________ 。

(1)反应过程中,NaOH稍过量的原因是
(2)图中装置缺少的仪器是
(3)假设盐酸和NaOH溶液的密度都是1g·cm-3,又知中和后生成溶液的比热容c=4.18J·g-1·℃-1,为了计算中和热,实验时还需测量的数据有(填字母)
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度
D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
Ⅱ.已知:①4g氢气在氧气中完全燃烧生成液态水时放出572 kJ的热量。
①CH4的燃烧热为ΔH=-890 kJ·mol-1。
请回答下列问题:
(4)写出H2燃烧热的热化学方程式
(5)11.2 L H2和CH4的混合气体(标准状况下)完全燃烧生成CO2和液态水时放出369.5 kJ的热量,则混合气体中H2和CH4的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=﹣1275.6kJ/mol
②H2O(l)═H2O(g)△H=+44.0kJ/mol
写出甲醇燃烧的热化学方程式________ .
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=﹣1275.6kJ/mol
②H2O(l)═H2O(g)△H=+44.0kJ/mol
写出甲醇燃烧的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)家用液化气的主要成分之一是丁烷(C4H10),当1kg丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5×104kJ,试写出表示丁烷燃烧热的热化学方程式___ 。
(2)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol。请回答下列问题:
①用太阳能分解10mol水消耗的能量是___ kJ;
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_____ ;
③研究NO2、SO2、CO等大气污染气体的处理具有重要意义,已知:
2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ/mol
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0kJ/mol
则反应NO2(g)+SO2(g)=SO3(g)+NO(g)的ΔH=___ kJ/mol。
(2)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol。请回答下列问题:
①用太阳能分解10mol水消耗的能量是
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式
③研究NO2、SO2、CO等大气污染气体的处理具有重要意义,已知:
2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ/mol
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0kJ/mol
则反应NO2(g)+SO2(g)=SO3(g)+NO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1 mol气态水过程中的能量变化图。
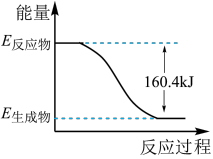
(1)该反应属于________ (填“吸热”或“放热”)反应。
(2)写出该火箭推进器中相关反应的热化学方程式:______ 。
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为_______ mol。

(1)该反应属于
(2)写出该火箭推进器中相关反应的热化学方程式:
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如下图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是_______ (填“吸热”或“放热”)反应,NO2和CO的总能量_______ (填“>”、“<”或“=”)CO2和NO的总能量。
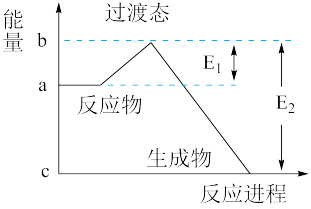
(2)在某体积为2L的密闭容器中充入0.5molNO2和1molCO,在一定条件下发生反应:NO2+CO⇌CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
①假设此反应在5min时达到平衡,则此时容器内气体的总物质的量为_______ ;
②下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ 。
A.容器内气体的密度保持不变
B.NO2的物质的量浓度不再改变
C.容器内气体的平均相对分子质量不变
D.NO2的消耗速率与CO2的消耗速率相等
E.容器内气体的压强保持不变
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如下图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是

(2)在某体积为2L的密闭容器中充入0.5molNO2和1molCO,在一定条件下发生反应:NO2+CO⇌CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
①假设此反应在5min时达到平衡,则此时容器内气体的总物质的量为
②下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.容器内气体的密度保持不变
B.NO2的物质的量浓度不再改变
C.容器内气体的平均相对分子质量不变
D.NO2的消耗速率与CO2的消耗速率相等
E.容器内气体的压强保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题。
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和_______ (填“大于”“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量_______ (填“>”“<”或“=”)572kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是_______ 。
(3)用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84kJ·mol-1
在H2SO4溶液中,1molCu与1molH2O2完全反应生成Cu2+(aq)和H2O(l)的反应热ΔH等于_______。
(1)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。
①该反应的生成物能量总和
②若2mol氢气完全燃烧生成水蒸气,则放出的热量
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g)⇌2SO3(g) ΔH1=-197kJ·mol-1
H2O(g)=H2O(l) ΔH2=-44kJ·mol-1
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是
(3)用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84kJ·mol-1
O2(g)=H2O(l) ΔH=-285.84kJ·mol-1在H2SO4溶液中,1molCu与1molH2O2完全反应生成Cu2+(aq)和H2O(l)的反应热ΔH等于_______。
| A.-417.91kJ·mol-1 | B.-319.68kJ·mol-1 |
| C.546.69kJ·mol-1 | D.-448.46kJ·mol-1 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
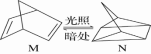
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ·mol-1, 则M与N较稳定的是_________ 。
(2)已知CH3OH(l)的燃烧热为726.5 kJ·mol-1,CH3OH(l) +1/2 O2(g)===CO2(g)+2H2O(g) ΔH=-a kJ·mol-1,则a________ 726.5(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时放出145 kJ热量,写出该反应的热化学方程式:_____________________________________________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为__________ 。
(5)已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N 键分别需要的能量是a kJ、b kJ、c kJ,则N2与H2反应生成NH3的热化学方程式为_________________________________ 。
(6)通过以下反应可获得新型能源二甲醚(CH3OCH3)。
①C(s)+H2O(g)===CO(g)+H2(g) ΔH1=a kJ·mol-1
②CO(g)+H2O(g)===CO2(g)+H2(g) ΔH2=b kJ·mol-1
③CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH3=c kJ·mol-1
④2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=d kJ·mol-1
则反应2CO(g)+4H2(g)===CH3OCH3(g)+H2O(g)的ΔH=__________________________________ 。(用含a,b,c,d的式子表示)
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6 kJ·mol-1, 则M与N较稳定的是

(2)已知CH3OH(l)的燃烧热为726.5 kJ·mol-1,CH3OH(l) +1/2 O2(g)===CO2(g)+2H2O(g) ΔH=-a kJ·mol-1,则a
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
(5)已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N 键分别需要的能量是a kJ、b kJ、c kJ,则N2与H2反应生成NH3的热化学方程式为
(6)通过以下反应可获得新型能源二甲醚(CH3OCH3)。
①C(s)+H2O(g)===CO(g)+H2(g) ΔH1=a kJ·mol-1
②CO(g)+H2O(g)===CO2(g)+H2(g) ΔH2=b kJ·mol-1
③CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH3=c kJ·mol-1
④2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=d kJ·mol-1
则反应2CO(g)+4H2(g)===CH3OCH3(g)+H2O(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化碳的综合利用具有重要意义。
(1)工业上以 和
和 为原料可以制取合成气(
为原料可以制取合成气( 和
和 )。
)。
①已知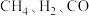 的燃烧热分别为
的燃烧热分别为 ,则反应
,则反应 的
的
___________ 。
(1)工业上以
 和
和 为原料可以制取合成气(
为原料可以制取合成气( 和
和 )。
)。①已知
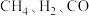 的燃烧热分别为
的燃烧热分别为 ,则反应
,则反应 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】石灰石脱硫法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:CaSO4 (s)+CO (g) =CaO(s)+SO2 (g)+CO2 (g) ΔH1=+218.4 kJ·mol-1(反应Ⅰ),CaSO4(s)+4CO(g)=CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1(反应Ⅱ),结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s)的反应的热化学方程式_______________ 。
您最近一年使用:0次



