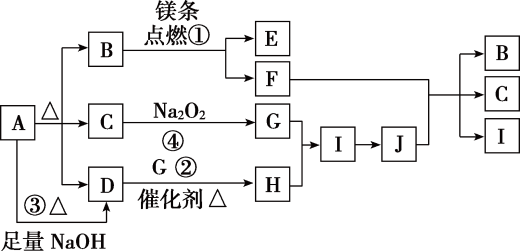
已知有以下物质相互转化
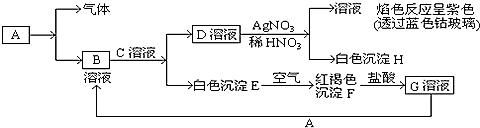
试回答:
(1)写出B的化学式___ 。C的化学式___ 。D的化学式___ 。
(2)写出由E转变成F的化学方程式___ 。
(3)把KSCN加到G溶液中的现象是___ ;向G溶液加入A的有关离子反应方程式___ 。
(4)焰色反应是___ (填物理或化学)变化,经过焰色反应试验后的铂丝可选择下面___ (填字母)试剂清洗。
A.硫酸 B.盐酸 C.硝酸
(5)选择合适的方法除杂:
①Fe2O3[Fe(OH)2]______ 。
②FeCl3溶液(FeCl2)______ 。
③FeCl2溶液(FeCl3)______ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)把KSCN加到G溶液中的现象是
(4)焰色反应是
A.硫酸 B.盐酸 C.硝酸
(5)选择合适的方法除杂:
①Fe2O3[Fe(OH)2]
②FeCl3溶液(FeCl2)
③FeCl2溶液(FeCl3)
19-20高一·全国·期末 查看更多[1]
(已下线)【南昌新东方】莲塘二中 2019-2020 高一(上)期末
更新时间:2020/04/18 08:37:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和条件被略去,A、 X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;B、C、E是常见气体,G的焰色反应呈黄色;I的溶液呈黄色。
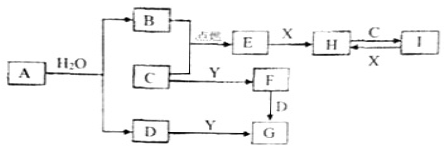
请回答下列问题:
(1)写出下列物质的化学式A___ 、F___ ;
(2)说出黄绿色气体C的一种用途___ ;
(3)实验室检验H中所含的金属阳离子的方法是,先加___ 无明显现象,再加氯水,溶液变为___ 色;
(4)写出C与H溶液反应的化学方程式___ .

请回答下列问题:
(1)写出下列物质的化学式A
(2)说出黄绿色气体C的一种用途
(3)实验室检验H中所含的金属阳离子的方法是,先加
(4)写出C与H溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F.溶液F空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
(1)单质A是一种黄色固体,组成单质A的元素在周期表中的位置是_______ 。用物理方法洗去试管内壁的A,应选择的试剂是_______ ;化学方法洗去试管内壁的A是发生歧化反应生成两种盐,但这两种盐在强酸性条件下不能大量共存,请写出化学方法洗去试管内壁的A时发生的化学反应方程式_______ 。
(2)FeCl3溶液中的Fe3+可以催化G与氧气在溶液中的反应,此催化过程分两步进行,请写出Fe3+参与的第一步反应的离子反应方程式_______ 。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为_______ ,当生成2mol二氧化氯时,转移电子_______ mol。
(4)将D溶于稀硫酸,向恰好完全反应后所得的溶液中加入过量氢氧化钡溶液,则加入氢氧化钡溶液的过程中的现象是_______ 。
(5)H的溶液与稀硫酸反应时生成有臭鸡蛋气味的气体和淡黄色单质,写出该反应化学方程式_______ 。
(1)单质A是一种黄色固体,组成单质A的元素在周期表中的位置是
(2)FeCl3溶液中的Fe3+可以催化G与氧气在溶液中的反应,此催化过程分两步进行,请写出Fe3+参与的第一步反应的离子反应方程式
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为
(4)将D溶于稀硫酸,向恰好完全反应后所得的溶液中加入过量氢氧化钡溶液,则加入氢氧化钡溶液的过程中的现象是
(5)H的溶液与稀硫酸反应时生成有臭鸡蛋气味的气体和淡黄色单质,写出该反应化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】工业上常通过高温分解FeSO4的方法制备较为纯净的Fe2O3,其反应方程式为:2FeSO4 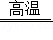 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
为了检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,先加入一定量稀盐酸使固体完全溶解,再向所得溶液中适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
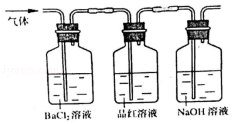
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2 和SO3
请回答下列问题:
(1)写出能说明FeSO4发生分解的现象__________________________________ ;
(2)写出KSCN溶液与Fe3+反应的离子方程式:_________________ ;
(3)实验②中,气体通过BaCl2时可以观察到的现象__________________________ ,产生该现象所对应的化学反应为___________________________________ (用一个化学反应方程式表示);
(4)实验②中最后要将通过品红溶液的气体通入NaOH溶液中,其目的是________________________ 。
 Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑为了检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,先加入一定量稀盐酸使固体完全溶解,再向所得溶液中适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2 和SO3
请回答下列问题:
(1)写出能说明FeSO4发生分解的现象
(2)写出KSCN溶液与Fe3+反应的离子方程式:
(3)实验②中,气体通过BaCl2时可以观察到的现象
(4)实验②中最后要将通过品红溶液的气体通入NaOH溶液中,其目的是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】石墨在材料领域有重要应用,某初级石墨中含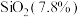 、
、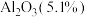 和
和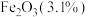 等杂质,提纯与综合利用工艺流程如下:
等杂质,提纯与综合利用工艺流程如下:
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃.
的沸点为57.6℃,金属氯化物的沸点均高于150℃.
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是______ 。
(2)“冷凝”后,所得“气体”的成分有 和
和______ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是______ ;取少量滤液于试管中,______ (实验操作及现象),证明已完全沉淀。
(4)“沉铝”得到的产物为 ,工业上由
,工业上由 制Al需发生两步反应,写出第一步得到
制Al需发生两步反应,写出第一步得到 的化学方程式
的化学方程式______ 。
(5)写出A1的一种用途______ 。
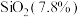 、
、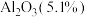 和
和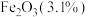 等杂质,提纯与综合利用工艺流程如下:
等杂质,提纯与综合利用工艺流程如下:
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃.
的沸点为57.6℃,金属氯化物的沸点均高于150℃.(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体”的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)“沉铝”得到的产物为
 ,工业上由
,工业上由 制Al需发生两步反应,写出第一步得到
制Al需发生两步反应,写出第一步得到 的化学方程式
的化学方程式(5)写出A1的一种用途
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
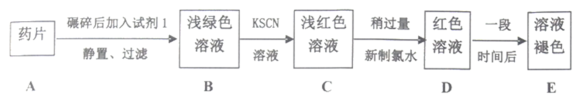
【推荐3】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁、呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸(主要成分:稀盐酸),服用时同维生素C一起服用效果会更好。某学习小组为了检测“速力菲”药片中Fe2+的存在,设计并进行了如图实验:
(1)试剂1是_______ (填化学式)。
(2)取少量B溶液于试管中,向其滴加NaOH溶液,最初观察到白色絮状沉淀,迅速变为灰绿色,最终变为红褐色,沉淀颜色变化的原因是_______ (用化学方程式表示)。
(3)由B到C过程中溶液出现浅红色现象的原因可能是_______ 。
(4)由C到D过程中加入新制氯水,溶液中发生反应的离子方程式是_______ ,有同学提出此过程用双氧水代替新制氯水更加合理,理由是_______ 。
(5)一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_______ 性。
(6)在上述实验中,同学们发现红色溶液放置一段时间后,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙两位同学对此进行了猜想:
你认为_______ (填“甲”或“乙”)同学的猜想更合理。请设计一个简单的实验加以验证你的判断:_______ 。
(1)试剂1是
(2)取少量B溶液于试管中,向其滴加NaOH溶液,最初观察到白色絮状沉淀,迅速变为灰绿色,最终变为红褐色,沉淀颜色变化的原因是
(3)由B到C过程中溶液出现浅红色现象的原因可能是
(4)由C到D过程中加入新制氯水,溶液中发生反应的离子方程式是
(5)一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
(6)在上述实验中,同学们发现红色溶液放置一段时间后,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙两位同学对此进行了猜想:
| 编号 | 猜想 |
| 甲 | 溶液中的+3价铁又被还原成+2价铁 |
| 乙 | 溶液中的SCN-被过量的新制氯水氧化 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】物质A-J间的转化关系如图所示,A、C为金属氧化物,其中A 为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解。

(1)A 的化学式是________________ ;
(2)I→J 反应的离子方程式是_______________________________ ;
(3)F转化为G的过程中观察到的现象是__________________________ ,反应的化学方程式是___________________________ ;
(4)检验E 中主要阳离子的方法________________________________ ;

(1)A 的化学式是
(2)I→J 反应的离子方程式是
(3)F转化为G的过程中观察到的现象是
(4)检验E 中主要阳离子的方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F六种物质的相互转化关系如 下图所示(反应条件未标出),其中反应①是置换反应。

(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是__________ 。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是________ ,反应③的化学方程式是____ 。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是________ 。

(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列转化关系中,X. Y是生活中用途广泛的两种金属单质,A.B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。
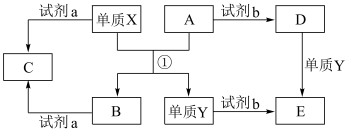
(1)物质B的化学式为___________ ;单质Y的化学式为___________
(2) 若试剂b是H2SO4,由D到E的离子方程式:___________ 。
(3)若试剂a是NaOH溶液,请写出B与NaOH溶液反应的离子方程式:___________ 。
(4)Y在高温与水蒸气反应的化学方程式为___________ 。
(5)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是___________ 。

(1)物质B的化学式为
(2) 若试剂b是H2SO4,由D到E的离子方程式:
(3)若试剂a是NaOH溶液,请写出B与NaOH溶液反应的离子方程式:
(4)Y在高温与水蒸气反应的化学方程式为
(5)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业氧化锌(含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质)的流程如下:
②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业ZnO粉碎,其目的是____________ 。
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和_____ ,其中玻璃棒的作用为_____________ 。
(3)②发生反应的离子方程式有2H2O+2 +3Mn2+=5MnO2↓+4H+和
+3Mn2+=5MnO2↓+4H+和_______ 。
(4)若④中产物仅为ZnCO3·xZn(OH)2,则发生反应的离子方程式为_________ ;取干燥后的滤饼ag,煅烧后可得到产品(ZnO)mg,则x等于_______ (用含a、m的代数式表示)。
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是___________ 。

②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业ZnO粉碎,其目的是
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和
(3)②发生反应的离子方程式有2H2O+2
 +3Mn2+=5MnO2↓+4H+和
+3Mn2+=5MnO2↓+4H+和(4)若④中产物仅为ZnCO3·xZn(OH)2,则发生反应的离子方程式为
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氢氧化氧镍( )难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含
)难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含 ,以及少量
,以及少量 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图: 的性质较稳定。
的性质较稳定。
回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
(2)“浸取渣”的主要成分为______ (填化学式)。
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:______ 。
(4)“转化”时 的作用是
的作用是______ ,实际生产中发现 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是______ 。
(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的 如下表所示:
如下表所示:
则“沉铁”过程中加入 溶液调节
溶液调节 的范围应为
的范围应为______ 。
(6)“氧化”时发生反应的离子方程式为______ 。若用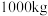 废料(其中
废料(其中 的质量分数为
的质量分数为 )经该流程制得
)经该流程制得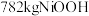 固体,则
固体,则 的产率为
的产率为______ 。( )
)
 )难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含
)难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含 ,以及少量
,以及少量 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图: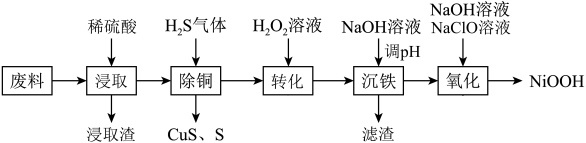
 的性质较稳定。
的性质较稳定。回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.使用 浓硫酸浸取 浓硫酸浸取 |
(2)“浸取渣”的主要成分为
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:
(4)“转化”时
 的作用是
的作用是 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的
 如下表所示:
如下表所示:金属阳离子 |
|
|
|
开始沉淀时的pH | 1.5 | 6.5 | 7.2 |
沉淀完全时的pH | 3.2 | 9.7 | 9.2 |
 溶液调节
溶液调节 的范围应为
的范围应为(6)“氧化”时发生反应的离子方程式为
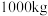 废料(其中
废料(其中 的质量分数为
的质量分数为 )经该流程制得
)经该流程制得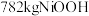 固体,则
固体,则 的产率为
的产率为 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属镓有“电子工业脊梁”的美誉,镓与铝的化学性质类似。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示。
回答下列问题。
(1)“酸浸”过程中禁止明火加热,原因是________ 。
(2)“结晶”过程中得到 的具体操作为
的具体操作为_______ 。
(3)“中和沉淀”过程中pH应调节的范围为________ 。
(4)“碳酸化”过程中不能通入过量 的原因为
的原因为________ (用离子方程式表示)。
(5)下列说法中不正确的是________ (填字母)。
a.为提高浸出率,可将刚玉渣研磨
b.由流程图可知酸性: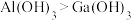
c.“碱浸”过程中可用氨水代替NaOH溶液
(6)GaN具有优异的光电性能。工业上常采用在1100℃条件下,利用Ga与 反应制备GaN,该过程的化学方程式为
反应制备GaN,该过程的化学方程式为___________ 。
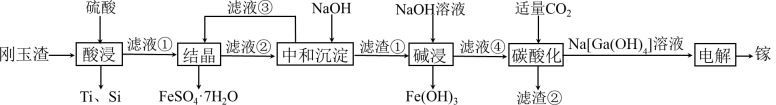
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 4.5 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 5.5 | 4.7 | 3.2 | 9.0 |
(1)“酸浸”过程中禁止明火加热,原因是
(2)“结晶”过程中得到
 的具体操作为
的具体操作为(3)“中和沉淀”过程中pH应调节的范围为
(4)“碳酸化”过程中不能通入过量
 的原因为
的原因为(5)下列说法中不正确的是
a.为提高浸出率,可将刚玉渣研磨
b.由流程图可知酸性:
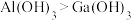
c.“碱浸”过程中可用氨水代替NaOH溶液
(6)GaN具有优异的光电性能。工业上常采用在1100℃条件下,利用Ga与
 反应制备GaN,该过程的化学方程式为
反应制备GaN,该过程的化学方程式为
您最近一年使用:0次