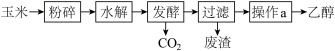
乙醇是一种常用的工业燃料,乙醇的生产过程可用下图表示:
已知: 。
。
(1)粉碎玉米的目的是____________________ 。
(2)请写出“发酵”过程中发生反应的化学方程式_________________ ;发酵产生的CO2的纯度可达到99%,可回收利用,请举出它的两项用途:________________ 、_________________ 。
(3)操作a的名称是_____________ ,检验乙醇中是否含有水可以用试剂 ________________ 。

已知:
 。
。(1)粉碎玉米的目的是
(2)请写出“发酵”过程中发生反应的化学方程式
(3)操作a的名称是
19-20高一下·全国·课时练习 查看更多[2]
更新时间:2020-04-19 18:03:29
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质之一,一般不溶于水,也不溶于有机溶剂。有机物A~F之间的转化如图所示(图中部分产物已略去,且B生成C的同时还有 生成):
生成):

(1)由A生成B的化学方程式为______________ 。
(2)B、C中均含有的官能团的电子式为_______________ 。
(3)从A转化为F的过程中发生反应的类型有( )
A.氧化反应 B.酯化反应 C.加成反应 D.水解反应
(4)写出C→D发生反应的化学方程式:____________ 。
(5)F有多种同分异构体,请写出其中与它具有相同官能团的所有同分异构体的结构简式:_____ 。
 生成):
生成):
(1)由A生成B的化学方程式为
(2)B、C中均含有的官能团的电子式为
(3)从A转化为F的过程中发生反应的类型有
A.氧化反应 B.酯化反应 C.加成反应 D.水解反应
(4)写出C→D发生反应的化学方程式:
(5)F有多种同分异构体,请写出其中与它具有相同官能团的所有同分异构体的结构简式:
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐2】利用含多糖(淀粉)的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:
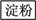
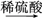
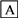 →
→ →
→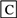 →
→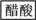
B是日常生活中有特殊香味 的常见有机物,在有些饮料中含有B。
的常见有机物,在有些饮料中含有B。
(1)C中官能团的名称是______________________ 。
(2)B→C的反应类型是________________ (填字母)。
A.取代反应 B.加成反应 C.氧化反应 D.还原反应
(3)写出由醋酸制备醋酸甲酯的化学反应方程式:
_________________________________________________ 。
(4)实验室由B可制备乙烯气体,写出将乙烯气体通入溴水中出现的现象:
__________________________________________________ 。
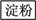
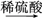
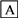 →
→ →
→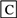 →
→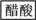
B是日常生活中有特殊香味
 的常见有机物,在有些饮料中含有B。
的常见有机物,在有些饮料中含有B。(1)C中官能团的名称是
(2)B→C的反应类型是
A.取代反应 B.加成反应 C.氧化反应 D.还原反应
(3)写出由醋酸制备醋酸甲酯的化学反应方程式:
(4)实验室由B可制备乙烯气体,写出将乙烯气体通入溴水中出现的现象:
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐3】有机化合物A→G之间的转化关系如下图所示.已知B、D是生活中的两种常见物质,F的产量是衡量一个国家石油化工发展水平的标志。回答下列问题:
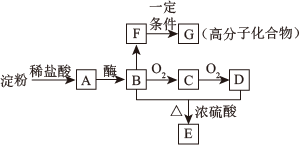
(1)A是淀粉水解的最终产物,A的化学式为__________ .
(2)B、D中官能团的名称分别为_________ 、__________ .
(3)F→G的反应类型为________ ,B+D→E的反应类型为__________ .
(4)一定条件下,B除了生成F外,还有水生成,写出该反应的化学方程式:__________ .
(5)分子中含有“—COO—”结构的E的同分异构体有_______ 种(不包含本身和立体异构).

(1)A是淀粉水解的最终产物,A的化学式为
(2)B、D中官能团的名称分别为
(3)F→G的反应类型为
(4)一定条件下,B除了生成F外,还有水生成,写出该反应的化学方程式:
(5)分子中含有“—COO—”结构的E的同分异构体有
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】气态烃A中碳元素与氢元素的质量比为6︰1,淀粉在一定条件下水解可生成B。B在人体组织中缓慢氧化,放出热量,提供生命活动所需能量。有关物质的转化关系如下图:
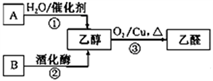
请回答:
(1)①的反应类型是_________________ 。
(2)向试管中加入2 mL10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入2 mL10% B溶液,加热。写出加热后观察到的现象_____________________________ 。
(3)反应③的化学方程式是__________________________________________________ 。

请回答:
(1)①的反应类型是
(2)向试管中加入2 mL10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入2 mL10% B溶液,加热。写出加热后观察到的现象
(3)反应③的化学方程式是
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】气态烃A中碳元素与氢元素的质量比为6∶l。淀粉在一定条件下水解可生成B,B在人体组织中发生缓慢氧化,放出热量,提供生命活动所需能量。有关物质的转化关系如图:
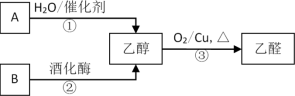
请回答:
(1)①的反应类型是_______ ,A中含有的官能团名称是_______ 。
(2)向试管中加入2 mL 10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入2 mL 10% B溶液,加热。写出加热后观察到的现象_______________ 。
(3)反应③的化学方程式是_______________ 。
(4)下列说法不正确的是( )
A.气态烃A可作水果的催熟剂
B.工业上,用原料A来合成聚乙烯
C.医疗上常用0.9%的乙醇溶液作消毒剂
D.有机物B通过途径②可被应用于酿酒

请回答:
(1)①的反应类型是
(2)向试管中加入2 mL 10%氢氧化钠溶液,滴加4~5滴5%硫酸铜溶液,振荡后加入2 mL 10% B溶液,加热。写出加热后观察到的现象
(3)反应③的化学方程式是
(4)下列说法不正确的是
A.气态烃A可作水果的催熟剂
B.工业上,用原料A来合成聚乙烯
C.医疗上常用0.9%的乙醇溶液作消毒剂
D.有机物B通过途径②可被应用于酿酒
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐3】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染,生产流程如下:
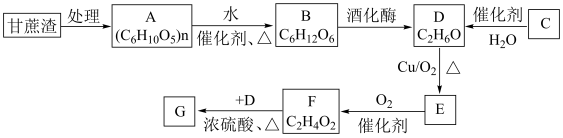
已知石油裂解已成为生产C的主要方法,G是具有果香味的液体,试填空:
(1)B的名称为_______ ;
(2)写出C发生加聚反应的方程式:_______ ;
(3)E的结构简式为_______ ;
(4)F→G的化学方程式为_______ ,该反应的反应类型为_______ ;
(5)已知HCOOCH3也具有果香味,该物质与F的关系互称为_______ 。

已知石油裂解已成为生产C的主要方法,G是具有果香味的液体,试填空:
(1)B的名称为
(2)写出C发生加聚反应的方程式:
(3)E的结构简式为
(4)F→G的化学方程式为
(5)已知HCOOCH3也具有果香味,该物质与F的关系互称为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐1】下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图,其中A是面粉的主要成分;C和E反应能生成F,F具有香味,B与E的实验式相同。
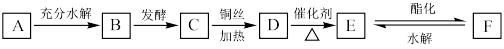
根据以上信息及各物质的转化关系完成下列各题:
(1)B的化学式为_____ ,C中所含官能团名称_____ ,与B同分异构体的一种物质的名称___ 。
(2)D与新制银氨溶液在水浴加热条件下发生反应的离子方程式________ 。
(3)其中能与新制氢氧化铜悬浊液在加热煮沸条件下能产生砖红色的沉定的物质有_______ (填名称)。
(4)写出C→D的化学方程式________ 。
(5)写出C+E→F的化学方程式_________ 。
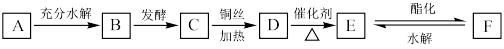
根据以上信息及各物质的转化关系完成下列各题:
(1)B的化学式为
(2)D与新制银氨溶液在水浴加热条件下发生反应的离子方程式
(3)其中能与新制氢氧化铜悬浊液在加热煮沸条件下能产生砖红色的沉定的物质有
(4)写出C→D的化学方程式
(5)写出C+E→F的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】以淀粉为原料,经过一系列反应可以制得酯F(C5H8O4)。B结构中有甲基,1mol B可以与2mol Na和1mol NaOH反应。
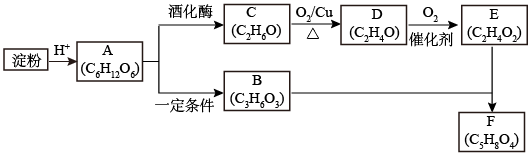
请回答:
(1)D中官能团名称是___________ 。
(2)D→E的反应类型是___________ 。
(3)C→D的化学反应方程式是___________ 。
(4)F的结构简式是___________ 。
(5)下列说法不正确的是___________。
(6)检验淀粉在酸性条件下水解产物A (C6H12O6)的操作是___________ 。

请回答:
(1)D中官能团名称是
(2)D→E的反应类型是
(3)C→D的化学反应方程式是
(4)F的结构简式是
(5)下列说法不正确的是___________。
| A.由A生成C时可以产生一种无色无味气体 |
| B.可以用新制Cu(OH)2悬浊液鉴别C、D、E (必要时可以加热) |
| C.相同物质的量的B、D耗氧量相同 |
| D.1mol C与足量钠反应,消耗钠2mol |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为了检验淀粉水解的产物,设计如下实验方案:

请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_________ ;
(2)试剂2为_________ ,其作用是_________ ,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________ ;
(3)反应①的化学方程式为_________ ;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________ ;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________ (填”能”或”否”)否,若不能,其原因是_________ 硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________ 。

请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是
(2)试剂2为
(3)反应①的化学方程式为
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的
您最近一年使用:0次
【推荐1】某同学用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3。不考虑其它杂质)制取绿矾(FeSO4· 7H2O),设计了如下流程(部分物质已略去)。
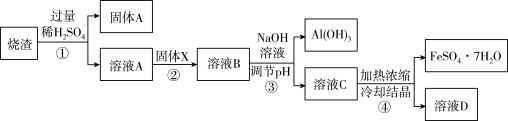
回答下列问题:
(1)硫铁矿的主要成分是FeS2,其中铁元素化合价为_______ ,焙烧产物之一的Fe2O3,俗称________ 。
(2)固体A的主要成分是_______ ,固体X为_________ 。
(3)写出①中Al2O3发生反应的离子方程式:__________ 。
(4)从溶液C到绿矾的过程中,须控制反应条件防止变质,检验其变质所用的化学试剂是________ ,步骤③所得Al(OH)3沉淀含有杂质,应如何洗涤?__________ 。

回答下列问题:
(1)硫铁矿的主要成分是FeS2,其中铁元素化合价为
(2)固体A的主要成分是
(3)写出①中Al2O3发生反应的离子方程式:
(4)从溶液C到绿矾的过程中,须控制反应条件防止变质,检验其变质所用的化学试剂是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】化工产品中,含氯物质众多,其用途广泛。回答下列化合价问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的类别A为_______ 、物质B为_______ (填化学式)。

(2)“84”消毒液的有效成分是次氯酸钠,而洁厕灵的有效成分是盐酸,两者不能混合使用,请用离子方程式解释原因:_______ 。
(3)电石渣[主要成分为 ]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取
]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取 的工艺流程如图所示:
的工艺流程如图所示:

已知: 易溶于水。
易溶于水。
①工业生产电石(CaC2)的反应为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
②“转化”发生反应的离子方程式为_______ 。
③上述流程中所用 是用
是用 与浓盐酸反应制得,该反应的离子方程式是
与浓盐酸反应制得,该反应的离子方程式是_______ ,其中盐酸体现的性质为_______ 、_______ 。
④流程中制 ,要控制温度
,要控制温度 以上,从化学反应速率的影响因素来考虑,你认为目的是
以上,从化学反应速率的影响因素来考虑,你认为目的是_______ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的类别A为

(2)“84”消毒液的有效成分是次氯酸钠,而洁厕灵的有效成分是盐酸,两者不能混合使用,请用离子方程式解释原因:
(3)电石渣[主要成分为
 ]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取
]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取 的工艺流程如图所示:
的工艺流程如图所示:
已知:
 易溶于水。
易溶于水。①工业生产电石(CaC2)的反应为
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为②“转化”发生反应的离子方程式为
③上述流程中所用
 是用
是用 与浓盐酸反应制得,该反应的离子方程式是
与浓盐酸反应制得,该反应的离子方程式是④流程中制
 ,要控制温度
,要控制温度 以上,从化学反应速率的影响因素来考虑,你认为目的是
以上,从化学反应速率的影响因素来考虑,你认为目的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。以硫铁矿(主要成分为FeS2,杂质不与盐酸反应)为原料制备三氯化铁晶体(FeC13•6H2O)的工艺流程如图所示:

回答下列问题:
(1)“焙烧”过程中,理论上1 molFeS2被氧化转移11 mol电子,则该反应的氧化产物为_____ 。
(2)“酸溶”不能用稀硫酸代替30%的盐酸,理由是_________ 。
(3)现有试剂:①稀盐酸②稀硫酸③稀硝酸④氯气⑤硫氰化钾溶液⑥高锰酸钾溶液⑦氢氧化钠溶液。为确认“酸溶”后的溶液中是否会含Fe2+,另取“焙烧”后的烧渣少许,用_______ (从上述试剂中选择,填标号)溶解,将所得溶液滴入_________ (从上述试剂中选择,填标号)中,若________ ,则说明“酸溶”后的溶液中含Fe2+。
(4)从FeCl3溶液中得到FeC13•6H2O的操作包括______ 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________ 。
(5)若以a吨硫铁矿为原料,最终制得b吨FeC13•6H2O,不计生产过程中的损失,则该硫铁矿中FeS2的含量为__________ (用含a、b的代数式表示)。

回答下列问题:
(1)“焙烧”过程中,理论上1 molFeS2被氧化转移11 mol电子,则该反应的氧化产物为
(2)“酸溶”不能用稀硫酸代替30%的盐酸,理由是
(3)现有试剂:①稀盐酸②稀硫酸③稀硝酸④氯气⑤硫氰化钾溶液⑥高锰酸钾溶液⑦氢氧化钠溶液。为确认“酸溶”后的溶液中是否会含Fe2+,另取“焙烧”后的烧渣少许,用
(4)从FeCl3溶液中得到FeC13•6H2O的操作包括
(5)若以a吨硫铁矿为原料,最终制得b吨FeC13•6H2O,不计生产过程中的损失,则该硫铁矿中FeS2的含量为
您最近一年使用:0次



