人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)将N2转化为含氮化合物的过程称为固氮。
①人工固氮,将N2→NH3,N2发生___ 反应(填“氧化”或“还原”)
②自然界固氮,可将少量N2转化为Ca(NO3)2等氮肥,转化途径如下(转化所需试剂及条件已略去):N2→NO→NO2→HNO3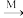 Ca(NO3)2。
Ca(NO3)2。
写出NO→NO2→HNO3的化学方程式___ 、___ 。
将HNO3转化为Ca(NO3)2,列举两种不同类别的化合物M___ (写化学式)。
(2)科学合理地保存、施用氮肥。
①NH4HCO3需阴凉处保存,原因是___ (写化学方程式)。
②铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式___ 。
(3)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如图所示(转化所需试剂及条件已略去):
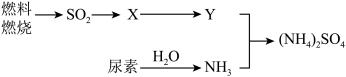
①Y与NH3反应生成(NH4)2SO4的化学方程式___ 。
②尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3。则尿素中C元素化合价为___ 。
(1)将N2转化为含氮化合物的过程称为固氮。
①人工固氮,将N2→NH3,N2发生
②自然界固氮,可将少量N2转化为Ca(NO3)2等氮肥,转化途径如下(转化所需试剂及条件已略去):N2→NO→NO2→HNO3
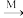 Ca(NO3)2。
Ca(NO3)2。写出NO→NO2→HNO3的化学方程式
将HNO3转化为Ca(NO3)2,列举两种不同类别的化合物M
(2)科学合理地保存、施用氮肥。
①NH4HCO3需阴凉处保存,原因是
②铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式
(3)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如图所示(转化所需试剂及条件已略去):

①Y与NH3反应生成(NH4)2SO4的化学方程式
②尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3。则尿素中C元素化合价为
更新时间:2020-04-24 16:37:46
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-
根据上述反应,XO4-、Z2、B2、A3+氧化性从强到弱的顺序为:___________
(2)已知KMnO4与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化产物和还原产物物质的量之比是___________ 。用单线桥法标出此反应的电子转移方向和数目_______________ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个配平的化学方程式:
________ +________ + H2SO4→ ________ +________ +________ (填化学式)
②反应中1mol氧化剂得到______ mol电子。
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-
根据上述反应,XO4-、Z2、B2、A3+氧化性从强到弱的顺序为:
(2)已知KMnO4与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化产物和还原产物物质的量之比是
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个配平的化学方程式:
②反应中1mol氧化剂得到
您最近一年使用:0次
【推荐2】Ⅰ.(1)①H2+CuO Cu+H2O
Cu+H2O
②CaCO3+2HCl=CaCl2+CO2↑+H2O
③3S+6NaOH 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O
④NH4NO3+Zn=ZnO+N2↑+2H2O
⑤Cu2O+4HCl=2HCuCl2+H2O
上述反应中,属于氧化还原反应的是________ (填序号)。
(2)配平下面氧化还原反应的化学方程式:KMnO4+SO2+H2O—K2SO4+MnSO4+H2SO4_____________ 。
Ⅱ.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是_____ 。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是________ 。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_____ ,离子反应方程式为_________ 。
(4)原溶液中可能大量存在的阴离子是下列的________ (填序号)。
A.Cl- B. C.
C. D.OH-
D.OH-
 Cu+H2O
Cu+H2O ②CaCO3+2HCl=CaCl2+CO2↑+H2O
③3S+6NaOH
 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O ④NH4NO3+Zn=ZnO+N2↑+2H2O
⑤Cu2O+4HCl=2HCuCl2+H2O
上述反应中,属于氧化还原反应的是
(2)配平下面氧化还原反应的化学方程式:KMnO4+SO2+H2O—K2SO4+MnSO4+H2SO4
Ⅱ.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有
(4)原溶液中可能大量存在的阴离子是下列的
A.Cl- B.
 C.
C. D.OH-
D.OH-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人体必需的微量元素。食用富含铁元素的食品,可以补充人体所需的铁元素。某实验小组通过化学实验的方法检验菠菜中的铁元素,体验实验研究的一般过程和化学知识在实际中的应用,回答下列问题:
(1)取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以________ (填离子符号)形式存在。
(2)另取新鲜菠菜剪碎、研磨、溶解、______________ ,然后将少许滤液加入试管中,加入少量H2O2溶液,再滴加几滴KSCN溶液,振荡,若观察到_______________ 现象,说明试验样品中含有铁元素。实验中加入H2O2溶液的目的为_______________ ,加入后Fe2+发生反应的离子方程式为________________ ,一段时间后,溶液中有气泡出现,产生气泡的原因是________________ 。
(3)甲同学查阅资料发现:KSCN中的硫元素为-2价。于是往(2)中继续滴加H2O2溶液,震荡,一段时间后发现溶液变为浅棕黄色,可能的原因是________________ ,小组同学为证实自己的猜想,设计如下对照实验:向1mL0.1mol·L-1KSCN溶液中加入足量5%H2O2溶液,再加入BaCl2溶液,观察到_______________ ,证实了甲同学的猜想是正确的。
(1)取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以
(2)另取新鲜菠菜剪碎、研磨、溶解、
(3)甲同学查阅资料发现:KSCN中的硫元素为-2价。于是往(2)中继续滴加H2O2溶液,震荡,一段时间后发现溶液变为浅棕黄色,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮和氮的化合物与人类有密切关系,回答以下问题:
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
(2)下列说法正确的是_______。
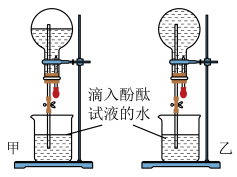
(3)甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据下图喷泉实验的装置进行实验都观察到美丽的红色喷泉。
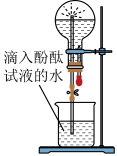
根据实验现象说明氨气具有的性质是_______ ,并用相应的方程式解释:_______ 。
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度_______ (填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度。
(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是_______ 。写出 ”的检验方法:
”的检验方法:_______ 。
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
| A.氮气分子很稳定 | B.尿素属于铵态氮肥 |
| C.工业合成氨是人工固氮 | D.闪电实现了大气固氮 |
| A.可用稀HNO3与FeS固体反应制取H2S |
| B.SO2能使酸性KMnO4、氯水褪色,说明SO2具有漂白作用 |
| C.少量NO2和足量SO2混合气体通入BaCl2溶液中,产生的沉淀只有BaSO4 |
D.向某溶液中滴加几滴盐酸酸化的BaCl2溶液,产生不溶于稀硝酸的白色沉淀则该溶液中一定含有 |

根据实验现象说明氨气具有的性质是
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度

(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是
 ”的检验方法:
”的检验方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮在自然界中的循环如图所示。

(1)过程①称为_______ ,写出合成氨反应的化学方程式:_______ ,该反应中氮气显_______ 性(填“氧化”或“还原”)。
(2)过程②称为_______ ,写出③中“雷电发庄稼”的化学方程式:_______ 。

(1)过程①称为
(2)过程②称为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】自然界中存在着很多的物质循环过程。
(1)下图是自然界中碳、氧循环的示意图。

①图一中,转化1是水吸收二氧化碳的过程,反应的化学反应方程式是____________ 。
②图二中,转化1是自然界中碳、氧循环的一个重要反应——绿色植物的光合作用,反应的化学方程式是____________ 。
③上述两个反应中的反应物相同,但得到的产物不同,原因是____________ 。
(2)下图是氮循环示意图,请回答下列问题。
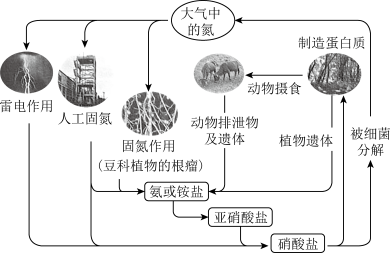
①自然界中的固氮和人工固氮的共同点是将氮元素由游离态转化为____________ 。
②雷电固氮反应的化学方程式是____________ ,其中氮元素被____________ (填“氧化”或“还原”)。
③根据循环图判断下列说法不正确的是____________ 。
a.氮元素均被氧化
b.工业合成氨属于人工固氮
c.含氮无机物和含氮有机物可相互转化
d.碳、氢、氧三种元素也参与了氮循环
(1)下图是自然界中碳、氧循环的示意图。

①图一中,转化1是水吸收二氧化碳的过程,反应的化学反应方程式是
②图二中,转化1是自然界中碳、氧循环的一个重要反应——绿色植物的光合作用,反应的化学方程式是
③上述两个反应中的反应物相同,但得到的产物不同,原因是
(2)下图是氮循环示意图,请回答下列问题。

①自然界中的固氮和人工固氮的共同点是将氮元素由游离态转化为
②雷电固氮反应的化学方程式是
③根据循环图判断下列说法不正确的是
a.氮元素均被氧化
b.工业合成氨属于人工固氮
c.含氮无机物和含氮有机物可相互转化
d.碳、氢、氧三种元素也参与了氮循环
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮是主要的非金属元素之一,也是人类较早认识的化学元素。氮元素也是生命元素,在自然界中有重要的循环过程。
(1)氨气的水溶液能使酚酞变红,请结合必要的化学用语解释原因_______ 。
(2)请写出实验室制 的化学方程式
的化学方程式_______ 。
(3)检验硝酸铵固体中铵根离子的实验方法_______ (写出步骤、现象、结论)。
(4)化肥氯化铵可以补充土壤中的氮元素,施用氯化铵时需要注意避免烈日曝晒,请结合必要的化学用语解释原因_______ 。
(1)氨气的水溶液能使酚酞变红,请结合必要的化学用语解释原因
(2)请写出实验室制
 的化学方程式
的化学方程式(3)检验硝酸铵固体中铵根离子的实验方法
(4)化肥氯化铵可以补充土壤中的氮元素,施用氯化铵时需要注意避免烈日曝晒,请结合必要的化学用语解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】概念辨析(括号内画“√”或“×”,正确的横线处不填,错误的说明原因)
(1)浓H2SO4与Cu、C的反应中,都体现了H2SO4的酸性和强氧化性。(___)____ 。
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应。(___)_____ 。
(3)铵盐加热均易分解且产生NH3。(___)_____ 。
(4)伴有能量变化的物质变化都是化学变化。(___)____ 。
(1)浓H2SO4与Cu、C的反应中,都体现了H2SO4的酸性和强氧化性。(___)
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应。(___)
(3)铵盐加热均易分解且产生NH3。(___)
(4)伴有能量变化的物质变化都是化学变化。(___)
您最近一年使用:0次
【推荐3】麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
(1)笑气是人类最早应用于医疗的麻醉剂之一,它可由NH4NO3在微热条件下分解产生,产物除N2O外还有一种,此反应的化学方程式为______________ 。有关理论认为N2O与CO2分子具有相似的结构(包括电子式),则其空间构型是_______ 型,N2O为_____________ 分子(极性或非极性)
(2)另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2 2HCl+2COCl2,为了防止事故,使用前可用于检验氯仿是否变质的试剂是_________ 。
A.淀粉-碘化钾溶液 B.NaOH溶液 C.酚酞溶液 D.硝酸酸化的AgNO3溶液
(1)笑气是人类最早应用于医疗的麻醉剂之一,它可由NH4NO3在微热条件下分解产生,产物除N2O外还有一种,此反应的化学方程式为
(2)另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2 2HCl+2COCl2,为了防止事故,使用前可用于检验氯仿是否变质的试剂是
A.淀粉-碘化钾溶液 B.NaOH溶液 C.酚酞溶液 D.硝酸酸化的AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求书写方程式:
(1)向NaAlO2溶液中通入过量CO2的离子方程式:____________________
(2)MnO2与浓盐酸制备氯气的离子方程式:__________________________
(3)工业上制备粗硅的化学方程式:___________________________________
(4)硫酸铵溶液与氢氧化钡溶液共热的离子方程式:___________________________ 。
(1)向NaAlO2溶液中通入过量CO2的离子方程式:
(2)MnO2与浓盐酸制备氯气的离子方程式:
(3)工业上制备粗硅的化学方程式:
(4)硫酸铵溶液与氢氧化钡溶液共热的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】易混易错题组:离子方程式的书写
(1)量变引起离子方程式的变化
将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为______________ 。
向Ca(HCO3)2溶液中滴加过量NaOH溶液,反应的离子方程式__________________ 。
(学法题)书写此类离子方程式的关键是,抓住______________ 量物质。
(2)反应顺序引起的变化
向NH4HCO3溶液中,滴加过量的NaOH溶液,反应的离子方程式为___________________ 。
在FeI2溶液中,滴加少量稀硝酸。该反应的离子方程式是:____________ 。
(学法题)书写此类离子方程式的关键是,抓住反应物中离子的__________ 顺序。
(3)反应介质的影响
①在酸性条件下,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为_________________ 。
②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为___________________________ 。
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是_______________ 。
④对比②和③实验所得的结果,将I2、ClO-、 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为___________ 。
(1)量变引起离子方程式的变化
将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为
向Ca(HCO3)2溶液中滴加过量NaOH溶液,反应的离子方程式
(学法题)书写此类离子方程式的关键是,抓住
(2)反应顺序引起的变化
向NH4HCO3溶液中,滴加过量的NaOH溶液,反应的离子方程式为
在FeI2溶液中,滴加少量稀硝酸。该反应的离子方程式是:
(学法题)书写此类离子方程式的关键是,抓住反应物中离子的
(3)反应介质的影响
①在酸性条件下,向含铬废水中加入FeSO4,可将
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是
④对比②和③实验所得的结果,将I2、ClO-、
 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是CaO。
(1)CaO属于___________ (填字母,下同)。
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物
H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、CaO等物质划分为一类。该同学的分类依据为___________。
(3)CaO可作干燥剂的理由是___________ (用化学方程式表示)。
(4)CaO可用于添加到燃煤中来减少对空气的污染,燃烧过程中体现CaO的性质是________ 。
(5)CaO氧化钙的说法正确的是___________
(1)CaO属于
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属氧化物
H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、CaO等物质划分为一类。该同学的分类依据为___________。
| A.酸 | B.碱 | C.氧化物 | D.干燥剂 |
(4)CaO可用于添加到燃煤中来减少对空气的污染,燃烧过程中体现CaO的性质是
(5)CaO氧化钙的说法正确的是___________
| A.误食CaO会导致口腔或食道被灼伤 |
| B.CaO的俗名是石灰石 |
| C.CaO可以用作建筑材料 |
| D.氧化钙作为钙肥,可以和磷肥和铵态氮肥混合使用 |
您最近一年使用:0次



