氮和氮的化合物与人类有密切关系,回答以下问题:
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
(2)下列说法正确的是_______。
(3)甲、乙两组同学用干燥的圆底烧瓶各收集一瓶氨气,根据下图喷泉实验的装置进行实验都观察到美丽的红色喷泉。
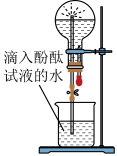
根据实验现象说明氨气具有的性质是_______ ,并用相应的方程式解释:_______ 。
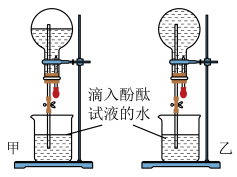
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度_______ (填“大于”、“小于”或“等于”)乙组同学所得氨水的物质的量浓度。
(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是_______ 。写出 ”的检验方法:
”的检验方法:_______ 。
(1)氮是植物生长的必需元素。有关说法中错误的是_______。
| A.氮气分子很稳定 | B.尿素属于铵态氮肥 |
| C.工业合成氨是人工固氮 | D.闪电实现了大气固氮 |
| A.可用稀HNO3与FeS固体反应制取H2S |
| B.SO2能使酸性KMnO4、氯水褪色,说明SO2具有漂白作用 |
| C.少量NO2和足量SO2混合气体通入BaCl2溶液中,产生的沉淀只有BaSO4 |
D.向某溶液中滴加几滴盐酸酸化的BaCl2溶液,产生不溶于稀硝酸的白色沉淀则该溶液中一定含有 |

根据实验现象说明氨气具有的性质是
(4)甲、乙两组同学完成喷泉实验后,圆底烧瓶中所得溶液如图所示。请通过分析确认:甲组同学所得氨水的物质的量浓度

(5)贮存铵态氮肥时要密封保存,并放在阴凉通风处,其原因是
 ”的检验方法:
”的检验方法:
更新时间:2023-01-14 09:20:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)工业上氨催化氧化生成NO的反应方程式为___________ 。
(2)下列化学反应属于固氮作用的是___________ (填字母代号)。
A.N2和H2在一定条件下反应生成NH3
B.NO遇O2转化为NO2
C.N2和O2放电时反应生成NO
D.由NH3制取碳酸氢铵
(3)肼(N2H4)又称联氨,是一种可燃性的液体,传统制备肼的方法是以NaClO氧化NH3,制得肼的稀溶液(NaClO对应还原产物为NaCl),该反应的离子方程式是___________ 。
(4)N和P是同族元素,PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是___________ (填字母代号)。
a.不能与NaOH反应
b.含离子键、共价键
c.受热会分解
(5)将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生0.25mol气体(不考虑N2O4),则所消耗的HNO3的物质的量是___________ 。
(1)工业上氨催化氧化生成NO的反应方程式为
(2)下列化学反应属于固氮作用的是
A.N2和H2在一定条件下反应生成NH3
B.NO遇O2转化为NO2
C.N2和O2放电时反应生成NO
D.由NH3制取碳酸氢铵
(3)肼(N2H4)又称联氨,是一种可燃性的液体,传统制备肼的方法是以NaClO氧化NH3,制得肼的稀溶液(NaClO对应还原产物为NaCl),该反应的离子方程式是
(4)N和P是同族元素,PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.不能与NaOH反应
b.含离子键、共价键
c.受热会分解
(5)将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生0.25mol气体(不考虑N2O4),则所消耗的HNO3的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
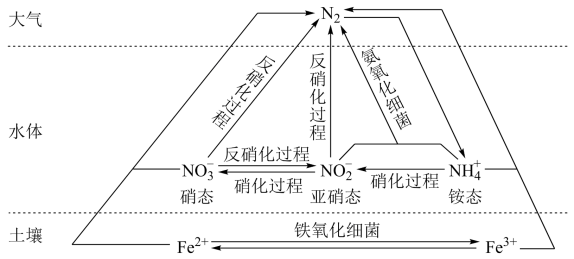
【推荐2】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。_______ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)农业生产过程中的铵态氮肥是水体中 的主要来源之一。
的主要来源之一。
①检验氮肥中 的实验方案是
的实验方案是_______ 。
②实验室制备少量氨气的化学方程式为_______ 。
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为_______ mol。
(4)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理_______ 。
(5)Fe2+与硝态氮(NO )反应脱氮生成N2,反应后的溶液为Fe(NO3)2和Fe(NO3)3的混合溶液。为检验溶液中含有Fe2+和Fe3+,相应的实验方案为
)反应脱氮生成N2,反应后的溶液为Fe(NO3)2和Fe(NO3)3的混合溶液。为检验溶液中含有Fe2+和Fe3+,相应的实验方案为_______ (实验中可选用的试剂:KSCN溶液、0.1mol·L-1的KMnO4溶液、3%的H2O2溶液)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)农业生产过程中的铵态氮肥是水体中
 的主要来源之一。
的主要来源之一。①检验氮肥中
 的实验方案是
的实验方案是②实验室制备少量氨气的化学方程式为
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理
(5)Fe2+与硝态氮(NO
 )反应脱氮生成N2,反应后的溶液为Fe(NO3)2和Fe(NO3)3的混合溶液。为检验溶液中含有Fe2+和Fe3+,相应的实验方案为
)反应脱氮生成N2,反应后的溶液为Fe(NO3)2和Fe(NO3)3的混合溶液。为检验溶液中含有Fe2+和Fe3+,相应的实验方案为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。
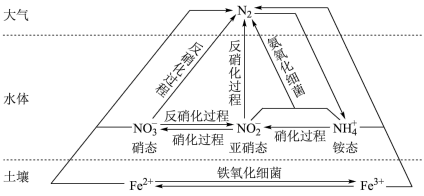
(1)氮循环中,属于氮的固定的有_______ (填字母序号,下同),属于氧化反应的有_______ 。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)铵态氮肥是水体中铵根的主要来源之一。氨气溶于水也能产生铵根,此过程中发生的反应有(用方程式表示)_______ ,检验某固态氮肥中铵根的实验操作与相应的现象及结论为_______ 。
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为_______ 。
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),原理为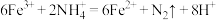 ,证明铁离子存在的实验操作及现象为:
,证明铁离子存在的实验操作及现象为:_______ 。
(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
①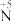 转化为
转化为 :
:_______
②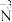 转化为
转化为 :
:_______

(1)氮循环中,属于氮的固定的有
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)铵态氮肥是水体中铵根的主要来源之一。氨气溶于水也能产生铵根,此过程中发生的反应有(用方程式表示)
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),原理为
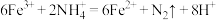 ,证明铁离子存在的实验操作及现象为:
,证明铁离子存在的实验操作及现象为:(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
①
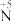 转化为
转化为 :
:②
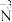 转化为
转化为 :
:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是某学习小组设计的利用氨气进行喷泉实验的装置示意图。

请回答下列问题:
(1)学生甲用装置 进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是________________________________________________________________________ 。
(2)学生乙将装置 误装为装置
误装为装置 ,但经与同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法与原理:
,但经与同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法与原理:_________________________________ 。

请回答下列问题:
(1)学生甲用装置
 进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是(2)学生乙将装置
 误装为装置
误装为装置 ,但经与同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法与原理:
,但经与同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法与原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口.立即倒置烧瓶,使玻璃管插入盛有水的烧杯里(预先在水里滴入少量酚酞溶液).打开橡皮管上的夹子,轻轻挤压滴管,使少量水进入烧瓶,可观察到的现象为: ________


您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将二氧化硫的水溶液在空气中放置一段时间后,在溶液中能检测到硫酸根离子的存在,且溶液的 变小,试说明其原因
变小,试说明其原因____ 。
 变小,试说明其原因
变小,试说明其原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】CuSO4是一种重要化工原料,其制备和有关性质如图所示。

(1)途径①②③,更好体现绿色化学思想的是______________ 。
(2)物质Y具有的性质是_________ (填“氧化性”或“还原性”)。
(3)混合气体X既能使品红溶液褪色又能使带火星木条复燃,则混合气体X的成分是_________ 。
(4)途径①所用混酸中H2SO4与HNO3物质的量之比是_________ 。并写出发生反应的离子方程式:__________________ 。

(1)途径①②③,更好体现绿色化学思想的是
(2)物质Y具有的性质是
(3)混合气体X既能使品红溶液褪色又能使带火星木条复燃,则混合气体X的成分是
(4)途径①所用混酸中H2SO4与HNO3物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等.
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为 .
(2)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)═6CaO(s)+P4(s)+5CO2(g)△H1=+Q1kJ•mol﹣1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣Q2kJ•mol﹣1
写出电炉中发生总反应的热化学方程式 .
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10;10C+P4O10=P4↑+10CO↑,上述反应中的各种物质,属于酸性氧化物的有 .
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如右图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象: ,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42﹣通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为 .

(Ⅲ)某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,利用相关工艺可进行提纯与综合利用.通入一定量的N2后,在1500℃下与Cl2充分反应得到纯化石墨与气体混合物,然后降温至80℃,分别得到不同状态的两类物质a和b.(注:石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃.)
(1)若a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性,化学反应方程式为 .
(2)若b与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有 .
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为 .
(2)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)═6CaO(s)+P4(s)+5CO2(g)△H1=+Q1kJ•mol﹣1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣Q2kJ•mol﹣1
写出电炉中发生总反应的热化学方程式 .
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10;10C+P4O10=P4↑+10CO↑,上述反应中的各种物质,属于酸性氧化物的有 .
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如右图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象: ,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42﹣通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为 .

(Ⅲ)某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,利用相关工艺可进行提纯与综合利用.通入一定量的N2后,在1500℃下与Cl2充分反应得到纯化石墨与气体混合物,然后降温至80℃,分别得到不同状态的两类物质a和b.(注:石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃.)
(1)若a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性,化学反应方程式为 .
(2)若b与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有 .
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应有工业生产、环保及科研中有广泛的应用,请根据以下信息,结合所掌握的化学知识,回答下列问题:
I.酸性KMnO4在生活、卫生医疗中常用作消毒剂。
(1)取300mL0.2mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是___________ mol。
(2)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474gKMnO4样品溶解酸化后,用0.100mol·L-1标准Na2S2O3溶液进行滴定,配平上述反应的离子方程式:___________ 。
______MnO +______S2O
+______S2O +______H+=______Mn2++______SO
+______H+=______Mn2++______SO +______H2O
+______H2O
实验中,滴定至终点时消耗Na2S2O3溶液12.00mL,则该样品中KMnO4的物质的量是___________ mol。按顺序写出检验SO 所需要的试剂
所需要的试剂___________ 。
II.钒性能优良,用途广泛,有金属“维生素”之称。
(3)将废钒催化剂(主要成分为V2O3)与稀硫酸、K2SO3溶液混合,充分反应后生成VO2+,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(4)V2O3能与盐酸反应生成VO2+和一种黄绿色气体,该黄绿色气体能与Na2SO3溶液反应而被吸收,则SO 、Cl-、VO2+的还原性由强到弱的顺序是
、Cl-、VO2+的还原性由强到弱的顺序是___________ 。
(5)偏钒酸铵在加热条件下反应会生成V2O5、NH3和H2O。V2O3在氮气氛围中,碳高温条件下还原氮化制备VN,还生成一种具有还原性的气体,则该反应的化学方程式为___________ 。生成标况下22.4L该还原性气体时,反应转电子数为___________ 。
I.酸性KMnO4在生活、卫生医疗中常用作消毒剂。
(1)取300mL0.2mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是
(2)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474gKMnO4样品溶解酸化后,用0.100mol·L-1标准Na2S2O3溶液进行滴定,配平上述反应的离子方程式:
______MnO
 +______S2O
+______S2O +______H+=______Mn2++______SO
+______H+=______Mn2++______SO +______H2O
+______H2O实验中,滴定至终点时消耗Na2S2O3溶液12.00mL,则该样品中KMnO4的物质的量是
 所需要的试剂
所需要的试剂II.钒性能优良,用途广泛,有金属“维生素”之称。
(3)将废钒催化剂(主要成分为V2O3)与稀硫酸、K2SO3溶液混合,充分反应后生成VO2+,该反应中氧化剂和还原剂的物质的量之比为
(4)V2O3能与盐酸反应生成VO2+和一种黄绿色气体,该黄绿色气体能与Na2SO3溶液反应而被吸收,则SO
 、Cl-、VO2+的还原性由强到弱的顺序是
、Cl-、VO2+的还原性由强到弱的顺序是(5)偏钒酸铵在加热条件下反应会生成V2O5、NH3和H2O。V2O3在氮气氛围中,碳高温条件下还原氮化制备VN,还生成一种具有还原性的气体,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】三位同学设计了下述三个方案,并都认为:如果观察到的现象和自己设计的方案一致,即可确定试液中有 。
。
方案甲:试液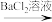 白色沉淀
白色沉淀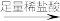 沉淀不溶解
沉淀不溶解
方案乙:试液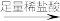 无沉淀
无沉淀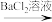 白色沉淀
白色沉淀
方案丙:试液 无沉淀
无沉淀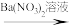 白色沉淀
白色沉淀
试评价上述各种方案是否严密,并分别说明理由。
(1)方案甲:___________ ,理由是___________ ;
(2)方案乙:___________ ,理由是___________ ;
(3)方案丙:___________ ,理由是___________ 。
 。
。方案甲:试液
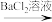 白色沉淀
白色沉淀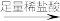 沉淀不溶解
沉淀不溶解方案乙:试液
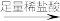 无沉淀
无沉淀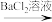 白色沉淀
白色沉淀方案丙:试液
 无沉淀
无沉淀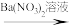 白色沉淀
白色沉淀试评价上述各种方案是否严密,并分别说明理由。
(1)方案甲:
(2)方案乙:
(3)方案丙:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某实验小组设计实验证明某碳酸钠粉末中混有硫酸钠和氯化钠,请完成下列空白:
| 实验步骤 | 实验现象 | 有关化学方程式 |
| ⑴取少量样品于试管中,加蒸馏水配成溶液。在溶液中先加足量的HNO3溶液 | 有气泡产生 | |
| ⑵再向(1)的溶液中加入过量的 | 产生白色沉淀 | |
| ⑶取(2)静置后的上层清液少许,滴加AgNO3溶液 | ||
| 结论:碳酸钠粉末中混有硫酸钠和氯化钠 | ||
您最近一年使用:0次



