水泥是重要的建筑材料,水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙的含量:先将水泥转变为草酸钙,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4-+H++H2C2O4→Mn2++CO2↑+H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.0500 mol·L−1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________ 。
2020高三·全国·专题练习 查看更多[2]
更新时间:2020/04/30 21:44:12
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】钢铁生锈的过程十分复杂,已知某铁锈含有Fe2O3•nH2O(n≤1),还可能有Fe(OH)3和FeCO3。某学习小组做了以下实验:
①取12.574g铁锈隔绝空气加热至恒重,得到固体10.528g。
②另取6.287g铁锈,在205.00 mL 1.000mol/L的稀硝酸中恰好完全溶解,产生NO气体89.60 mL(标准状况)。
(1)根据实验①,铁锈中是否只含Fe2O3•nH2O?试通过计算回答。
_____________ ,_____________ ;
(2)根据实验②,能否确定铁锈中含有FeCO3?理由是什么?
_____________ ,_____________ ;
(3)若n=0.8,试通过计算确定6.287g铁锈的成分以及它们的物质的量。
_____________ ;
①取12.574g铁锈隔绝空气加热至恒重,得到固体10.528g。
②另取6.287g铁锈,在205.00 mL 1.000mol/L的稀硝酸中恰好完全溶解,产生NO气体89.60 mL(标准状况)。
(1)根据实验①,铁锈中是否只含Fe2O3•nH2O?试通过计算回答。
(2)根据实验②,能否确定铁锈中含有FeCO3?理由是什么?
(3)若n=0.8,试通过计算确定6.287g铁锈的成分以及它们的物质的量。
您最近一年使用:0次
【推荐2】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
请回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是______ g,产生氢气的体积(标准状况)_________ L。
(2)反应②中_________ 作氧化剂,___________ 是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是____________ 。
(4)用单线桥法表示反应③电子转移的方向和数目。KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
______________
(5)反应③中盐酸表现_________________ 性。
②Cu+2H2SO4(浓)
 CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
请回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是
(2)反应②中
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是
(4)用单线桥法表示反应③电子转移的方向和数目。KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(5)反应③中盐酸表现
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】生活离不开化学,家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①漂白粉;②NaClO;③Cl2;④Na2CO3;⑤小苏打(NaHCO3);⑥生铁;⑦甲烷。回答下列问题:
(1)漂白液的有效成分NaClO在水溶液的电离方程式:___________ 。
(2)厨卫用品的主要成分(括号内的物质):是电解质的有___________ (填序号,下同),是非电解质的有___________ 。
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为___________ g。
(4)实验室制Cl2的化学方程式___________ ,收集到33.6L(折算到标准状态)氯气时该反应总共转移的电子数___________ 。
(1)漂白液的有效成分NaClO在水溶液的电离方程式:
(2)厨卫用品的主要成分(括号内的物质):是电解质的有
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为
(4)实验室制Cl2的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】镁带在空气中充分燃烧后,将所得固体产物加到50mL一定浓度的盐酸中,向该溶液中加入0.50 mol•L-1的NaOH溶液所得某些产物与加入NaOH溶液体积的关系如图所示(不考虑气体溶解)。(已知:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑)请计算:
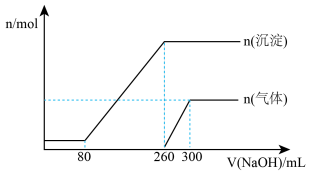
(1)加NaOH反应后产生NH3的体积为_______ L(标况)
(2)该盐酸的物质的量浓度为_______ mol•L-1
(3)燃烧产物中氮化镁的质量为_______ g。

(1)加NaOH反应后产生NH3的体积为
(2)该盐酸的物质的量浓度为
(3)燃烧产物中氮化镁的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】肼(N2H4)是一种强还原剂,用 与
与 反应可用于生产肼(N2H4),其反应的化学方程式为:
反应可用于生产肼(N2H4),其反应的化学方程式为: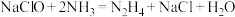 。工业碱性
。工业碱性 溶液中含有
溶液中含有 会影响所得肼的产品质量。测定碱性
会影响所得肼的产品质量。测定碱性 溶液中的
溶液中的 含量的方法如下:取
含量的方法如下:取 碱性
碱性 溶液试样,加入过量
溶液试样,加入过量 ,将
,将 完全还原
完全还原 (
( 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,除去过量的
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,除去过量的 ,冷却至室温,加入稀硫酸至酸性,再加入
,冷却至室温,加入稀硫酸至酸性,再加入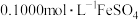 溶液
溶液 ,充分反应,将
,充分反应,将 完全还原
完全还原 ,再用
,再用 酸性
酸性 溶液氧化多余的
溶液氧化多余的 (
( 被还原为
被还原为 ),消耗酸性
),消耗酸性 溶液
溶液 。
。
(1) 与次氯酸钠反应的离子方程式为
与次氯酸钠反应的离子方程式为_______ 。
(2)通常不选用盐酸酸化 的原因是
的原因是_______ 。
(3)计算样品中 的含量(以g/L表示),写出计算过程。
的含量(以g/L表示),写出计算过程。_______ 。
 与
与 反应可用于生产肼(N2H4),其反应的化学方程式为:
反应可用于生产肼(N2H4),其反应的化学方程式为: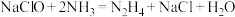 。工业碱性
。工业碱性 溶液中含有
溶液中含有 会影响所得肼的产品质量。测定碱性
会影响所得肼的产品质量。测定碱性 溶液中的
溶液中的 含量的方法如下:取
含量的方法如下:取 碱性
碱性 溶液试样,加入过量
溶液试样,加入过量 ,将
,将 完全还原
完全还原 (
( 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,除去过量的
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,除去过量的 ,冷却至室温,加入稀硫酸至酸性,再加入
,冷却至室温,加入稀硫酸至酸性,再加入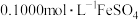 溶液
溶液 ,充分反应,将
,充分反应,将 完全还原
完全还原 ,再用
,再用 酸性
酸性 溶液氧化多余的
溶液氧化多余的 (
( 被还原为
被还原为 ),消耗酸性
),消耗酸性 溶液
溶液 。
。(1)
 与次氯酸钠反应的离子方程式为
与次氯酸钠反应的离子方程式为(2)通常不选用盐酸酸化
 的原因是
的原因是(3)计算样品中
 的含量(以g/L表示),写出计算过程。
的含量(以g/L表示),写出计算过程。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】将3.9 g Mg、Al合金溶于一定物质的量浓度的HCl溶液400 mL中,刚好完全反应,经检测合金和盐酸都无剩余,再向反应后的溶液中加入1mol/L的NaOH溶液后,生成沉淀。如果加入一定量的NaOH溶液至沉淀量最大时,溶液的总体积刚好为合金溶解时体积的两倍,假设完全反应(不考虑体积变化),试求:
(1)生成的沉淀的最大值是多少_________ ?
(2)原合金中Mg的质量百分含量_________ (计算结果保留一位小数点)。
(1)生成的沉淀的最大值是多少
(2)原合金中Mg的质量百分含量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将一定量NaHCO3和Na2CO3的混合物充分加热,使NaHCO3完全分解,混合物质量减少了3.1g,将加热后剩余的固体物质与足量盐酸反应,收集到8.8g气体。计算原固体混合物中Na2CO3和NaHCO3的物质的量各为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】现有含碳酸钠杂质的氯化钠样品10克,与足量的盐酸反应,生成的气体在标准状况下体积为224mL,求:
(1)生成的气体是______________,物质的量为____________。
(2)该样品中含氯化钠的质量分数?(写出计算过程)
(1)生成的气体是______________,物质的量为____________。
(2)该样品中含氯化钠的质量分数?(写出计算过程)
您最近一年使用:0次



