某容器中发生一个化学反应,反应过程存在H2O、ClO-、CN-、HCO3-、N2、Cl-6种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是


| A.当有3molClO-参加反应时,则有1molN2生成 |
| B.HCO3-作为碱性介质参与反应 |
| C.当有5molClO-参加反应时,则有1molN2生成 |
| D.若生成2.24LN2,则转移电子0.6mol |
更新时间:2020-04-27 16:33:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】将NO3-+Zn+OH-+H2O → NH3+Zn(OH)42- 配平后,离子方程式中H2O的系数是
| A.2 | B.4 | C.6 | D.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种易溶于水、高效的多功能水处理剂。工业上通常先制得高铁酸钠,然后在一定温度下,向高铁酸钠溶液中加入KOH至饱和,从而使高铁酸钾析出。下列叙述正确的是( )
| A.高铁酸钾溶于水可吸附水中悬浮物,净水原理和明矾相同 |
| B.高铁酸钾与水反应生成O2、Fe(OH)3(胶体)和KOH,该反应中高铁酸钾既做氧化剂又做还原剂 |
| C.在无水条件下制备高铁酸钠的主要反应为2FeSO4+a Na2O2=2Na2FeO4+bX+2Na2SO4+cO2↑,该反应中物质X的化学式为NaOH |
| D.向Fe(OH)3和过量KOH溶液的混合物中通入氯气,得到紫色固体的反应为3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O |
您最近一年使用:0次
【推荐3】Ar气氛下,高价态钒镁氧化物晶体作为催化剂进行乙苯脱氢制备苯乙烯,并将CO2转化为CO,反应机理如图(a)所示;同时采用电解法处理含苯乙烯的废水,其工作原理如图(b)(电解液是含苯乙烯和硫酸的废水,pH≈ 6),已知:·OH具有很强的氧化性。下列说法不正确的是
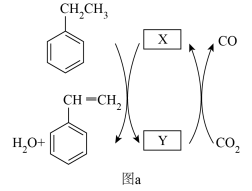
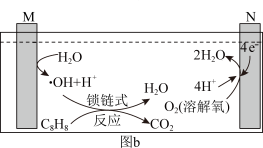


| A.图a由MgVmOn+1转化为MgVmOn的过程,乙苯发生氧化反应 |
| B.M连接电源的正极 |
| C.苯乙烯被·OH氧化的化学方程式为C8H8-40e- +40·OH =8CO2↑+ 24H2O |
| D.若电路中通过10mol电子,理论上有26g苯乙烯(M= 104 g/mol)被氧化成CO2和H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A 为26.88L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol/L,则关于该反应下列叙述中错误的是
| A.反应中共消耗Zn 91g |
| B.气体A 中SO2 和H2 的体积比为1:1 |
| C.硫酸分子的氧化性强于H+ |
| D.反应中共转移2.4mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】据报道,我国科学家找到了水稻突变体“耐砷富硒”开关,这对提高水稻营养价值、降低砷的毒性意义重大。下列说法错误的是
| A.砷与磷属于同族元素 | B.原子半径: |
C. 既有氧化性又有还原性 既有氧化性又有还原性 | D.砷的简单氢化物为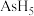 |
您最近一年使用:0次

 、CO都属于酸性氧化物
、CO都属于酸性氧化物 和
和 分子存在
分子存在

