Ar气氛下,高价态钒镁氧化物晶体作为催化剂进行乙苯脱氢制备苯乙烯,并将CO2转化为CO,反应机理如图(a)所示;同时采用电解法处理含苯乙烯的废水,其工作原理如图(b)(电解液是含苯乙烯和硫酸的废水,pH≈ 6),已知:·OH具有很强的氧化性。下列说法不正确的是
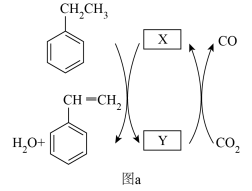
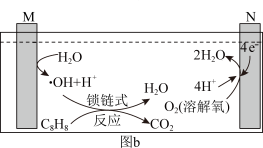


| A.图a由MgVmOn+1转化为MgVmOn的过程,乙苯发生氧化反应 |
| B.M连接电源的正极 |
| C.苯乙烯被·OH氧化的化学方程式为C8H8-40e- +40·OH =8CO2↑+ 24H2O |
| D.若电路中通过10mol电子,理论上有26g苯乙烯(M= 104 g/mol)被氧化成CO2和H2O |
2023·黑龙江哈尔滨·模拟预测 查看更多[2]
更新时间:2023-06-13 23:33:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业用铜矿石(主要含有CuS、CuO)制取胆矾的主要流程如图所示。下列说法错误的是
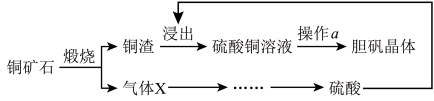

| A.气体X为SO2 |
| B.操作a为蒸发 |
| C.流程中铜元素化合价没有变化 |
| D.用流程中生成的硫酸浸出铜渣,还需另外补充硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】能正确表示下列反应的离子方程式是
A.用碳酸钠溶液处理水垢中的硫酸钙: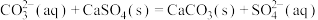 |
B.用足量氨水吸收二氧化硫: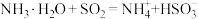 |
C.向草酸溶液中滴加酸性高锰酸钾溶液: |
D.将等物质的量浓度的氢氧化钡溶液和硫酸氢铵溶液以体积比1∶2混合: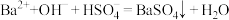 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠(xNa2CO3•yH2O2)。
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:
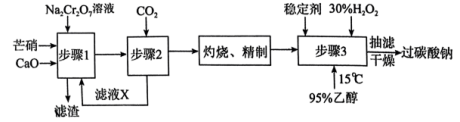
Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:

Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
| A.步骤1中2mol芒硝参与反应时,消耗1molNa2Cr2O7 |
| B.滤渣的主要成分为CaSO4 |
C.步骤2的方程式为2Na2CrO4+2CO2+H2O Na2Cr2O7+2NaHCO3↓ Na2Cr2O7+2NaHCO3↓ |
| D.稳定剂的作用是阻止微量杂质金属离子的催化作用,减少双氧水的分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以纯碱溶液为原料,通过电解的方法可制备小苏打,原理装置图如下:

上述装置工作时,下列有关说法正确的是

上述装置工作时,下列有关说法正确的是
A.乙池电极接电池正极,气体X为 |
B. 由乙池穿过交换膜进入甲池 由乙池穿过交换膜进入甲池 |
C.甲池中只发生反应: |
| D.NaOH溶液Z的浓度比NaOH溶液Y的小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】铀(U)可用作核燃料。核废料中+6价的铀[U(Ⅵ)]可以通过以下两种方法处理。电化学还原法。U(Ⅵ)还原为U(Ⅳ)的电化学装置如图-1所示。

阴极上发生反应: 、
、
阴极区溶液中发生反应: 、
、
以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图-2所示。下列说法不 正确的是

阴极上发生反应:
 、
、
阴极区溶液中发生反应:
 、
、
以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图-2所示。下列说法
A.反应 中,每生成0.1 mol N2转移电子0.4 mol 中,每生成0.1 mol N2转移电子0.4 mol |
| B.阴极区溶液中加入N2H5NO3的目的是消耗反应中生成HNO2,防止HNO2与U4+反应 |
| C.电解0~100 min,电路中每转移1 mol e-,阴极区H+减少2 mol |
D.100~200 min,c(H+)下降速率低于100 min前,原因是相同时间内,转移等量电子时, 比 比 消耗的 消耗的 更少,且生成的HNO2与 更少,且生成的HNO2与 反应有H+生成 反应有H+生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】液态太阳燃料是利用太阳能将温室气体二氧化碳作为碳资源,是践行生态文明建设的一个重要举措,其技术路线如图所示。下列有关说法错误的是


| A.太阳能最终转化为电能和热能 |
B.燃料电池正极反应式为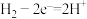 |
| C.H2O和CO2可循环利用 |
| D.该技术的关键是氢气如何安全、高效储存及转移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用下图所示装置提纯含有碳酸钾杂质的粗 溶液。下列说法正确的是
溶液。下列说法正确的是

 溶液。下列说法正确的是
溶液。下列说法正确的是
A.粗 溶液从 溶液从 处加入 处加入 |
B.电子从电极 经导线流向电极 经导线流向电极 |
C.电极 的电极反应为 的电极反应为 |
D. 穿过阳离子交换膜时,电极 穿过阳离子交换膜时,电极 上产生气体体积 上产生气体体积 (标准状况) (标准状况) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用惰性电极电解AgNO3溶液一段时间后,下列有关说法正确的是
| A.阳极质量增加 |
| B.向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况 |
| C.电解过程中溶液的pH不断升高 |
| D.电解后两极产生的气体体积比为2:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将1 L含有0.4 mol Cu(NO3)2和0.4 mol KCl的水溶液,用惰性电极电解一段时间后,在一电极上析出19.2 g Cu。此时,在另一电极上放出气体的体积在标准状况下为(不考虑产生的气体在水中的溶解)( )
| A.6.72 L | B.13.44 L | C.3.36 L | D.5.6 L |
您最近一年使用:0次


 和
和 ,原理如图所示。下列说法不正确的是
,原理如图所示。下列说法不正确的是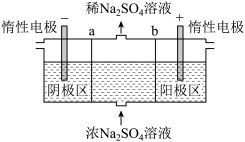
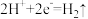

 增大
增大
 时还可得到硫酸和
时还可得到硫酸和 电子时,有
电子时,有 生成
生成

