下列说法正确的是( )
| A.F、Cl、Br原子的最外层电子数都是7,次外层电子数都是8 |
| B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律 |
| C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用 |
| D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4 |
更新时间:2020-05-06 12:17:25
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】2016年IUPAC将117号元素符号定为Ts,Ts的最外层电子数是7。下列说法正确的是
| A.在同族元素中非金属性最弱 |
B.中子数为176的Ts,其核素符号是 |
| C.Ts是第七周期第ⅥA族元素 |
| D.Ts的气态氢化物在同族氢化物中最稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是
| 选项 | 陈述Ⅰ | 类比推理陈述Ⅱ |
| A | 单质的熔点Br2<I2 | 单质的熔点Li<Na |
| B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
| C | 还原性:I->Br- | 还原性:S2->O2- |
| D | 实验室:Cl2+2KBr(aq)=2KCl(aq)+Br2 | 实验室:F2+2KBr(aq)=2KF(aq)+Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】短周期元素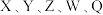 在元素周期表中的相对位置如图所示,其中
在元素周期表中的相对位置如图所示,其中 原子的质子数是其
原子的质子数是其 层电子数的三倍,下列说法不正确的是
层电子数的三倍,下列说法不正确的是
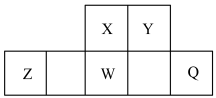
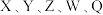 在元素周期表中的相对位置如图所示,其中
在元素周期表中的相对位置如图所示,其中 原子的质子数是其
原子的质子数是其 层电子数的三倍,下列说法不正确的是
层电子数的三倍,下列说法不正确的是
A.与Y同主族的短周期元素,其最高价氧化物中氧元素的质量分数为 |
B.最高价氧化物对应水化物的酸性: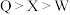 |
C.简单离子半径: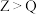 |
D.非金属性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】随着原子序数的递增,下列说法正确的是( )
| A.最外层电子数逐渐增多 |
| B.原子半径逐渐减小 |
| C.元素的主要化合价逐渐增加 |
| D.元素的化合价、原子半径、最外层电子数、得失电子能力、金属性与非金属性呈周期性变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列叙述正确的有( )
①卤素原子的最外层均有7个电子,次外层均有8个电子
②Li、Na、K的原子半径和密度随原子序数的增加而增大
③碱金属元素和卤素在自然界中都只以化合态形式存在
④液溴易挥发,在存放液溴的试剂瓶中应加水液封
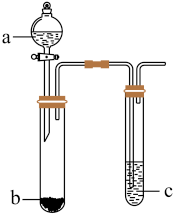
⑤如图所示,若a、b、c中分别盛放浓盐酸、 固体、淀粉KI溶液,则通过实验可证明氧化性:
固体、淀粉KI溶液,则通过实验可证明氧化性: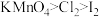
①卤素原子的最外层均有7个电子,次外层均有8个电子
②Li、Na、K的原子半径和密度随原子序数的增加而增大
③碱金属元素和卤素在自然界中都只以化合态形式存在
④液溴易挥发,在存放液溴的试剂瓶中应加水液封
⑤如图所示,若a、b、c中分别盛放浓盐酸、
 固体、淀粉KI溶液,则通过实验可证明氧化性:
固体、淀粉KI溶液,则通过实验可证明氧化性: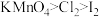

| A.5句 | B.4句 | C.3句 | D.2句 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知各共价键的键能如表所示,下列说法正确的是
| 共价键 | H—H | F—F | H—F | H—Cl | H—I |
| 键能E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
| A.键的极性大小顺序:H—I>H—Cl>H—F |
| B.表中最稳定的共价键是F—F键 |
| C.432kJ/mol>E(H—Br)>298kJ/mol |
| D.上述键能可以说明热稳定性的顺序是:HF<HCl<HI |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是( )
| A.O、S、Na的原子半径依次减小 |
| B.LiOH、KOH、CsOH的碱性依次减弱 |
| C.NH3、PH3、SiH4的热稳定性依次减弱 |
| D.HCl、HBr、HI的还原性依次减弱 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列实验操作无法达到目的的是
| A | B | C | D |
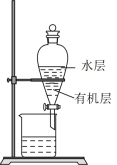 |  |  | 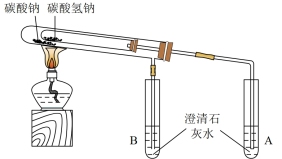 |
| 分离溴苯与水 | 石油的分馏 | 比较C和Si的非金属性 | 比较NaHCO3和Na2CO3的热稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 、
、 分别与
分别与 反应
反应 、
、 溶液中通入过量氨气
溶液中通入过量氨气 轨道上有5个电子,Z与Y属于同一主族,X的气态氢化物水溶液呈碱性。下列说法正确的是
轨道上有5个电子,Z与Y属于同一主族,X的气态氢化物水溶液呈碱性。下列说法正确的是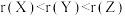
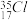 与
与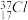 得电子能力相同
得电子能力相同

