(1)家用液化气的主要成分之一是丁烷(C4H10),当1 kg丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5×104kJ,试写出表示丁烷燃烧热的热化学方程式:________
(2)已知:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的悬浮气,且混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为_______________ 。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=—24.8 kJ·mol-1
3Fe2O3 (s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=—47.4 kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5 kJ·mol-1
写出CO(g)还原FeO(s)得到Fe (s)体和CO2(g)的热化学反应方程式:___________ 。
(2)已知:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的悬浮气,且混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=—24.8 kJ·mol-1
3Fe2O3 (s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=—47.4 kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5 kJ·mol-1
写出CO(g)还原FeO(s)得到Fe (s)体和CO2(g)的热化学反应方程式:
更新时间:2020-05-18 18:32:27
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.已知下列热化学方程式:①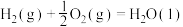
 kJ/mol,
kJ/mol,
②
 kJ/mol,
kJ/mol,
③
 kJ/mol,
kJ/mol,
④
 kJ/mol,回答下列问题:
kJ/mol,回答下列问题:
(1)C燃烧热的热化学方程式为___________ ;(填序号)
(2)燃烧1 g 生成气态水,放出的热量为
生成气态水,放出的热量为___________ 。
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为
 kJ/mol。
kJ/mol。
(3)下列各组试剂混合发生反应的离子方程式为 的是
的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1mol ,则反应放出的热量
,则反应放出的热量___________ (填“大于”“等于”或“小于”)57.3kJ。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热
___________ 0。
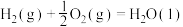
 kJ/mol,
kJ/mol,②

 kJ/mol,
kJ/mol,③

 kJ/mol,
kJ/mol,④

 kJ/mol,回答下列问题:
kJ/mol,回答下列问题:(1)C燃烧热的热化学方程式为
(2)燃烧1 g
 生成气态水,放出的热量为
生成气态水,放出的热量为Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为

 kJ/mol。
kJ/mol。(3)下列各组试剂混合发生反应的离子方程式为
 的是
的是A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1mol
 ,则反应放出的热量
,则反应放出的热量Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】文献查阅得到如下数据:
C2H4的燃烧热为1411kJ/mol
C2H6的燃烧热为1558kJ/mol
H2的燃烧热为285.8kJ/mol
(1)表示气体C2H4燃烧热的热化学方程式为____ 。
(2)C2H4(g)+H2(g)=C2H6(g) ΔH=____ 。
(3)已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol,一些化学键键能如下:H—H为436kJ/mol;O=O为498kJ/mol;则O—H键的键能为____ kJ/mol。
(4)用C2H4与O2可以组成新型燃料电池,若该电池以Pt为电极,以KOH为电解质溶液,写出该燃料电池的负极反应式____ 。用该电池作为电源电解600mL0.2mol/LCuSO4溶液,当转移0.06mol电子时消耗标准状况下O2的体积为____ L;此时,电解后溶液的pH为____ 。(假设电解后溶液体积不变)
C2H4的燃烧热为1411kJ/mol
C2H6的燃烧热为1558kJ/mol
H2的燃烧热为285.8kJ/mol
(1)表示气体C2H4燃烧热的热化学方程式为
(2)C2H4(g)+H2(g)=C2H6(g) ΔH=
(3)已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol,一些化学键键能如下:H—H为436kJ/mol;O=O为498kJ/mol;则O—H键的键能为
(4)用C2H4与O2可以组成新型燃料电池,若该电池以Pt为电极,以KOH为电解质溶液,写出该燃料电池的负极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)丙烯腈可用“丙烯氨氧化法”生产,生成丙烯腈的热化学方程式为:
CH2=CHCH3(g)+NH3(g)+3/2O2(g)= CH2=CHCN (g)+3H2O(g) △H=-515kJ/mol。该法在生产中有多种副产物生成,其中丙烯醛是主要副产物之一。若气态丙烯与氧气反应生成22.4g气态丙烯醛和水蒸气,同时放出141.2kJ热量,则反应的热化学方程式为:______ ,该反应在任何温度下都能自发进行,其原因是______ 。
(2)图(a)为在某一时间段一密闭体系中生成丙烯腈的反应速率与反应进程的曲线关系。由图可知,t1时刻表示体系改变的反应条件为______ ;t2时刻表示体系改变的另一反应条件为______ ,此时平衡______ 移动(填“正向”、“逆向”或“不”)。
(3)图(b)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃ 。在相同的反应时间内,高于460℃时丙烯腈产率降低的可能原因是______ (填序号)。
A.平衡常数变大
B.平衡常数变小
C.副反应增多
D.反应活化能增大
在相同的反应时间内.低于460℃时丙烯腈的产率______ (填“是”或“不是”)对应温度下的平衡转化率,判断理由是_________ 。
CH2=CHCH3(g)+NH3(g)+3/2O2(g)= CH2=CHCN (g)+3H2O(g) △H=-515kJ/mol。该法在生产中有多种副产物生成,其中丙烯醛是主要副产物之一。若气态丙烯与氧气反应生成22.4g气态丙烯醛和水蒸气,同时放出141.2kJ热量,则反应的热化学方程式为:
(2)图(a)为在某一时间段一密闭体系中生成丙烯腈的反应速率与反应进程的曲线关系。由图可知,t1时刻表示体系改变的反应条件为

(3)图(b)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃ 。在相同的反应时间内,高于460℃时丙烯腈产率降低的可能原因是
A.平衡常数变大
B.平衡常数变小
C.副反应增多
D.反应活化能增大
在相同的反应时间内.低于460℃时丙烯腈的产率
您最近一年使用:0次
【推荐2】低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)用 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
_____  (用含a、b的式子表示)。
(用含a、b的式子表示)。

(2)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:

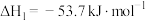


则

_____  。
。
(3)在 (g)完全燃烧生成
(g)完全燃烧生成 和液态水的反应中,每有1molCO2生成时,放出650kJ的热量,写出
和液态水的反应中,每有1molCO2生成时,放出650kJ的热量,写出 (g)燃烧热的热化学方程式
(g)燃烧热的热化学方程式_____ 。
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取C的太阳能工艺如图:
制取C的太阳能工艺如图:

①工艺过程中的能量转化形式为_____ 。
②已知“重整系统”发生的反应中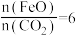 ,则
,则 (y<8)的化学式为
(y<8)的化学式为_____ ,“热分解系统”中每转移2mol电子,需消耗
_____ mol。
(1)用
 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: ,该反应体系的能量随反应过程变化关系如图所示,则该反应的
,该反应体系的能量随反应过程变化关系如图所示,则该反应的
 (用含a、b的式子表示)。
(用含a、b的式子表示)。
(2)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
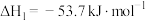


则


 。
。(3)在
 (g)完全燃烧生成
(g)完全燃烧生成 和液态水的反应中,每有1molCO2生成时,放出650kJ的热量,写出
和液态水的反应中,每有1molCO2生成时,放出650kJ的热量,写出 (g)燃烧热的热化学方程式
(g)燃烧热的热化学方程式(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取C的太阳能工艺如图:
制取C的太阳能工艺如图:
①工艺过程中的能量转化形式为
②已知“重整系统”发生的反应中
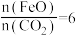 ,则
,则 (y<8)的化学式为
(y<8)的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
(1)已知298K时白磷、红磷完全燃烧的热化学方程式分别为P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1,P(红磷,s)+ O2(g)=
O2(g)=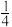 P4O10(s)ΔH2=-738.5kJ·mol-1。则该温度下白磷转化为红磷的热化学方程式为
P4O10(s)ΔH2=-738.5kJ·mol-1。则该温度下白磷转化为红磷的热化学方程式为___ 。
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) ΔH=-1638kJ·mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),恰好完全反应,则所得到的P4O10与P4O6的物质的量之比为___ ,反应过程中放出的热量为____ 。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P198,Cl—Cl243,P—Cl331。

则反应P4(白磷,s)+6Cl2(g)=4PCl3(s)的反应热ΔH=___ 。
(4)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为-890.2kJ•mol-1、-285.8kJ•mol-1和-283.0kJ•mol-1,则生成1molCO所需热量为___ 。
(1)已知298K时白磷、红磷完全燃烧的热化学方程式分别为P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1,P(红磷,s)+
 O2(g)=
O2(g)=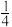 P4O10(s)ΔH2=-738.5kJ·mol-1。则该温度下白磷转化为红磷的热化学方程式为
P4O10(s)ΔH2=-738.5kJ·mol-1。则该温度下白磷转化为红磷的热化学方程式为(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) ΔH=-1638kJ·mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),恰好完全反应,则所得到的P4O10与P4O6的物质的量之比为
(3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P198,Cl—Cl243,P—Cl331。

则反应P4(白磷,s)+6Cl2(g)=4PCl3(s)的反应热ΔH=
(4)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为-890.2kJ•mol-1、-285.8kJ•mol-1和-283.0kJ•mol-1,则生成1molCO所需热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)足量 在
在 中完全燃烧生成
中完全燃烧生成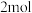 液态水,放出
液态水,放出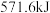 的热量,
的热量, 的燃烧热ΔH=
的燃烧热ΔH=___________ 。
(2)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:___________ 。
(3)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:

下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
CO2与H2转化为1 mol CH3OH(g)和H2O(g)的反应为___________ 反应(填吸热或放热),其ΔH=___________ 。
(4)已知下列两个热化学方程式:
 ,
,
 则
则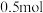 丙烷燃烧生成
丙烷燃烧生成 和气态水时释放的热量为
和气态水时释放的热量为___________ 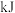
(5)已知:2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol,CO(g)+1/2O2(g)=CO2(g) ∆H=-283.0kJ/mol。某 和
和 的混合气体完全燃烧时放出
的混合气体完全燃烧时放出 热量,同时生成
热量,同时生成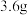 液态水,则原混合气体中
液态水,则原混合气体中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(1)足量
 在
在 中完全燃烧生成
中完全燃烧生成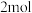 液态水,放出
液态水,放出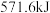 的热量,
的热量, 的燃烧热ΔH=
的燃烧热ΔH=(2)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:
(3)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:

下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
(4)已知下列两个热化学方程式:

 ,
,
 则
则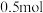 丙烷燃烧生成
丙烷燃烧生成 和气态水时释放的热量为
和气态水时释放的热量为
(5)已知:2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol,CO(g)+1/2O2(g)=CO2(g) ∆H=-283.0kJ/mol。某
 和
和 的混合气体完全燃烧时放出
的混合气体完全燃烧时放出 热量,同时生成
热量,同时生成 液态水,则原混合气体中
液态水,则原混合气体中 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为___________ 。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。。
(1)H2燃烧热的热化学方程式为
(2)燃烧1gH2生成液态水,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
【推荐3】氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)===2H2O(1) ΔH=-572kJ·mol-1。请回答下列问题:
(1)生成物能量总和_____ (填“大于”“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量______ (填“大于”“小于”或“等于”)572kJ。
(3)H2的标准燃烧热ΔH=_____ 。
(4)反应2H2+O2 2H2O的能量变化如图所示。
2H2O的能量变化如图所示。

已知拆开1molH2、1molO2和1 mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)_____ (填“吸收”或“放出”)_____ kJ。
(1)生成物能量总和
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量
(3)H2的标准燃烧热ΔH=
(4)反应2H2+O2
 2H2O的能量变化如图所示。
2H2O的能量变化如图所示。
已知拆开1molH2、1molO2和1 mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= +49.0kJ/mol
②CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
由上述方程式可知:CH3OH的燃烧热____ (填“大于”“等于”或“小于”)192.9kJ/mol。已知水的气化热为44kJ/mol。则表示氢气燃烧热的热化学方程式为___ 。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式___ 。
(3)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1= -272.0kJ/mol
O2(g)=FeO(s) ΔH1= -272.0kJ/mol
②2Al(s)+ O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是___ 。铝热反应的反应类型___ ,某同学认为,铝热反应可用于工业炼铁,你的判断是____ (填“能”或“不能”),你的理由____ 。
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101KPa下:
①H2(g)+ O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol
②CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____ 。
②CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol由上述方程式可知:CH3OH的燃烧热
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(3)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1= -272.0kJ/mol
O2(g)=FeO(s) ΔH1= -272.0kJ/mol②2Al(s)+
 O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2= -1675.7kJ/molAl和FeO发生铝热反应的热化学方程式是
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101KPa下:
①H2(g)+
 O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol②CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol写出CO2和H2生成气态甲醇等产物的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷还能让心脏有规律地跳动、维持肾脏正常机能和传达神经刺激的重要物质。许多磷的化合物是工业上的重要原料。请完成下列填空:
P(s,红磷)+ O2(g)=
O2(g)= P4O10(s)+738.5 kJ
P4O10(s)+738.5 kJ
P4(s,白磷)+ 5O2(g)=P4O10(s)+2983.2 kJ
(1)则白磷转化为红磷的热化学方程式_____________________ 。
(2)红磷在KOH溶液的悬浊液中和KOCl作用,可以生成K6P6O12的钾盐和KCl等产物。请写出该反应的化学方程式,并标出电子转移方向和数目。____
(3)制备MgNH4PO4时通常在镁盐(如氯化镁)溶液中加Na2HPO4 、氨水和铵盐溶液(如氯化铵),反应式为MgCl2+Na2HPO4+NH3=2NaCl+MgNH4PO4↓。在此反应中,如果不加铵盐,在碱性溶液中,Mg2+将会被氨水沉淀,其离子方程式为____________________ ;加入铵盐之后,可防止产生Mg(OH)2沉淀。请用电离平衡原理解释原因:_________
(4)H3PO3与碘水反应,碘水的棕黄色褪去,生成磷酸,向上述反应后的溶液中加入过量的AgNO3溶液,生成黄色沉淀。则H3PO3与碘水反应的化学方程式为___________ ;黄色沉淀是_________ ,可用作于_____________________ (写出任意一种用途即可)。
P(s,红磷)+
 O2(g)=
O2(g)= P4O10(s)+738.5 kJ
P4O10(s)+738.5 kJ P4(s,白磷)+ 5O2(g)=P4O10(s)+2983.2 kJ
(1)则白磷转化为红磷的热化学方程式
(2)红磷在KOH溶液的悬浊液中和KOCl作用,可以生成K6P6O12的钾盐和KCl等产物。请写出该反应的化学方程式,并标出电子转移方向和数目。
(3)制备MgNH4PO4时通常在镁盐(如氯化镁)溶液中加Na2HPO4 、氨水和铵盐溶液(如氯化铵),反应式为MgCl2+Na2HPO4+NH3=2NaCl+MgNH4PO4↓。在此反应中,如果不加铵盐,在碱性溶液中,Mg2+将会被氨水沉淀,其离子方程式为
(4)H3PO3与碘水反应,碘水的棕黄色褪去,生成磷酸,向上述反应后的溶液中加入过量的AgNO3溶液,生成黄色沉淀。则H3PO3与碘水反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1;
③C(s)+O2(g)===CO2(g) ΔH=-393.5kJ·mol-1。
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量_______ (填“>”“<”或“=”)890.3kJ。
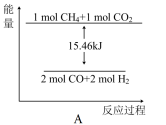
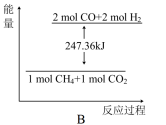
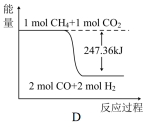
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2===2CO+2H2,1gCH4完全反应可释放15.46kJ的热量,能表示该反应过程中能量变化的是________ (填字母)。

(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)===CH4(g)的反应热无法直接测量,但通过上述反应可求出其反应热ΔH=________ 。
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1;
③C(s)+O2(g)===CO2(g) ΔH=-393.5kJ·mol-1。
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2===2CO+2H2,1gCH4完全反应可释放15.46kJ的热量,能表示该反应过程中能量变化的是




(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)===CH4(g)的反应热无法直接测量,但通过上述反应可求出其反应热ΔH=
您最近一年使用:0次



