某同学用如图所示做水果电池的实验,测得数据如下表所示:
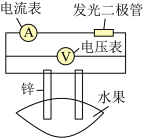
请回答以下问题:
(1)实验⑥中负极的电极反应式为_____________ 。
(2)实验①、⑤中电流方向相反的原因是_________ 。
(3)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做________ (填“合理”或“不合理”)。

实验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
① | 锌 | 铜 | 菠萝 | 3 | 900 |
② | 锌 | 铜 | 苹果 | 3 | 650 |
③ | 锌 | 铜 | 柑橘 | 3 | 850 |
④ | 锌 | 铜 | 西红柿 | 3 | 750 |
⑤ | 锌 | 铜 | 菠萝 | 3 | 650 |
⑥ | 锌 | 铜 | 苹果 | 3 | 450 |
(1)实验⑥中负极的电极反应式为
(2)实验①、⑤中电流方向相反的原因是
(3)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做
更新时间:2020-05-22 19:38:22
|
相似题推荐
【推荐1】氨的合成为氮肥的生产工业奠定了基础,其原理为:N2(g)+3H2(g) ⇋ 2NH3(g)
(1)下表列出了相关化学键的键能,已知H2(g)和N2(g)完全反应生成1mol NH3(g)时放出46kJ的热量,则表中a的数值为___________ ;
(2)在合成氨反应中,一段时间后,NH3的浓度增加了0.9mol/L。用N2表示其反应速率为0.15 mol·L-1·s-1,则所经过的时间为________ ;
(3)在一个绝热、容积不变的密闭容器中发生此可逆反应。下列各项能说明该反应已经达到平衡状态的是_________ 。
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6 mol N—H键
D.反应消耗N2、H2与产生NH3的速率之比1︰3︰2
(4)在一个起始容积为1L的密闭容器内充入1molN2和3molH2进行该反应,保持恒温、恒压,当反应达到平衡时,NH3的体积分数为40 %。则反应达到平衡时,容器的容积为_______ L。
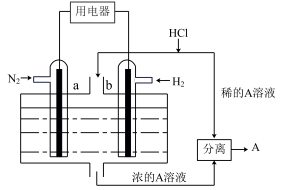
(5)以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如下图所示。b电极为______ 极,A溶液中所含溶质为_____ ,a极电极反应方程式为________ 。
(1)下表列出了相关化学键的键能,已知H2(g)和N2(g)完全反应生成1mol NH3(g)时放出46kJ的热量,则表中a的数值为
| 化学键 | H—H | N—H | N≡N |
| 键能kJ/mol | a | 391 | 946 |
(3)在一个绝热、容积不变的密闭容器中发生此可逆反应。下列各项能说明该反应已经达到平衡状态的是
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6 mol N—H键
D.反应消耗N2、H2与产生NH3的速率之比1︰3︰2
(4)在一个起始容积为1L的密闭容器内充入1molN2和3molH2进行该反应,保持恒温、恒压,当反应达到平衡时,NH3的体积分数为40 %。则反应达到平衡时,容器的容积为
(5)以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如下图所示。b电极为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】如图所示,水槽中的试管内有一枚铁钉,放置数天观察。

(1)铁钉逐渐生锈,铁钉的腐蚀属于___________ (填“化学”或“电化学”)腐蚀。
(2)若试管内液面上升,则发生___________ (填“析氢”或“吸氧”)腐蚀,写出正极电极反应式___________ 。
(3)若试管内液面下降,则发生___________ (填“析氢”或“吸氧”)腐蚀,写出负极电极反应式:___________ 。
(4)若溶液甲为水,溶液乙为海水,则铁钉在溶液___________ (填“甲”或“乙”)中腐蚀的速率快。

(1)铁钉逐渐生锈,铁钉的腐蚀属于
(2)若试管内液面上升,则发生
(3)若试管内液面下降,则发生
(4)若溶液甲为水,溶液乙为海水,则铁钉在溶液
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】现有如下两个反应:
A.
B.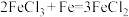
(1)根据两反应本质判断,___________________________ (填“A”或“B”)反应能设计成原电池。
(2)如果不能设计成原电池,原因是______________________________________________________ 。
(3)如果可以设计成原电池,则负极反应为_______________________________________ ,正极反应为_______________________________________ 。
(4)根据(3)中的电极反应,设计一个化学电池(给出若干导线,电极材料和电解质溶液自选)________ 。
要求:①标出电子流动方向;②注明负极电极材料;③写出电解质溶液。
(5)若该电池外电路中有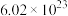 个电子转移,则电解质溶液质量增加了
个电子转移,则电解质溶液质量增加了________________ g。
A.

B.
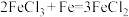
(1)根据两反应本质判断,
(2)如果不能设计成原电池,原因是
(3)如果可以设计成原电池,则负极反应为
(4)根据(3)中的电极反应,设计一个化学电池(给出若干导线,电极材料和电解质溶液自选)
要求:①标出电子流动方向;②注明负极电极材料;③写出电解质溶液。
(5)若该电池外电路中有
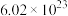 个电子转移,则电解质溶液质量增加了
个电子转移,则电解质溶液质量增加了
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
(1)探究BaCO3和BaSO4之间的转化,实验操作如下:
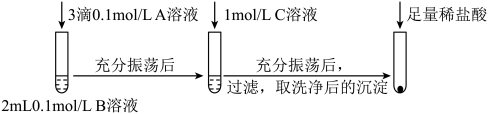
①实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,____ 。
②实验Ⅱ中加入稀盐酸后发生反应的离子方程式是______ 。
③实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______
(2)探究AgCl和AgI之间的转化
实验Ⅲ:

实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
①实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是____ (填序号)。
a AgNO3溶液 b NaCl溶液 c KI溶液
②实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是_______ 。
③结合信息,解释实验Ⅳ中b<a的原因:_______ 。
④实验Ⅳ的现象能说明AgI转化为AgCl,理由是____ 。
| 物质 | BaSO4 | BaCO3 | AgI | AgCl |
| 溶解度/g (20 ℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |

| 试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
| 实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
| 实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
②实验Ⅱ中加入稀盐酸后发生反应的离子方程式是
③实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:
(2)探究AgCl和AgI之间的转化
实验Ⅲ:

实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
| 装置 | 步骤 | 电压表 读数 |
 | ⅰ.如图连接装置并加入试剂,闭合K | a |
| ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | |
| ⅲ.再向B中投入一定量NaCl(s) | c | |
| ⅳ.重复i,再向B中加入与ⅲ等量NaCl(s) | a |
①实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是
a AgNO3溶液 b NaCl溶液 c KI溶液
②实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是
③结合信息,解释实验Ⅳ中b<a的原因:
④实验Ⅳ的现象能说明AgI转化为AgCl,理由是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某化学研究性学习小组针对原电池形成条件,设计了实验方案,进行如下探究。
(1)请填写有关实验现象并得出相关结论。
①通过实验2和3,可得出原电池的形成条件是___________ 。
②通过实验1和3,可得出原电池的形成条件是___________ 。
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是___________ 。
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:___________ 。
Cu棒:___________ 。
(3)实验3的电流是从___________ 棒流出(填“Zn”或“Cu”),反应过程中若有0.4mol电子发生了转移,则Zn电极质量减轻___________ g。
(1)请填写有关实验现象并得出相关结论。
| 编号 | 实验装置 | 实验现象 |
| ① | 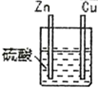 | 锌棒逐渐溶解,表面有气体生成;铜棒表面无现象 |
| ② | 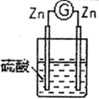 | 两锌棒逐渐溶解,表面均有气体生成;电流计指针不偏转 |
| ③ | 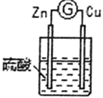 | 铜棒表面的现象是有气体生成,电流计指针发生偏转 |
②通过实验1和3,可得出原电池的形成条件是
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:
Cu棒:
(3)实验3的电流是从
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池,画出装置图并回答
(1)画出装置图_____________ 。
(2)从理论上讲,预期看到的现象是_____________
(3)实验过程中,观察到锌片上有少量气泡冒出,铜片上有大量气泡冒出。试解释:________ 。
(4)此电池的负极是______ ,正极的电极反应式是______________________ 。
(5)该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少3.25 g。请计算理论上导线中共通过了______ mol电子
(1)画出装置图
(2)从理论上讲,预期看到的现象是
(3)实验过程中,观察到锌片上有少量气泡冒出,铜片上有大量气泡冒出。试解释:
(4)此电池的负极是
(5)该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少3.25 g。请计算理论上导线中共通过了
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】某原电池装置如图所示,装置中盐桥的作用是使整个装置形成一个闭合回路,电解质溶液足量,闭合开关,观察到电流计指针发生偏转,回答下列问题。
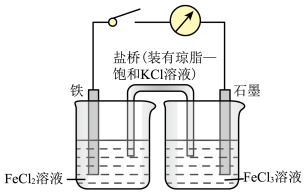
(1)该原电池工作过程中,电池的负极上的电极反应式为___________ ,石墨电极上发生了___________ (填“氧化”或“还原”)反应。
(2)该原电池工作时,下列说法正确的是___________(填标号)。
(3)当铁电极减少 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为___________  ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了___________  。
。
(4)原电池工作时能量转化形式为_______ ,根据原电池形成条件,下列反应理论上可以设计成原电池的是_______ (填标号)。
A. 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应
C. 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应
(5)以 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
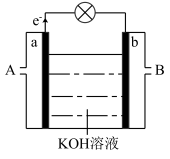
①A处加入的是___________ ,a处的电极反应式是_______ 。
②当消耗标准状况下3.36L 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是___________ mol。

(1)该原电池工作过程中,电池的负极上的电极反应式为
(2)该原电池工作时,下列说法正确的是___________(填标号)。
A.电子移动的方向:石墨 铁 铁 |
B.盐桥中的 会向右侧烧杯移动 会向右侧烧杯移动 |
C. 溶液的颜色会逐渐变浅 溶液的颜色会逐渐变浅 |
D.将 盐桥换成 盐桥换成 盐桥,该装置不能长时间正常工作 盐桥,该装置不能长时间正常工作 |
 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为 ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了 。
。(4)原电池工作时能量转化形式为
A.
 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应C.
 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应(5)以
 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
①A处加入的是
②当消耗标准状况下3.36L
 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】填空。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O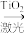 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为_______ 能;分解海水的反应属于_____ 反应(填“放热”或“吸热”)
(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式_______ 。
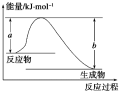
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=_______ kJ∙mol−1,x=________ 。
(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O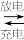 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为_____ 。
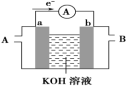
(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为______ 。
(1)已知2H→H2放出437.6kJ的热量,下列说法正确的是___________
| A.氢气分子内每个氢原子都达到稳定结构 |
| B.氢气分子的能量比两个氢原子的能量低 |
| C.1molH2离解成2molH要放出437.6kJ热量 |
| D.氢原子比氢气分子稳定 |
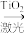 2H2↑+O2↑。分解海水时,实现了光能转化为
2H2↑+O2↑。分解海水时,实现了光能转化为(3)4g硫粉完全燃烧生成二氧化硫气体,放出37kJ热量,热化学方程式
(4)已知键能H-H为436 kJ∙mol−1、O=O为x kJ∙mol−1、O-H为463 kJ∙mol−1。下图示表示反应H2(g)+1/2O2(g)=H2O(g) ΔH=−241.8 kJ∙mol−1,则b=

(5) 高铁电池的总反应为:3Zn+2K2FeO4+8H2O
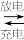 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,则正极反应式为(6)甲烷燃料电池的工作原理示意如图所示,a、b均为惰性电极。a极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.某实验小组同学进行如图1实验,以检验化学反应中的能量变化。请回答下列问题:
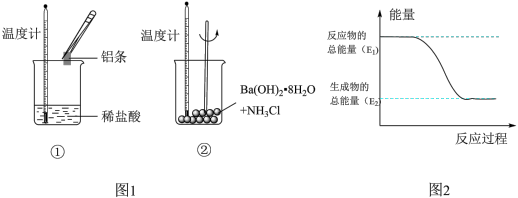
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是________ 热反应。反应过程________ (填“①”或“②”)的能量变化可用图2表示。
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
(2)根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是________ 。
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是________ 。
A. B.
B.
C. D.
D.

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 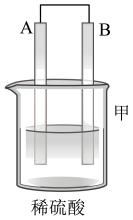 | 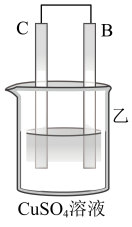 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如下图所示:

(1)写出甲池中负极的电极反应式:_______ 。
(2)写出乙池中总反应的离子方程式_______ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出_____ 活动性更强,而乙会判断出_____ 活动性更强。(填写元素符号)
(4)由此实验,可得到如下哪些正确结论_______ 。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析

(1)写出甲池中负极的电极反应式:
(2)写出乙池中总反应的离子方程式
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)由此实验,可得到如下哪些正确结论
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂,反应受条件的影响较大,因此应具体问题具体分析
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某同学用如图所示做水果电池的实验,测得数据如表所示:
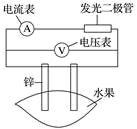
请回答以下问题:
(1)实验⑥中负极的电极反应式为_______ 。
(2)实验①、⑤中电流方向相反的原因是_______ 。
(3)影响水果电池电压的因素有_______ 、_______ 。
(4)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做_______ (填“合理”或“不合理”) 。

| 实验编号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| ① | 锌 | 铜 | 菠萝 | 3 | 900 |
| ② | 锌 | 铜 | 苹果 | 3 | 650 |
| ③ | 锌 | 铜 | 柑橘 | 3 | 850 |
| ④ | 锌 | 铜 | 西红柿 | 3 | 750 |
| ⑤ | 锌 | 铝 | 菠萝 | 3 | 650 |
| ⑥ | 锌 | 铝 | 苹果 | 3 | 450 |
(1)实验⑥中负极的电极反应式为
(2)实验①、⑤中电流方向相反的原因是
(3)影响水果电池电压的因素有
(4)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入 2 mol·L−1的H2SO4溶液中,乙同学将电极放入 6 mol·L−1 的 NaOH 溶液中,如图所示。
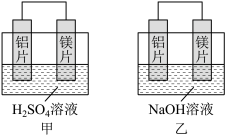
(1)写出甲中正极的电极反应式:_______ 。
(2)装置乙中负极为_______ ,该电极的反应式为_______ ,写出总反应的离子方程式:_______ 。
(3)当装置乙的导线中通过0.3mol电子时,装置乙烧杯中溶液的质量的变化为_______ (填增加或减轻多少g)
(4)由此实验得出的下列结论中,正确的有_______

(1)写出甲中正极的电极反应式:
(2)装置乙中负极为
(3)当装置乙的导线中通过0.3mol电子时,装置乙烧杯中溶液的质量的变化为
(4)由此实验得出的下列结论中,正确的有_______
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
您最近一年使用:0次



