研究表明N2O与CO在Fe+作用下发生可逆反应的能量变化及反应历程如图所示。下列说法不正确的是


| A.反应中Fe+是催化剂,FeO+是中间产物 |
| B.当有14g N2生成时,转移1mol e− |
| C.升高温度,总反应的平衡常数K减小 |
| D.总反应速率由反应②的速率决定 |
更新时间:2020-05-26 14:38:45
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定条件下,硫的某种含氧酸H2SOx(x≤4且为正整数)与H2S可发生如下反应:H2S+H2SOx→S+(x-3)SO2+H2O(未配平),则下列有关推断合理的是
| A.该反应中,一定有SO2生成 |
| B.当x=4时,则每生成1mol S原子,转移的电子为4mol |
| C.若x=3,则还原剂与氧化剂的粒子个数之比为1:1 |
| D.若x=4,若改变条件(如加热),H2S可能被氧化为SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在反应3Cl2+6KOH(浓) KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
 KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为| A.5∶1 | B.4∶1 | C.1∶5 | D.1∶4 |
您最近一年使用:0次
【推荐3】铜是生命必须的元素,也是人类最早使用的金属之一、铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分Cu2S)可以用于制铜,反应方程式为 ,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是

 ,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
,制得的粗铜通过电解法进行精炼。关于用辉铜矿制备粗铜反应的相关说法正确的是
| A.Cu+转化为基态Cu,得到的电子填充在3d轨道上 |
| B.O2和SO2都是非极性分子 |
| C.Cu2S晶胞中S2-位置如图所示,则一个晶胞中含有8个Cu+ |
| D.标准状况下,每有22.4 LO2参与反应,转移电子4 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据图示的能量转化关系判断下列说法正确的是
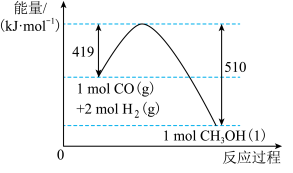

A. 与 与 反应生成32 g 反应生成32 g  吸收91 kJ能量 吸收91 kJ能量 |
| B.形成2 mol H-H和1 mol C≡O(CO)共吸收419 kJ的能量 |
C. 分子中只含有极性共价键 分子中只含有极性共价键 |
D.1 mol  具有的能量高于2 mol 具有的能量高于2 mol  和1 mol 和1 mol  具有的能量 具有的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上,合成氨反应N2+3H2 2NH3的微观历程如图所示。下列说法正确的是
2NH3的微观历程如图所示。下列说法正确的是

 2NH3的微观历程如图所示。下列说法正确的是
2NH3的微观历程如图所示。下列说法正确的是
| A.①→②过程中,催化剂在吸附反应物分子时,破坏了分子中的非极性键 |
| B.②→③是形成N原子和H原子的过程,同时释放能量 |
| C.③→④形成了新的化学键,且是一个放热过程 |
| D.使用合适的催化剂,能提高反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是

 CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
| A.该反应的ΔH<0 |
| B.在500℃条件下达平衡时CO 的转化率为60% |
| C.平衡常数K1(3000C)<K2(5000C) |
| D.图2中达化学平衡的点为c、d、e |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以CO、H2为原料合成甲烷的反应原理为CO(g)+3H2(g) CH4(g)+H2O(g) ∆H,某温度下向体积为2L恒温恒容反应器中加入2 mol CO、8 mol H2进行该反应,c(CH4)与时间的关系如图。下列说法正确的是
CH4(g)+H2O(g) ∆H,某温度下向体积为2L恒温恒容反应器中加入2 mol CO、8 mol H2进行该反应,c(CH4)与时间的关系如图。下列说法正确的是

 CH4(g)+H2O(g) ∆H,某温度下向体积为2L恒温恒容反应器中加入2 mol CO、8 mol H2进行该反应,c(CH4)与时间的关系如图。下列说法正确的是
CH4(g)+H2O(g) ∆H,某温度下向体积为2L恒温恒容反应器中加入2 mol CO、8 mol H2进行该反应,c(CH4)与时间的关系如图。下列说法正确的是
| A.∆H<0 | B.10min时:c(H2)=1.75 mol·L-1 |
| C.前5min:v(H2)=0.1 mol·L-1·min-1 | D.5~10min:正反应速率为0 |
您最近一年使用:0次




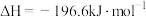 ,能量变化如图所示。下列说法中不正确的是
,能量变化如图所示。下列说法中不正确的是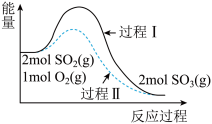
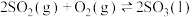 的
的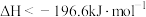
 增大
增大

