现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第_____ ,周期第_____ 族;
(2)元素②⑤⑥⑧的简单离子半径由大到小的顺序是________ ;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的离子方程式为____ ;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的化学方程式_______ 。
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(pm) | 74 | 102 | 152 | 110 | 99 | 186 | 75 | 143 |
| 最高价态 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低价态 | -2 | -2 | -3 | -1 | -3 |
试回答下列问题:
(1)元素③在周期表中的位置是第
(2)元素②⑤⑥⑧的简单离子半径由大到小的顺序是
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的离子方程式为
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的化学方程式
更新时间:2020-06-11 15:09:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.在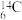 、
、 N、
N、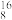 O、
O、 Cl、
Cl、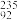 U、
U、 U中:
U中:
(1)___ 和_____ 的质量数相等,但不能互称为同位素。
(2)___ 和____ 的中子数相等,但质子数不相等,所以不是同一种元素。以上所列共有______ 种元素。
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个基本视角。

(3)Y的分子式为________ 。
(4)图中X的电子式为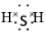 ;其水溶液长期在空气中放置容易变浑浊,原因是
;其水溶液长期在空气中放置容易变浑浊,原因是________ (用化学方程式表示);该变化体现出:S非金属性比O____ (填“强”或“弱”)。用原子结构解释原因:同主族元素从上到下,__________ ,得电子能力逐渐减弱。
(5)Z与图表中某物质反应生成SO2的化学方程式是______________________ 。
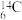 、
、 N、
N、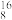 O、
O、 Cl、
Cl、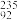 U、
U、 U中:
U中:(1)
(2)
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个基本视角。

(3)Y的分子式为
(4)图中X的电子式为
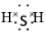 ;其水溶液长期在空气中放置容易变浑浊,原因是
;其水溶液长期在空气中放置容易变浑浊,原因是(5)Z与图表中某物质反应生成SO2的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表列出了A~R九种元素在周期表的位置:
(1)写出R单质分子的电子式___ 。
(2)A、C、D三种元素的氧化物对应的水化物中碱性最强的是__ (填化学式)。
(3)A、B、C三种元素的阳离子按离子半径由大到小的顺序排列为___ 。(用元素的离子符号表示)。
(4)写出A的单质与水反应的化学方程式___ 。
(5)X元素是A~R九种元素中的一种,X的原子核里有14个中子,2.7gX在氧气里燃烧时,质量增加2.4g。X的氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。X的元素符号是___ ,它位于元素周期表中第___ 周期、第___ 族。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
(1)写出R单质分子的电子式
(2)A、C、D三种元素的氧化物对应的水化物中碱性最强的是
(3)A、B、C三种元素的阳离子按离子半径由大到小的顺序排列为
(4)写出A的单质与水反应的化学方程式
(5)X元素是A~R九种元素中的一种,X的原子核里有14个中子,2.7gX在氧气里燃烧时,质量增加2.4g。X的氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。X的元素符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表中的一部分,列出10种元素在周期表中的位置,用化学符号回答下列各题。
(1)10种元素中,化学性质最不活泼的是___________ 。
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物的化学式为___________ 。
(5)①和⑨两元素形成化合物的电子式为___________ :该化合物焰色试验为___________ 色。
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为___________ 。
| 主族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨两元素形成化合物的电子式为
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、B、M、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、M同周期,A、D同主族,A为短周期原子半径最小的元素,M原子最外层电子数为次外层的3倍,A、M常温下能形成两种液态化合物A2M和A2M2,E元素的周期数与主族序数相等。请用化学用语回答下列问题:
(1)B元素在周期表中的位置为_________ ;由A、M、D三种元素组成的化合物中含有的化学键为_________ ;A2M分子的空间结构为_________ ;
(2)用电子式表示D2M的形成过程_________
(3)D、E、M形成的简单离子半径从大到小的顺序为_________ (用离子符号表示)
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2M2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式___________ 。
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放出氢气,且反应后的溶液呈碱性。若将0.1mol的DA和0.1mol的E单质混合后加入足量的水,充分反应后生成的气体在标准状况下的体积是___________ L。
(1)B元素在周期表中的位置为
(2)用电子式表示D2M的形成过程
(3)D、E、M形成的简单离子半径从大到小的顺序为
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2M2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式
(5)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放出氢气,且反应后的溶液呈碱性。若将0.1mol的DA和0.1mol的E单质混合后加入足量的水,充分反应后生成的气体在标准状况下的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素化学性质最不活泼的是______ ,只有负价而无正价的是__________ ,
(2)最高价氧化物的水化物碱性最强的是__________ ,呈两性的是__________ ;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的__________ ;
(4)在B、C、D、E、F、G、H中,原子半径最大的是__________ .
(5)A和E形成化合物的化学式____________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、D、E、F、G、H中,原子半径最大的是
(5)A和E形成化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac(放热反应)。完成下列填空:
[Cu(NH3)3CO]Ac(放热反应)。完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是____ 。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式____ 。
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)____ 。
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为____ 。通过比较____ 可判断氮、磷两种非金属元素的非金属性强弱。
(5)已知CS2与CO2分子结构相似,CS2的结构式是____ 。
 [Cu(NH3)3CO]Ac(放热反应)。完成下列填空:
[Cu(NH3)3CO]Ac(放热反应)。完成下列填空:(1)如果要提高上述反应的反应速率,可以采取的措施是
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为
(5)已知CS2与CO2分子结构相似,CS2的结构式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W在元素周期表中的位置_________________ 。
(2)X与Y可形成一种化合物Y2X4,请写出该化合物的电子式__________ ,工业合成Y的简单氢化物的化学方程式为________________ 。
(3)X和Z组成的既含有极性共价键又含有非极性共价键的化合物的结构式是______________ ;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为______________
(4)写出铜和Y的最高价氧化物的水化物的稀溶液反应的离子方程式______________ 。
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式______________ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(1)W在元素周期表中的位置
(2)X与Y可形成一种化合物Y2X4,请写出该化合物的电子式
(3)X和Z组成的既含有极性共价键又含有非极性共价键的化合物的结构式是
(4)写出铜和Y的最高价氧化物的水化物的稀溶液反应的离子方程式
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)Z元素位于周期表第_____ 周期,第____ 族。Z单质与水反应的离子方程式为_____________ 。
(2)由、X、Y、Z三种元素组成的化合物中,含有的化学键类型有____ (填字母)
A.离子键 B.极性共价键 C.非极性共价键
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是____ (填化学式),此化合物可将碱性工业废水中的CN-氧化为可溶性碳酸盐和氨,相应的离子方程式为_________________ 。
(1)Z元素位于周期表第
(2)由、X、Y、Z三种元素组成的化合物中,含有的化学键类型有
A.离子键 B.极性共价键 C.非极性共价键
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有 X、Y、Z 三种元素:①X、Y、Z 的单质在常温下均为气体,②X 单质可以在 Z 的单质中燃烧,生 成化合物 XZ,火焰呈苍白色,③XZ 极易溶于水,在水溶液中电离处 X+和 Z﹣,其水溶液能使蓝色石蕊试 纸变红,④每两个 X2 分子能与一个 Y2分子化合成两个 X2Y 分子,X2Y 常温下为液体,⑤Z 单质溶于 X2Y 中,所得的溶液具有漂白性。
(1)写出下列微粒的电子式:X+_____ ,Z﹣______ ,Y 原子_____ 。
(2)写出 X2Y 的化学式_____ 。按要求与 X2Y 分子具有相同电子数的微粒的化学符号:两个原子核 的阴离子_____ ,5 个原子核的分子_____ 。
(3)写出 Z 单质溶于 X2Y 中发生反应的离子方程式:_____ ,所得溶液能使淀粉碘 化钾溶液变蓝,主要起作用的微粒是_____ 。
(4)实验室制备 XZ 的化学方程式:_____ ,如何检验 XZ 是否收集满__________ 。
(1)写出下列微粒的电子式:X+
(2)写出 X2Y 的化学式
(3)写出 Z 单质溶于 X2Y 中发生反应的离子方程式:
(4)实验室制备 XZ 的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
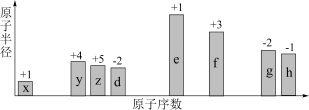
【推荐1】随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同)______ >_______ ;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______ >____ 。
(3)画出x2d2的电子式:____________________ ;
(4)已知1mol e的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:____________________________________________ 。
(5)写出用惰性电极电解eh溶液的化学方程式:________________________________ 。
根据判断出的元素回答问题:
(1)f在元素周期表的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同)
(3)画出x2d2的电子式:
(4)已知1mol e的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
(5)写出用惰性电极电解eh溶液的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】据有关媒体报道,美国华裔科学家叶军领导一个研究小组成功制造出全球最准确的时钟,两亿年误差不足一秒。它是一个锶原子钟,比铯原子喷泉钟准确得多,估计将可大大促进不同的电讯网络的发展,将使全球各地的船只导航变得更为准确。请根据锶、铯在元素周期表中的位置,推断下列内容:
(1)锶元素属于________ (填“金属”或“非金属”)元素,金属性比钙元素________ (填“强”或“弱”),锶原子的核内质子数为________ ,原子核外有________ 个电子层,其原子结构示意图为________ ,其原子半径________ 镁(填“大于”、“小于”或“等于”);铯的原子核外共有________ 层电子,最外层电子数为________ 。
(2)铯与水起剧烈反应,放出________ 色气体,同时使滴有紫色石蕊试液的溶液显________ 色,因为______________________ (写出化学方程式)。
(3)碳酸锶是________ 色粉末,与盐酸反应的离子方程式为__________________________ 。
(1)锶元素属于
(2)铯与水起剧烈反应,放出
(3)碳酸锶是
您最近一年使用:0次



