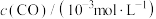N元素的单质及其化合物之间的转化关系:NH3N2NO NO2HNO3。回答下列问题:
(1)N元素在元素周期表中的位置为_______ ;
(2)上述四种气体只能用排水法收集的是_______ (填化学式,下同),只能用排空气法收集的是______ ;
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_____ ;
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为______ ;
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程______ ;
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度_______ (写出解题过程)。
(1)N元素在元素周期表中的位置为
(2)上述四种气体只能用排水法收集的是
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度
更新时间:2020-06-15 13:13:17
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)以下①Cl2②SiO2③Na2O2④(NH4)2SO4四种物质中,可用于自来水消毒的是___________ (填序号,下同),可做化肥的是___________ ,可做供氧剂的是___________ ,可做光导纤维的是___________ 。
(2)现有下列4种物质:①NO、②SO2、③NaHCO3、④FeCl3。其中,溶于水呈碱性的是___________ (填序号,下同);遇空气变红棕色的是___________ ;能使品红溶液褪色是___________ ;能与NaOH溶液反应生成沉淀的是___________ 。
(1)以下①Cl2②SiO2③Na2O2④(NH4)2SO4四种物质中,可用于自来水消毒的是
(2)现有下列4种物质:①NO、②SO2、③NaHCO3、④FeCl3。其中,溶于水呈碱性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的氧化物 是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。
是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。
(1) 能形成酸雨,写出
能形成酸雨,写出 溶于水生成
溶于水生成 的化学方程式:
的化学方程式:__________ 。
(2)NO和 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,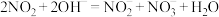 。将NO、
。将NO、 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1∶1.若
物质的量之比接近1∶1.若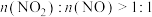 ,则会导致
,则会导致__________ ,若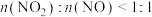 ,则会导致
,则会导致__________ 。
(3)在汽车尾气系统中,安装催化转化器可有效降低 的排放。实验室为了模拟反应
的排放。实验室为了模拟反应 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
①前2s的平均反应速率
____________ ,4s时NO的转化率为__________ 。
②若已知该反应的瞬时速率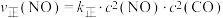 ,其中
,其中 为速率常数,
为速率常数,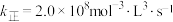 ,当NO的浓度变为原来的
,当NO的浓度变为原来的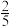 时,
时,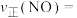
__________ 。
(4)由 、
、 、熔融盐
、熔融盐 组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成氮的最高价氧化物Y。
组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成氮的最高价氧化物Y。
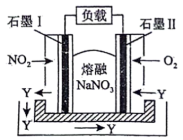
①石墨Ⅱ电极为_____________ (填“正极”或“负极”)。
②写出石墨Ⅰ电极反应式_____________ 。
 是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。
是大气污染物之一,含有氮氧化物的尾气需处理后才能排放。(1)
 能形成酸雨,写出
能形成酸雨,写出 溶于水生成
溶于水生成 的化学方程式:
的化学方程式:(2)NO和
 可用NaOH溶液吸收,主要反应:
可用NaOH溶液吸收,主要反应: ,
,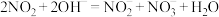 。将NO、
。将NO、 通入石灰乳中可制备重要的工业原料
通入石灰乳中可制备重要的工业原料 。该工艺需控制NO和
。该工艺需控制NO和 物质的量之比接近1∶1.若
物质的量之比接近1∶1.若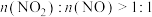 ,则会导致
,则会导致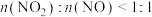 ,则会导致
,则会导致(3)在汽车尾气系统中,安装催化转化器可有效降低
 的排放。实验室为了模拟反应
的排放。实验室为了模拟反应 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 10.00 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

②若已知该反应的瞬时速率
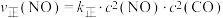 ,其中
,其中 为速率常数,
为速率常数,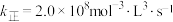 ,当NO的浓度变为原来的
,当NO的浓度变为原来的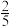 时,
时,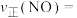
(4)由
 、
、 、熔融盐
、熔融盐 组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成氮的最高价氧化物Y。
组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成氮的最高价氧化物Y。①石墨Ⅱ电极为
②写出石墨Ⅰ电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(一)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
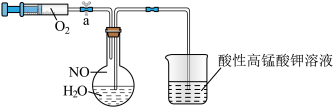
(1)打开止水夹,推动针筒活塞,使氧气进入烧瓶,观察到的现象是______ ,产生此现象的化学方程式为______ 。
(2)关上止水夹,轻轻摇动烧瓶,观察的现象为①______ ;②______ ,产生此现象的化学方程式为____ 。
(3)烧杯中盛放的是酸性高锰酸钾溶液,能吸收尾气,已知NO能与MnO 在酸性条件下反应生成NO
在酸性条件下反应生成NO 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式_____ 。
(二)有关氮循环是近年来科学研究的一个热点,含氮物质有如图转换关系:
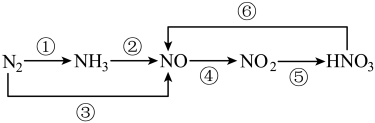
(4)转化⑤中,氧化剂与还原剂的物质的量之比为_____ 。
(5)转化②是工业生成硝酸的关键步骤,写出该转化的化学方程式______ 。

(1)打开止水夹,推动针筒活塞,使氧气进入烧瓶,观察到的现象是
(2)关上止水夹,轻轻摇动烧瓶,观察的现象为①
(3)烧杯中盛放的是酸性高锰酸钾溶液,能吸收尾气,已知NO能与MnO
 在酸性条件下反应生成NO
在酸性条件下反应生成NO 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式(二)有关氮循环是近年来科学研究的一个热点,含氮物质有如图转换关系:

(4)转化⑤中,氧化剂与还原剂的物质的量之比为
(5)转化②是工业生成硝酸的关键步骤,写出该转化的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将盛有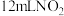 和
和 的混合气体的量筒倒立于水槽中,充分反应后,还剩余
的混合气体的量筒倒立于水槽中,充分反应后,还剩余 无色气体。
无色气体。
(1)若剩余的气体是_______ ,则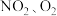 的体积分别是
的体积分别是_______ 。
(2)若剩余的气体是_______ ,则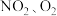 的体积分别是
的体积分别是_______ 。
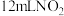 和
和 的混合气体的量筒倒立于水槽中,充分反应后,还剩余
的混合气体的量筒倒立于水槽中,充分反应后,还剩余 无色气体。
无色气体。(1)若剩余的气体是
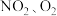 的体积分别是
的体积分别是(2)若剩余的气体是
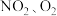 的体积分别是
的体积分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)写出胆矾的化学式:_______
(2)写出乙醛的结构简式:_______
(3)写出二氧化氮溶于水发生反应的化学方程式:_______
(4)写出乙烯与水在一定条件下发生反应的化学方程式:_______
(1)写出胆矾的化学式:
(2)写出乙醛的结构简式:
(3)写出二氧化氮溶于水发生反应的化学方程式:
(4)写出乙烯与水在一定条件下发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)将N2转化为含氮化合物的过程称为固氮
① 人工固氮,将N2→NH3, N2发生_________ 反应
② 自然界固氮,可将少量N2转化为Ca(NO3)2等氮肥,转化途径如下(转化所需试剂及条件已略去):N2→NO→NO2→HNO3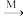 Ca(NO3)2。写出NO→NO2→HNO3的化学方程式
Ca(NO3)2。写出NO→NO2→HNO3的化学方程式__________ 、__________ 。将HNO3转化为Ca(NO3)2,列举三种不同类别 的化合物M_______ (写化学式)。
(2)科学合理地保存、施用氮肥
① NH4HCO3需阴凉处保存,原因是__________ (写化学方程式)。
② 铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式________ 。
(3)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去):

① X可能是______ 、_______ 。 Y是___________ 。
② 尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3则尿素中C元素化合价为__________ 。
(1)将N2转化为含氮化合物的过程称为固氮
① 人工固氮,将N2→NH3, N2发生
② 自然界固氮,可将少量N2转化为Ca(NO3)2等氮肥,转化途径如下(转化所需试剂及条件已略去):N2→NO→NO2→HNO3
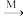 Ca(NO3)2。写出NO→NO2→HNO3的化学方程式
Ca(NO3)2。写出NO→NO2→HNO3的化学方程式(2)科学合理地保存、施用氮肥
① NH4HCO3需阴凉处保存,原因是
② 铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式
(3)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去):

① X可能是
② 尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3则尿素中C元素化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素的单质和常见的化合物在工、农业生产中用途广泛。NH3、NH3·H2O、NH4Cl、HNO3是最常见的含氮化合物。
(1)氮气常用作食品袋中填充气和某些场合下的保护气,与此相关的氮气的性质是______ 。
(2)上述4种含氮化合物中,属于盐的是_________ ,属于碱的是___________ 。
(3)NH3常用作制冷剂,其在空气中与HCl相遇产生白烟,这里“白烟”是_________ ,打开盛浓硝酸的试剂瓶塞,瓶口有白雾出现,这里“白雾”是___________ 。
(4)Fe粉与稀硝酸反应生成硝酸铁的化学方程式为________________________ 。该反应中硝酸表现出的化学性质主要有_____________________ 。
(1)氮气常用作食品袋中填充气和某些场合下的保护气,与此相关的氮气的性质是
(2)上述4种含氮化合物中,属于盐的是
(3)NH3常用作制冷剂,其在空气中与HCl相遇产生白烟,这里“白烟”是
(4)Fe粉与稀硝酸反应生成硝酸铁的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学是一门以实验为基础的自然科学。根据题意回答下列问题:
(1)在 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到___________ (填“蓝色”或“红色”)的沉淀。
(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体___________ (填化学式),能漂白___________ (填“蓝色”或“红色”)品红溶液。
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为___________ ;铜和稀硝酸反应缓慢,化学方程式为___________ ;对比现象可以说明浓硝酸的氧化性比稀硝酸___________ (填“强”或“弱”)。
(1)在
 溶液中逐滴滴入
溶液中逐滴滴入 溶液,观察到
溶液,观察到(2)铜和浓硫酸在加热时反应,产生无色刺激性气味的气体
(3)铜和浓硝酸反应剧烈,产生红棕色气体,离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】
(1)由CO、CO2组成的混合气体36g,其中含C原子数为NA个,则C、O原子个数比为_______ ;用过氧化钠吸收CO2制氧气的化学方程式是___________________________ ;
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①当酸足量时,“三酸”与“两碱”之间共可发生六个化学反应,用两个离子方程式即可表达这六个反应的本质,这两个离子方程式是:____________ 、____________ 。
②“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是________ 。
A.Fe B.Cu C.Al D.Pt
(3)第三周期元素中,离子半径最小的离子是____ (写符号),得电子能力最强的原子是___ (写符号)。
(1)由CO、CO2组成的混合气体36g,其中含C原子数为NA个,则C、O原子个数比为
(2)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①当酸足量时,“三酸”与“两碱”之间共可发生六个化学反应,用两个离子方程式即可表达这六个反应的本质,这两个离子方程式是:
②“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是
A.Fe B.Cu C.Al D.Pt
(3)第三周期元素中,离子半径最小的离子是
您最近一年使用:0次