I.由三种元素组成的化合物A,式量在200- -300之间。在一 定条件下A能发生如下图的转化,其中B的焰色反应为紫色(透过蓝色钴玻璃),C是不溶于酸的白色沉淀。
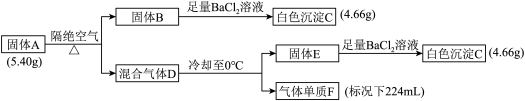
请回答∶
(1) C的化学式是______ ,组成A的三种元素是________ 。
(2) A加热分解的化学方程式是_____ 。
(3) E可以和SCl2反应生成一种常用于有机合成的物质SOCl2和另一种常见气体,反应的化学方程式是________ 。
II.实验室测定某铁铝合金中的铝含量,利用如图装置和试剂完成。
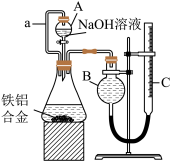
请回答∶
(1)下列有关该实验的说法中正确的是_______ 。
A.由于恒压分液漏斗的存在,该装置不能进行气密性检查
B.读数前需将量气管C上下移动使B、C中的液面相平
C.反应完成后生成的氢气都要转移至装置B中
D.需要控制NaOH的量以防止产生气体过多超过量气装置的量程
(2)若将恒压分液漏斗(A) 去掉导管a,改成普通分液漏斗,则测得铁铝合金中的铝含量______ ,(填“偏大”、“偏小”或“不变”),请说明理由_____ 。

请回答∶
(1) C的化学式是
(2) A加热分解的化学方程式是
(3) E可以和SCl2反应生成一种常用于有机合成的物质SOCl2和另一种常见气体,反应的化学方程式是
II.实验室测定某铁铝合金中的铝含量,利用如图装置和试剂完成。

请回答∶
(1)下列有关该实验的说法中正确的是
A.由于恒压分液漏斗的存在,该装置不能进行气密性检查
B.读数前需将量气管C上下移动使B、C中的液面相平
C.反应完成后生成的氢气都要转移至装置B中
D.需要控制NaOH的量以防止产生气体过多超过量气装置的量程
(2)若将恒压分液漏斗(A) 去掉导管a,改成普通分液漏斗,则测得铁铝合金中的铝含量
更新时间:2020-06-18 16:35:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~L物质存在如下转化关系(反应条件已略去),已知通常情况下A、J为金属单质,C为厨房中常见的调味品,B、D、H为气体单质,E为淡黄色固体,F为最常见的无色液体,J单质由地壳中含量最高的金属元素组成。

请回答下列问题:
(1)写出下列物质的化学式:E_______ ;J_______ 。
(2)写出纯净的H在盛有B的集气瓶中燃烧的实验现象:_______ 。
(3)①写出E与F反应的离子方程式:_______ 。②写出过量G与K反应的离子方程式:_______ 。
(4)下列关于A的叙述中正确的是_______(填序号)。

请回答下列问题:
(1)写出下列物质的化学式:E
(2)写出纯净的H在盛有B的集气瓶中燃烧的实验现象:
(3)①写出E与F反应的离子方程式:
(4)下列关于A的叙述中正确的是_______(填序号)。
| A.自然界中没有游离态的A | B.A与D的反应在常温下无法进行 |
| C.少量A可以保存在冷水里 | D.A着火时应用细沙盖灭 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,回答有关问题。
(1)在元素①~⑧中,金属性最强的元素的离子结构示意图是_______ 。
(2)前三周期所有元素中,原子最外层电子数是元素所处周期数2倍的元素有_______ 种。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为_______ 。
(4)在②、③、④这些元素形成的最简单离子中,离子半径由大到小的顺序为_______ (填离子符号)。
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)⑥、⑦和⑧三种元素的最低价气态氢化物的热稳定性由弱到强的依次为_______ (填化学式)。
(7)写出元素⑤的单质与元素③最高价氧化物的水化物反应的离子方程式_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)前三周期所有元素中,原子最外层电子数是元素所处周期数2倍的元素有
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为
(4)在②、③、④这些元素形成的最简单离子中,离子半径由大到小的顺序为
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有
(6)⑥、⑦和⑧三种元素的最低价气态氢化物的热稳定性由弱到强的依次为
(7)写出元素⑤的单质与元素③最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】I.A,B,C,D是中学化学的常见物质。已知:①A为黄绿色气体,B为金属单质;②A与B化合生成C,C的水溶液遇KSCN溶液呈红色;③D是第三周期的金属单质,能与盐酸、氢氧化钠溶液反应产生氢气,请回答:
(1)C的化学式为___________ ;
(2)写出D与氢氧化钠溶液反应的化学方程式是___________ ;
(3)B与C的水溶液反应的离子方程式为___________ 。
(4)A可用于制取漂白粉,漂白粉的有效成分是___________ (填化学式)。
Ⅱ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
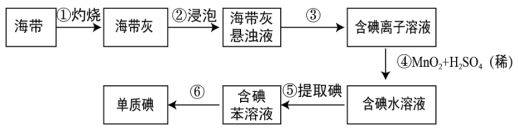
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___________ (从下列仪器中选出所需的仪器,用标号字母填写在空自处)。
A.烧杯B.坩埚C.表面皿D.泥三角E.酒精灯F.干燥器
(2)步骤③的实验操作名称是___________ 。
(3)步骤④中还可以用 ,请写出
,请写出 氧化
氧化 的离子方程式:
的离子方程式:___________ 。
(4)检验水溶液中是否含有单质碘可以用___________ 溶液。
(1)C的化学式为
(2)写出D与氢氧化钠溶液反应的化学方程式是
(3)B与C的水溶液反应的离子方程式为
(4)A可用于制取漂白粉,漂白粉的有效成分是
Ⅱ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯B.坩埚C.表面皿D.泥三角E.酒精灯F.干燥器
(2)步骤③的实验操作名称是
(3)步骤④中还可以用
 ,请写出
,请写出 氧化
氧化 的离子方程式:
的离子方程式:(4)检验水溶液中是否含有单质碘可以用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】镍矾(NiSO4·7H2O)常用于电镀、镍电池、催化剂以及制取其他镍盐等。以镍废渣(主要成分为Ni,含少量Fe、Al、Fe3O4、Al2O3和不溶性杂质等)为原料合成镍矾的流程如下:

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
回答下列问题:
(1)"碱浸"的目的是___________ ;为提高"酸浸"浸出率,可采取的措施有___________ (任写两条)。
(2)"转化"过程中加入H2O2的目的是___________ (用离子方程式表示);Fe2+的转化率随温度的变化如图,温度高于40℃,Fe2+转化率急速降低的原因可能是___________ 。

(3)"除铁"过程需要调节pH至a,a的取值范围是___________ ;从化学平衡移动角度解释加入氧化镍除去铁元素的原理___________ 。
(4)准确称取ω g镍矾产品配成250mL溶液,取20.00mL所配溶液于锥形瓶中,用c mol·L-1EDTA(Na2H2Y)标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+,不考虑杂质反应),三次实验消耗标准溶液的体积分别为20.02mL、19.98mL、19.40mL,则镍矾的纯度为___________ (只列计算式)。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| A13+ | 3.0 | 4.7 |
| Fe2+ | 7.0 | 9.0 |
| Ni2+ | 7.1 | 9.2 |
(1)"碱浸"的目的是
(2)"转化"过程中加入H2O2的目的是

(3)"除铁"过程需要调节pH至a,a的取值范围是
(4)准确称取ω g镍矾产品配成250mL溶液,取20.00mL所配溶液于锥形瓶中,用c mol·L-1EDTA(Na2H2Y)标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+,不考虑杂质反应),三次实验消耗标准溶液的体积分别为20.02mL、19.98mL、19.40mL,则镍矾的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组用SiCl4和(CH3CO)2O合成四乙酸硅,装置如图所示(夹持装置略),相关物质的性质如表所示:
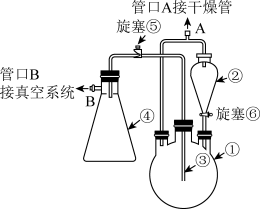
回答下列问题:
(1)仪器①的名称是____ ,管口A所接干燥管中盛装的试剂是____ (填“P2O5”、“CaCl2”或“碱石灰”)。
(2)检查上述装置气密性,具体操作为先向②中注入一定量的____ (填“水”或“苯”),然后密封管口A和B,打开旋塞⑥,若____ (填现象),则证明装置的气密性良好。
(3)取255gSiCl4放入1L仪器①中,关闭旋塞⑥,再由分液漏斗滴入稍过量的乙酸酐,反应发生,放出大量的热,混合物略微带色,不久仪器①底部析出大颗粒晶体。写出制备四乙酸硅的化学方程式:____ ,该过程中,玻璃管③的管口必须保持在液面上方的原因是____ 。
(4)待放置一段时间,用干冰—丙酮冷冻剂冷却,然后____ (填具体操作),小心缓慢地除去仪器①中的残留液体,接着再分两次由分液漏斗各滴入75mL左右的乙酸酐,再缓慢除去,最后得到335g精制的四乙酸硅,则四乙酸硅的产率为____ %(保留到小数点后一位)。

| 物质 | 性质 |
| SiCl4 | 无色油状液体,能剧烈水解生成硅酸和HCl |
| 乙酸酐[(CH3CO)2O] | 无色油状液体,吸湿性很强 |
| 四乙酸硅[Si(CH3COO)4] | 米黄色晶体,可溶于苯,遇水会迅速水解,超过160℃时可分解成乙酸酐和二氧化硅 |
| 乙酰氯(CH3COCl) | 无色油状液体,遇水剧烈反应 |
(1)仪器①的名称是
(2)检查上述装置气密性,具体操作为先向②中注入一定量的
(3)取255gSiCl4放入1L仪器①中,关闭旋塞⑥,再由分液漏斗滴入稍过量的乙酸酐,反应发生,放出大量的热,混合物略微带色,不久仪器①底部析出大颗粒晶体。写出制备四乙酸硅的化学方程式:
(4)待放置一段时间,用干冰—丙酮冷冻剂冷却,然后
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】I.金属互化物A (仅含二种常见短周期的金属元素),A中某元素的单质可用于制造信号弹,某研究小组为了探究金属互化物A的组成和性质,设计并完成了如下实验。

回答下列问题:
(1)金属互化物A的化学式是_______ 。
(2)写出金属互化物A与过量NaOH溶液反应的化学方程式_______ 。
(3)写出溶液C与过量CO2反应的离子方程式_______ 。
II.现用如图装置来制定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为500 mL,供选择的电极材料有纯铜片和纯锌片,请回答下列问题:
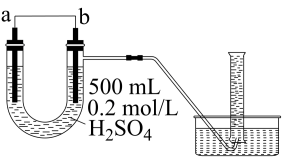
(1)b电极反应式为_______ 。
(2)当量筒中收集到336 mL(标准状况下)气体时,通过导线的电子的物质的量为_______ mol。

回答下列问题:
(1)金属互化物A的化学式是
(2)写出金属互化物A与过量NaOH溶液反应的化学方程式
(3)写出溶液C与过量CO2反应的离子方程式
II.现用如图装置来制定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为500 mL,供选择的电极材料有纯铜片和纯锌片,请回答下列问题:

(1)b电极反应式为
(2)当量筒中收集到336 mL(标准状况下)气体时,通过导线的电子的物质的量为
您最近一年使用:0次



