下表为10种元素在元素周期表中的位置,请回答有关问题:
(1)表中最活泼的金属是___ (填元素符号,下同),非金属性最强的元素是_____ 。
(2)表中能形成两性氢氧化物的元素是____ ,写出该元素的氢氧化物与⑨最高价氧化物对应的水化物反应的化学方程式____ 。
(3)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱_____ 。
| ⅠA | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氢氧化物的元素是
(3)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱
更新时间:2020-07-12 11:40:20
|
相似题推荐
【推荐1】银铜合金广泛用于航空工业,从切割废料中回收银并制备铜化工产品的工艺如图:
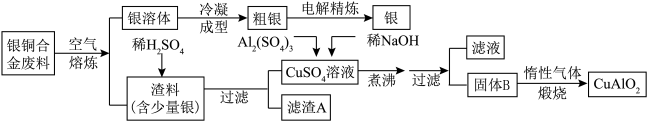
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为_____________ 。
(2)固体混合物B的组成为_________ ;在生成固体B的过程中,需控制NaOH的加入量。若NaOH过量,则因过量引起的反应的离子方程式_____________________ 。
(3)完成煅烧过程中一个反应的化学方程式:____ CuO+____ Al2O3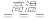
____ CuAlO2+____ 。
(4)若银铜合金中铜的质量分数为64%,理论上5.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液________ L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是________ 、冷却结晶、过滤、洗涤和干燥。

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为
(2)固体混合物B的组成为
(3)完成煅烧过程中一个反应的化学方程式:
(4)若银铜合金中铜的质量分数为64%,理论上5.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液
(5)CuSO4溶液也可用于制备胆矾,其基本操作是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,注:部分反应条件和产物省略 ,回答下题。
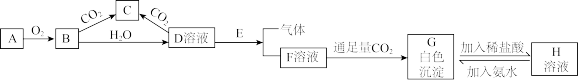
(1)实验室中 常常保存在盛放
常常保存在盛放_______ 的广口瓶, 焰色反应为
焰色反应为_______ 色。
(2)写出 转变成
转变成 的化学方程式
的化学方程式_______ 。该反应中氧化剂是_______ ,还原剂是_______ ,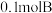 参与该反应,转移电子的个数为
参与该反应,转移电子的个数为_______ 。
(3)写出D溶液与E反应生成F和气体的化学方程式:_______ 。
(4)F→G的离子方程式_______ 。
(5)H→G的离子方程式_______ 。

(1)实验室中
 常常保存在盛放
常常保存在盛放 焰色反应为
焰色反应为(2)写出
 转变成
转变成 的化学方程式
的化学方程式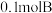 参与该反应,转移电子的个数为
参与该反应,转移电子的个数为(3)写出D溶液与E反应生成F和气体的化学方程式:
(4)F→G的离子方程式
(5)H→G的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题:
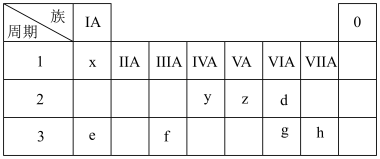
(1)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >_______ ;
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >_______ 。
(3)用电子式表示e、g组成的简单化合物的形成过程:_______ 。
(4)下列说法不正确的是_______。
(5)由表中两种元素的原子按 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)_______ 。
(6)上述元素可组成盐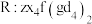 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
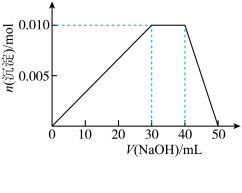
若向上述 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为_______  。
。

(1)比较d、e常见离子的半径大小(用化学式表示,下同):
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:
(3)用电子式表示e、g组成的简单化合物的形成过程:
(4)下列说法不正确的是_______。
A.最简单的氢化物的稳定性 |
B.最高价氧化物对应的水化物的碱性 |
| C.与y元素同主族的第四周期元素的单质是半导体材料 |
| D.y、h两元素组成的化合物中一定只含共价键 |
(5)由表中两种元素的原子按
 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)(6)上述元素可组成盐
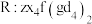 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
若向上述
 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,请参照元素①—⑨在表中的位置,回答下列问题:
(1)第三周期中元素非金属性最强的元素的原子结构示意图为___________ 。
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)___________
(3)下列可以判断⑤和⑥金属性强弱的是___________ 。
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式___________ 。用⑥与赤铁矿冶炼金属铁的化学方程式___________ 。
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
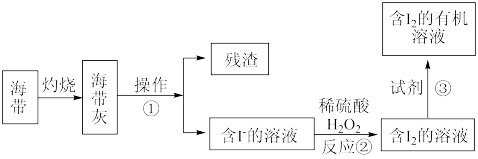
操作①的名称是___________ ;反应②的离子方程式是___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)
(3)下列可以判断⑤和⑥金属性强弱的是
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

操作①的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】NiS难溶于水,易溶于稀酸,可利用沉淀转化的原理除去镍电解液中的铜离子,NiS在潮湿的空气中可转化为磁式硫化高镍 ,从而降低除铜离子能力、实验室模拟制取NiS装置如图(加热、夹持装置略去),先通氮气排尽装置内空气后,同时通入硫化氢气体和氨气,制得NiS沉淀,回答下列问题:
,从而降低除铜离子能力、实验室模拟制取NiS装置如图(加热、夹持装置略去),先通氮气排尽装置内空气后,同时通入硫化氢气体和氨气,制得NiS沉淀,回答下列问题:______ 。
(2)装置图中,仪器a的名称为______ ,装置Ⅱ中的试剂为______ 。
(3)装置Ⅲ中反应的离子方程式为中。
(4)反应结束后关闭 、
、 ,在b、c处分别连接下图两个装置,打开
,在b、c处分别连接下图两个装置,打开 、
、 进行抽滤和洗涤。装置Ⅳ接在
进行抽滤和洗涤。装置Ⅳ接在______ (填“b”或“c”)处。______ (用化学方程式结合文字作答)。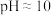 的氨性缓冲溶液5mL,紫脲酸铵指示剂少许,用
的氨性缓冲溶液5mL,紫脲酸铵指示剂少许,用
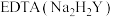 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。滴定达终点时消耗EDTA标准溶液VmL。
。滴定达终点时消耗EDTA标准溶液VmL。
①样品的纯度为______ %。
②滴定过程中,若氨性缓冲溶液pH过低,导致测得的产品纯度______ (填“偏低”、“偏高”或“不影响”)。
 ,从而降低除铜离子能力、实验室模拟制取NiS装置如图(加热、夹持装置略去),先通氮气排尽装置内空气后,同时通入硫化氢气体和氨气,制得NiS沉淀,回答下列问题:
,从而降低除铜离子能力、实验室模拟制取NiS装置如图(加热、夹持装置略去),先通氮气排尽装置内空气后,同时通入硫化氢气体和氨气,制得NiS沉淀,回答下列问题:
(2)装置图中,仪器a的名称为
(3)装置Ⅲ中反应的离子方程式为中。
(4)反应结束后关闭
 、
、 ,在b、c处分别连接下图两个装置,打开
,在b、c处分别连接下图两个装置,打开 、
、 进行抽滤和洗涤。装置Ⅳ接在
进行抽滤和洗涤。装置Ⅳ接在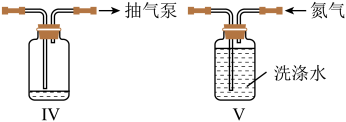

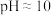 的氨性缓冲溶液5mL,紫脲酸铵指示剂少许,用
的氨性缓冲溶液5mL,紫脲酸铵指示剂少许,用
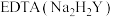 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。滴定达终点时消耗EDTA标准溶液VmL。
。滴定达终点时消耗EDTA标准溶液VmL。①样品的纯度为
②滴定过程中,若氨性缓冲溶液pH过低,导致测得的产品纯度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如图为元素周期表的一部分,参照元素①~⑩在表中的位置,回答下列问题:
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置______ 。
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为______ 。
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)______ 。
(4)写出②的单质在足量④的单质中燃烧产物的电子式______ 。用电子式表示⑤和⑩组成简单化合物的形成过程______ 。
(5)④和⑨的单质均能与 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性______ (填化学式)。
(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为______ (填字母)。
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式______ 。
ⅲ.Z→N的化学方程式______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为
(3)③⑦⑧最高价氧化物对应水化物酸性由强到弱的顺序为(填化学式)
(4)写出②的单质在足量④的单质中燃烧产物的电子式
(5)④和⑨的单质均能与
 反应生成
反应生成 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性(6)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:

i.M中所含的化学键种类为
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.生成Z和M的离子方程式
ⅲ.Z→N的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】C、O、Na、Al、Si、S、Cl是常见的几种元素。请回答下列问题:
(1)C元素的一种同位素可以测定文物年代,这种同位素的符号为_______ 。
(2)用“大于”、“小于”或“等于”填空。
(3)在C、O、Si、S、Cl元素形成的简单氢化物中,稳定性最差的简单氢化物的电子式为_______ 。
(4)利用如图所示装置可验证同主族元素非金属性的变化规律。

①仪器A的名称为_______ ,干燥管D的作用是_______ 。
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下可反应生成Cl2,该反应的化学方程式为_______ ,C中加淀粉KI混合溶液,观察到C中溶液_______ (填现象),即可证明,该反应的离子方程式为_______ 。从环境保护的角度考虑,此装置缺少尾气处理装置,请描述你的改进措施_______ 。
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,有同学认为观察到C中溶液中出现白色沉淀,即可证明。你是否同意该同学的观点,_______ (填“同意”或“不同意”,若“同意”下一问不必作答,或“不同意”请在后面的横线上说明理由)_______ 。
(1)C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”、“小于”或“等于”填空。
| ①离子半径 | ②酸性 | ③得电子能力 |
| O2- | H2SO4 | 35Cl |
(4)利用如图所示装置可验证同主族元素非金属性的变化规律。

①仪器A的名称为
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,KMnO4与浓盐酸常温下可反应生成Cl2,该反应的化学方程式为
③若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,有同学认为观察到C中溶液中出现白色沉淀,即可证明。你是否同意该同学的观点,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组利用如图1实验装置进行制取氯酸钾和验证元素的非金属性相对强弱的实验。已知氯气在加热条件下与氢氧化钾反应生成氯酸钾、水和氯化钾。
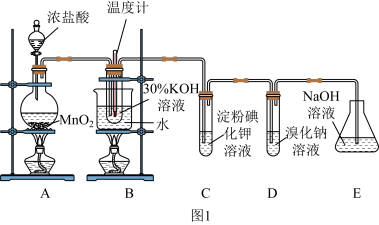
(1)A装置中反应的离子方程式为_______ ,B装置中反应的离子方程式为_______ ,B装置采用水浴加热的优点是_______ 。
(2)若对调B和C装置的位置,_____ (填“能”或“不能”)提高B中氯酸钾的产率。
(3)验证非金属性:Cl>I的实验现象是_______ ,该装置______ (填“能”或“不能”)验证非金属性:Cl>Br>I。
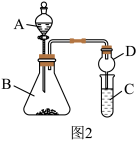
(4)利用如图2装置验证非金属性:C>Si,B中加Na2CO3,C中加Na2SiO3溶液,A中应该加入_____ ,C中反应的化学方程式:_____ ,D装置的作用是______ 。

(1)A装置中反应的离子方程式为
(2)若对调B和C装置的位置,
(3)验证非金属性:Cl>I的实验现象是
(4)利用如图2装置验证非金属性:C>Si,B中加Na2CO3,C中加Na2SiO3溶液,A中应该加入

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、R、W为五种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题。
(1)Y元素的名称为_______ ,在周期表中位于第三周期_______ 族。
(2)W与Z单质化合得到的物质属于_______ (选填“离子”或“共价”)化合物,向其溶液中加入足量NaOH溶液,反应的离子方程式为_______ 。
(3)工业上常用W单质与氨气在1700 ℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式_______ 。
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式_______ 。
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是_______ (填字母序号)。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易程度
c.比较这两种元素的气态氢化物的稳定性
(1)Y元素的名称为
(2)W与Z单质化合得到的物质属于
(3)工业上常用W单质与氨气在1700 ℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易程度
c.比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次



