A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,B与C的单质在加热条件下反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和
(1)写元素符号:A为______ ,C为______ ,D的最高价氧化物的水化物化学式是______ 。
(2)写出A、B形成的化合物与E反应的化学方程式:______
(3)E属于______ (“离子”或“共价”)化合物。
(4)C与D两元素可形成化合物______ 。
(1)写元素符号:A为
(2)写出A、B形成的化合物与E反应的化学方程式:
(3)E属于
(4)C与D两元素可形成化合物
11-12高一下·浙江温州·阶段练习 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。
请根据以上情况,回答下列问题:
(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_______ 。
(2)B的氢化物分子的立体构型是_______ 。其中心原子采取_______ 杂化。
(3)E的核外电子排布式是_______ ,ECl3形成的配合物的化学式_______ 。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是_______ 。
(5)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),碱式硫酸铜中非金属元素电负性由大到小的顺序是_______ ,SO 的空间构型为
的空间构型为_______ 。
(6)氨缩脲(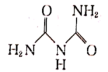 )分子中氮原子的杂化类型为
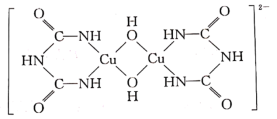
)分子中氮原子的杂化类型为_______ ,σ 键与π键的数目之比为_______ 。氨缩脲与胆矾溶液反应得到如图所示的紫色物质,1 mol紫色物质中含配位键的数目为_______ 。
请根据以上情况,回答下列问题:
(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物分子的立体构型是
(3)E的核外电子排布式是
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
(5)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),碱式硫酸铜中非金属元素电负性由大到小的顺序是
 的空间构型为
的空间构型为(6)氨缩脲(
 )分子中氮原子的杂化类型为
)分子中氮原子的杂化类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表列出了元素周期表中6种短周期元素的有关数据。
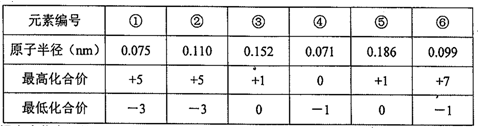
根据表中信息回答下列问题(均使用化学用语填空):
(1)写出下列编号对应元素的符号:②______ ,③________ 。
(2)表中元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应
生成的盐的化学式为______________________ 。
(3)请写出①、②、④三种元素的简单氢化物的稳定性由强到弱的顺序______________ 。
(4)元素⑥所在的主族中,氢化物的还原性最强的是______________ 。(放射性元素除外)

根据表中信息回答下列问题(均使用化学用语填空):
(1)写出下列编号对应元素的符号:②
(2)表中元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应
生成的盐的化学式为
(3)请写出①、②、④三种元素的简单氢化物的稳定性由强到弱的顺序
(4)元素⑥所在的主族中,氢化物的还原性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D四种核电荷数小于20的元素,A原子最外层电子数是次外层的2倍;B原子核外K层比M层电子数多1;C原子最外层电子数是其电子层数的3倍;D能形成D2-,D2-的M层为最外层。试回答下列问题:
(1)写出A、B、C、D 四种元素的元素符号:A______ 、B______ 、C______ 、D______ .
(2)写出A、B、C、D 四种元素中的任意3种元素所能形成的常见化合物的化学式______ 、______ 、______ 。
(1)写出A、B、C、D 四种元素的元素符号:A
(2)写出A、B、C、D 四种元素中的任意3种元素所能形成的常见化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】Q、W、X、Y、Z为短周期元素,Q是原子半径最小的元素,W是地壳中含量最高的元素,X原子的质子数等于Z与Y的质子数之和: Z与Y位于同一周期, Y原子核外最外层电子比次外层多3个电子,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y、 Z的元素名称分别为_______ 、_______
(2)X在周期表中的位置是_______ ,其离子结构示意图为_______
(3)W元素有多种核素,请写出中子数为10的W元素的一种核素符号_______
(4)X、Y、Z三种元素原子半径由大到小的顺序为_______ (填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,写出X单质与氢氧化钠溶液反应的化学方程式 _______
(5)Y和W两种元素形成的最简单的氢化物中,更稳定的是_______ (用化学式表示)
(1)Y、 Z的元素名称分别为
(2)X在周期表中的位置是
(3)W元素有多种核素,请写出中子数为10的W元素的一种核素符号
(4)X、Y、Z三种元素原子半径由大到小的顺序为
(5)Y和W两种元素形成的最简单的氢化物中,更稳定的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下表中几种短周期元素的原子半径及主要化合价,回答下列问题:
(1)元素D组成的常见单质有两种,分别是_______ 、________ (写名称)。
(2)用电子式表示IE2的形成过程:_________________________ 。
(3)A、H、J的离子半径由大到小顺序是_________ (用离子符号表示)。
(4)78 g J2B2与足量的水反应生成_______ L(标准状况下)气体。
(5)元素E的单质与水反应的离子方程式为_______________ 。
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径 | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
(2)用电子式表示IE2的形成过程:
(3)A、H、J的离子半径由大到小顺序是
(4)78 g J2B2与足量的水反应生成
(5)元素E的单质与水反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】a、b、c、d为四种由短周期元素构成的中性微粒,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是常见单原子微粒,a单质可用作半导体材料,a原子核外电子排布式为______ 。M层上的能级能量大小关系为_________ ,3p能级上的电子应满足_______ 。
(2)b是两原子化合物,常温下为无色无味气体。b的化学式为________ 。人一旦吸入b气体后,就易引起中毒,是因为________ 而中毒。
(3)c是两原子单质,写出其电子式___________ 。c分子中所含共价键的类型为_______ (填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是____ 。
(4)d是四原子有机化合物,其结构式为______________ ;d分子内所含共价键有________ 个σ键,________ 个π键;σ键与π键的强度大小关系为σ___ π(填“>”、“<”或“=”),原因是:_______ 。
(1)a是常见单原子微粒,a单质可用作半导体材料,a原子核外电子排布式为
(2)b是两原子化合物,常温下为无色无味气体。b的化学式为
(3)c是两原子单质,写出其电子式
(4)d是四原子有机化合物,其结构式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D、E五种短周期元素,其元素特征信息如下表。
回答下列问题。
(1)写出下列元素的名称:C_______ ,E_______ 。
(2)写出A、B、C形成的化合物的化学式_______ 。
(3)B、C、D的简单离子半径由大到小的顺序是_______ (用化学式表示)。
(4)①写出E单质与A、B、C形成的化合物反应的化学方程式:_______ 。
②写出D单质与A、B、C形成的化合物的水溶液反应的离子方程式:_______ 。
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B 可以形成两种氧化物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期中最小 |
(1)写出下列元素的名称:C
(2)写出A、B、C形成的化合物的化学式
(3)B、C、D的简单离子半径由大到小的顺序是
(4)①写出E单质与A、B、C形成的化合物反应的化学方程式:
②写出D单质与A、B、C形成的化合物的水溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素W、X、Y、Z、M、N、Q原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,X与M同主族,Z与N同主族,Z2-电子层结构与氖原子相同。
(1)M在元素周期表中的位置是______ 。
(2)化合物p由W、X、Y、N四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热,可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为______ 。
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为______ 。
(4)(XY)2的性质与单质Q2相似,(XY)2与NaOH溶液常温下反应的离子方程式为______ 。
(5)常温下,1 mol Z3能与Y的最简单氢化物反应,生成一种常见的含氧酸盐和1 mol Z2,该反应的化学方程式为______ 。
(6)Z元素与除M外的其余五种元素间两两形成的化合物都不止一种,写出符合下列条件的化合物分子式_____
①Z与其它原子的个数比为2:1;
②分子中电子总数为奇数
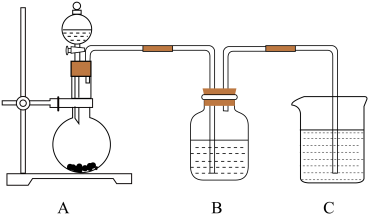
(7)用如图的装置,既可设计比较X、M、N非金属性强弱的实验,也可设计比较N、Q非金属性强弱的实验。若用强酸制弱酸的原理比较X、M、N非金属性强弱,则A装置中发生反应的化学方程式是_______ ;若用氧化还原反应原理比较N、Q非金属性强弱,则B装置中发生反应的离子方程式是________ (此空供选用的实验试剂有:KMnO4固体、MnO2固体、稀盐酸、浓盐酸、Na2S溶液、Na2SO3溶液、NaOH溶液)。
(1)M在元素周期表中的位置是
(2)化合物p由W、X、Y、N四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热,可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为
(3)由X、Y、Z三种元素可组成摩尔质量为84 g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为
(4)(XY)2的性质与单质Q2相似,(XY)2与NaOH溶液常温下反应的离子方程式为
(5)常温下,1 mol Z3能与Y的最简单氢化物反应,生成一种常见的含氧酸盐和1 mol Z2,该反应的化学方程式为
(6)Z元素与除M外的其余五种元素间两两形成的化合物都不止一种,写出符合下列条件的化合物分子式
①Z与其它原子的个数比为2:1;
②分子中电子总数为奇数
(7)用如图的装置,既可设计比较X、M、N非金属性强弱的实验,也可设计比较N、Q非金属性强弱的实验。若用强酸制弱酸的原理比较X、M、N非金属性强弱,则A装置中发生反应的化学方程式是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D为同一周期的4种元素,已知0.2 mol A与足量酸充分反应后生成2.24 L H2(标准状况下)。B的氧化物既可溶于酸又可溶于强碱溶液。C、D离子的电子层结构与氩原子相同,C点燃时与氧气反应生成的氧化物可与C的气态氢化物反应得到C的单质,D单质常温下为气态。
(1)A、B、C、D的元素名称分别为:A____ ,B____ ,C____ ,D____ 。
(2)画出B的原子结构示意图________ 。
(3)C在周期表中位于第____ 周期_______ 族。
(1)A、B、C、D的元素名称分别为:A
(2)画出B的原子结构示意图
(3)C在周期表中位于第
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、R、W的原子序数逐渐增大,X原子的P轨道半充满,且X、Y、Z同周期,Y与R的价电子数相同。
(1)在化合物 中中心原子的VSEPR模型为
中中心原子的VSEPR模型为_______ ,X与Y的离子半径由小到大的顺序为_______ 。
(2)基态X原子的价层电子排布式为_______ ,X的一氢化物 是一种火箭燃料的成分,
是一种火箭燃料的成分, 分子中X原子轨道的杂化类型是
分子中X原子轨道的杂化类型是_______ ,NH3分子中的N原子有一个孤电子对,能发生反应:NH3 +HCl=NH4Cl,试写出将上述液态氮氢化合物加入少量盐酸中时,发生反应的化学方程式:_______ 。
(3)R、W两元素电负性较强的是(写元素符号)_______ ;写出证明这一结论的一个实验事实(用化学方程式表示):_______ 。
(1)在化合物
 中中心原子的VSEPR模型为
中中心原子的VSEPR模型为(2)基态X原子的价层电子排布式为
 是一种火箭燃料的成分,
是一种火箭燃料的成分, 分子中X原子轨道的杂化类型是
分子中X原子轨道的杂化类型是(3)R、W两元素电负性较强的是(写元素符号)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩十种元素,填写下列空白:
(1)元素②是周期表中形成化合物种类最多的元素,其原子结构示意图为_______ ,原子的电子式为_______ ;②的多种核素中有一种考古时用于测定文物年代,请写出其原子符号_______ 。
(2)元素①和⑤形成化合物的化学式为_______ ,该化合物中存在的化学键是_______ 。
(3)元素Se属于VIA族元素,Se的氢化物的化学式为_______ ,元素Se和元素⑨的氢化物稳定性强弱比较:_______ >_______ 。
(4)这十种元素的主族元素中,非金属性最强的元素为_______ (写元素符号);原子半径最大的是_______ (写元素符号);⑧⑨⑩三种元素的最高价氧化物对应的水化物中,酸性最强的是_______ (写酸的化学式)。
(5)⑤⑨⑩三种元素的简单离子半径,由大到小依次为_______ (写离子符号)
(6)元素⑤的单质在空气中加热,生成的产物与二氧化碳反应的化学方程式为_______ 。
(7)元素⑥的单质与水反应的化学方程式_______ 。
(8)元素⑦的硫酸盐溶液与氨水反应的离子方程式为_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①和⑤形成化合物的化学式为
(3)元素Se属于VIA族元素,Se的氢化物的化学式为
(4)这十种元素的主族元素中,非金属性最强的元素为
(5)⑤⑨⑩三种元素的简单离子半径,由大到小依次为
(6)元素⑤的单质在空气中加热,生成的产物与二氧化碳反应的化学方程式为
(7)元素⑥的单质与水反应的化学方程式
(8)元素⑦的硫酸盐溶液与氨水反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有部分短周期元素的性质或原子结构如下:
(1)X的无中子原子的符号为____________ ,Y的原子结构示意图为_____________ ,Q在元素周期表中的位置为___________________ 。
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______________________ (用化学式表示),写出两者反应的离子方程式:__________________________________________ 。
(3)M、W两种元素中非金属性较强的是______________ (用元素符号表示),下列表述中能证明这一事实的____________________ (填序号),
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
| 元素 | 元素的性质或原子结构 |
| X | 该元素的一种原子无中子 |
| Y | 原子半径最大的短周期元素 |
| Z | 第三周期元素中简单离子半径最小 |
| M | 地壳中含量最多的元素 |
| Q | 其氧化物是光导纤维的基本原料 |
| W | 其核电荷数为M元素核电荷数的2倍 |
(2)Y、Z的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)M、W两种元素中非金属性较强的是
a. 常温下,M的单质与W的单质的状态不同
b. 向W的氢化物中通入M2,有淡黄色固体析出
c. M、W形成的化合物中W元素为正价
您最近一年使用:0次



