下列对分子的性质的解释中,不正确的是:


| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
B.乳酸(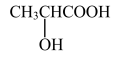 )有一对对映异构体,因为其分子中含有一个手性碳原子 )有一对对映异构体,因为其分子中含有一个手性碳原子 |
| C.水很稳定(1000 ℃以上才会部分分解)是因为水中含有大量的氢键 |
| D.由图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 |
19-20高二下·辽宁大连·阶段练习 查看更多[2]
(已下线)2.3 分子的结构与物质的性质(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)辽宁省大连市大连海湾高级中学2019-2020学年高二下学期第一次质量检测化学试题
更新时间:2020-07-21 13:12:26
|
相似题推荐
【推荐1】铁杉脂素是重要的木脂素类化合物,其结构简式如图所示。下列有关铁杉脂素的说法正确的是
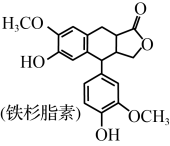

| A.能与甲醛发生缩聚反应 |
| B.分子中有3个手性碳原子 |
| C.分子中所有的碳原子可能处于同一平面 |
| D.1mol铁杉脂素与NaOH溶液反应最多消耗4molNaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科研人员发现g-C3N4非金属半导体可以在光照下催化水产生氢气。g-C3N4是一种平面二维片层结构,其基本结构如图,基本单元无限延伸,形成网状结构。下列说法正确的是
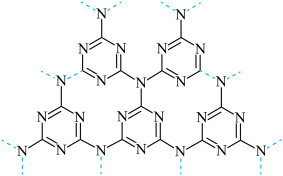
| A.g-C3N4属于离子晶体 |
| B.其核心元素氮的氢化物分子间存在氢键,因此加热时很难分解 |
| C.g-C3N4中氮原子为sp2杂化方式 |
| D.g-C3N4中含有手性碳原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列对分子的性质的解释中,不正确的是


| A.水很稳定(1000℃以上才会部分分解),但与水中含有大量氢键无关 |
| B.[Cu(NH3)4]SO4和(NH4)2SO4两种物质中都有配位键,所以都是配合物 |
| C.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
| D.由如图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的结构决定物质的性质,下列性质差异与结构因素匹配正确 的是
| 性质差异 | 结构因素 | |
| A | 热稳定性:HF大于HCl | HF分子间存在氢键,HCl分子间不存在氢键 |
| B | 酸性:CH3COOH>CH3CH2OH | 羟基的极性 |
| C | 键角:CH4(109.5°)大于NH3(107.3°) | 中心原子的杂化方式 |
| D | 熔点: | 晶体类型 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】不久前,科学家研发了一种能让人如鱼那样从水中持续不断吸收氧气的水晶材料——“海王水晶”,其吸收氧气的能力依靠的是钴离子。下列有关说法正确的是
| A.氧气在水中溶解度小是因为O2是非极性分子 |
| B.H2O分子内存在的化学键按分类有极性键、σ键和氢键 |
| C.矿物水晶的结构式为O=Si=O |
| D.钴元素位于元素周期表VIIIB族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列对一些实验事实的理论解释,正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 溴单质、碘单质在四氯化碳中的溶解度比在水中大 | 溴单质、碘单质和四氯化碳都为极性分子 |
| B | 卤素单质从F2到I2,在常温、常压下的聚集状态由气态、液态到固态 | 范德华力逐渐减小 |
| C | 在常温常压下,1体积水可以溶解700体积氨气 | 氨是极性分子且有氢键影响 |
| D | HF的沸点高于HCl | H-F的键长比H-Cl的短 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列物质分子内和分子间均可形成氢键的是( )
| A.NH3 | B.  | C.H2S | D.C2H5OH |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是:
| A.HF、HCl、HBr、HI的熔沸点依次升高 |
| B.碘和干冰的升华克服相同类型的作用力 |
| C.NaOH是离子化合物,NH4NO3是共价化合物 |
| D.NaHSO4溶于水时只破坏了离子键 |
您最近一年使用:0次

 低于NaBF4
低于NaBF4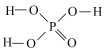 )中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
)中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是 H++H2PO2-、H2PO2-
H++H2PO2-、H2PO2-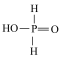
 杂化有关
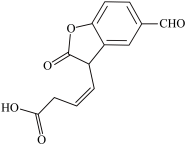
杂化有关 是新型环烯类储氢材料,利用物理吸附的方法来储存氢分子,其分子结构如图所示,下列相关说法不正确的是
是新型环烯类储氢材料,利用物理吸附的方法来储存氢分子,其分子结构如图所示,下列相关说法不正确的是
 键和
键和 键的数目比为4∶1
键的数目比为4∶1 间的作用力为氢键
间的作用力为氢键

