CO是一种重要的能源物质。
(1)下列反应原理适合实验室制备CO的是_______ (填选项字母)。
A.C+H2O CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH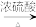 CO+H2O
CO+H2O
(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将_______ 能转化为______ 能。
②工作时,电极 I 作____ 极,电极 II 上的电极反应式为_____________ 。
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为___ mol/L
(1)下列反应原理适合实验室制备CO的是
A.C+H2O
 CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH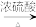 CO+H2O
CO+H2O(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将
②工作时,电极 I 作
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为
更新时间:2020-07-22 20:31:48
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)氢氧燃料电池的工作原理如图所示。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题:

碱式电池的电极反应:负极:___ ,正极:___ 。
(2)已知铅蓄电池放电的总反应为:PbO2+Pb+2H2SO4=2PbSO4+2H2O(原电池)。
写出放电负极的电极反应式为___ ,充电时负极与外接电源的___ 极相连。(填“正”或“负”)

碱式电池的电极反应:负极:
(2)已知铅蓄电池放电的总反应为:PbO2+Pb+2H2SO4=2PbSO4+2H2O(原电池)。
写出放电负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】看图回答下列问题
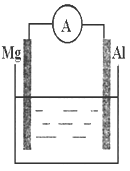
(1)若烧杯中溶液为稀硫酸,则观察到的现象是__________ ,电流表指针_______ (填偏转或不偏转),两极反应式为:
正极_______________________ ;
负极________________________ 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为__________ (填Mg或Al),总反应方程式为__________ 。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右下图所示:A、B两个电极均由多孔的碳块组成。
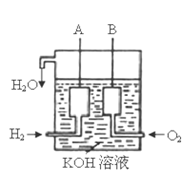
该电池的正极反应式为:_____________________ 。
(4)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电 池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:_________________ 。

(1)若烧杯中溶液为稀硫酸,则观察到的现象是
正极
负极
(2)若烧杯中溶液为氢氧化钠溶液,则负极为
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右下图所示:A、B两个电极均由多孔的碳块组成。

该电池的正极反应式为:
(4)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电 池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一个完整的氧化还原反应方程式可以拆分,写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2++Cu2+,可以写成:氧化反应 Cu-2e-=Cu2+;还原反应 2Fe3++2e—=2Fe2+(或Fe3++e-=Fe2+)。
(1)根据以上信息将反应3NO2+H2O=2H++2 +NO拆分成两个“半反应式”:氧化反应式
+NO拆分成两个“半反应式”:氧化反应式_________________________________ ;还原反应式___________________________ 。
(2)已知某一反应的“半反应式”为CH4+10OH--8e-= +7H2O;O2+2H2O+4e-=4OH-,则总反应式为
+7H2O;O2+2H2O+4e-=4OH-,则总反应式为_____________________________________ 。
(1)根据以上信息将反应3NO2+H2O=2H++2
 +NO拆分成两个“半反应式”:氧化反应式
+NO拆分成两个“半反应式”:氧化反应式(2)已知某一反应的“半反应式”为CH4+10OH--8e-=
 +7H2O;O2+2H2O+4e-=4OH-,则总反应式为
+7H2O;O2+2H2O+4e-=4OH-,则总反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下图为Cu-Zn稀硫酸原电池的装置示意图,根据此图回答下列问题:

(1)什么是原电池装置?___________________________________ 。
(2)负极材料是________ ,发生反应,电极反应式______________ ,正极材料是________ ,发生反应,电极反应式________________________________ 。

(1)什么是原电池装置?
(2)负极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】电能是现代社会应用最广泛的能源之一、
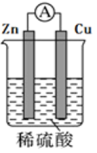
(1)某原电池装置如图所示。其中,Zn电极为原电池的___________ 极(填“正”或“负”)。
(2)Zn电极的电极反应式是___________ 。
(3)Cu电极上发生的反应属于___________ (填“氧化”或“还原”)反应。
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了___________ mol电子。
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2

(1)某原电池装置如图所示。其中,Zn电极为原电池的
(2)Zn电极的电极反应式是
(3)Cu电极上发生的反应属于
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】人们常常利用化学反应中的能量变化为人类服务。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是_________ 。
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是_________ 。
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:
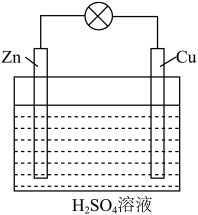
①负极材料是_______ ,正极上能够观察到的现象是_______________________ ,
②正极的电极反应式是______________ 。
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体________ L(标况下)。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:

①负极材料是
②正极的电极反应式是
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】电能是现代社会应用最广泛的能源之一、

(1)某原电池装置如图所示。其中,Zn电极为原电池的___________ 极(填“正”或“负”)。
(2)Zn电极的电极反应式是___________ 。
(3)Cu电极上发生的反应属于___________ (填“氧化”或“还原”)反应。
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了___________ mol电子。
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2

(1)某原电池装置如图所示。其中,Zn电极为原电池的
(2)Zn电极的电极反应式是
(3)Cu电极上发生的反应属于
(4)当铜表面析出4.48L氢气(标准状况)时,导线中通过了
(5)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①CaO+H2O=Ca(OH)2
②2H2+O2=2H2O
③2FeCl3+Cu=CuCl2+2FeCl2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
①已知:放电时,负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2,则正极反应式为__ 。
②放电时,_____ (填“正”或“负”)极附近溶液的碱性增强。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
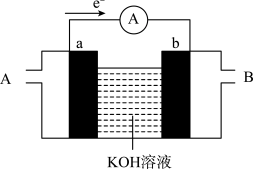
①使用时,空气从_____ 口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇(CH3OH),a极的电极反应式为__ 。
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:①已知:放电时,负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2,则正极反应式为
②放电时,
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲醇(CH3OH),a极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】氢氧燃料电池以 溶液为电解质,其总反应的化学方程式为
溶液为电解质,其总反应的化学方程式为 。
。
(1)负极上的电极反应为_______ 。
(2)消耗标准状况下的 时,有
时,有________  电子发生转移。
电子发生转移。
(3)工作过程中时,溶液的
________  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
 溶液为电解质,其总反应的化学方程式为
溶液为电解质,其总反应的化学方程式为 。
。(1)负极上的电极反应为
(2)消耗标准状况下的
 时,有
时,有 电子发生转移。
电子发生转移。(3)工作过程中时,溶液的

 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知:2H2+O2 2H2O。
2H2O。
(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量___________ 。
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:___________ 。
②如把H2改为甲烷,则负极反应式为:_______ ,该甲烷燃料电池总反应的离子方程式为:________ 。
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为_______ ;若导线中转移电子2mol,则标况下,正极消耗的O2为_______ L
 2H2O。
2H2O。(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:
②如把H2改为甲烷,则负极反应式为:
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应: ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
(1)B的转化率___________ 。
(2)恒温达平衡时容器内的压强与开始时压强比___________ 。
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
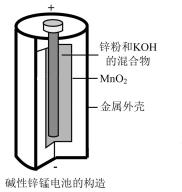
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是___________ (填名称),负极上发生的电极反应为___________ 。若反应消耗13g负极材料,则电池中转移电子的物质的量为___________ mol。
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为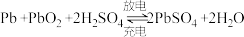 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。
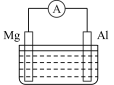
(5)镁铝电池的构造如图所示,当电解质溶液为NaOH溶液时,可知电池的负极材料为_______ (填“Mg”或“Al”),正极上的电极反应式为___________ 。
 ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:(1)B的转化率
(2)恒温达平衡时容器内的压强与开始时压强比
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为
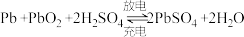 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。| A.电解液中H2SO4的浓度始终保持不变 |
B.放电时正极上的电极反应式为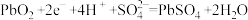 |
| C.放电时,当外电路通过1mol电子时,理论上负极质量增加48g |
D.放电时,溶液中的 向正极移动 向正极移动 |

您最近一年使用:0次





