下列操作或结论不正确 的是
| A.蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置 |
| B.中和滴定时, 滴定管需用所要盛装的溶液润洗内壁 2~ 3 次 |
C.在未知溶液中滴加 BaCl2溶液出现白色沉淀, 加稀盐酸, 沉淀不溶解, 说明该未知溶液中一定存在SO |
| D.配制一定物质的量浓度的 NaOH 溶液时, NaOH 固体溶解后未冷却就转移至容量瓶中,则所配制的溶液浓度偏高 |
19-20高二下·浙江丽水·期末 查看更多[3]
更新时间:2020-07-24 16:25:10
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作、现象及结论正确的是
| A.过量铜与稀硝酸充分反应后,再滴加一定量稀硫酸,铜又能继续溶解 |
B.向某溶液中加入浓的 溶液并加热,产生的气体能使湿润的蓝色石蕊试纸变红,说明原溶液中存在 溶液并加热,产生的气体能使湿润的蓝色石蕊试纸变红,说明原溶液中存在 |
C.向某溶液中加入 溶液,有白色沉淀生成,说明原溶液中一定含有 溶液,有白色沉淀生成,说明原溶液中一定含有 |
| D.高温下,将铁片放入浓硫酸中,无明显现象,说明铁与浓硫酸发生钝化现象 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列依据实验现象推理得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向淀粉溶液中加入几滴稀硫酸,加热,待溶液冷却后向其中加入银氨溶液,水浴加热,无银镜产生 | 淀粉未发生水解 |
| B | 向乙醇样品中加入一小块金属钠,有气泡生成 | 该乙醇样品中含有水 |
| C | 某盐溶液中加入 溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该盐溶液中含有 |
| D | 某溶液中加入 溶液,产生白色沉淀,再加稀硝酸沉淀不溶解 溶液,产生白色沉淀,再加稀硝酸沉淀不溶解 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中受热所剩固体的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | 探究KI与FeCl3反应的限度 | 取5mL0.1mol·L-1KI溶液于试管中,加入1mL0.1mol·L-1FeCl3溶液,充分反应后滴入几滴KSCN溶液 | 若溶液变红,则KI与FeCl3的反应有一定限度 |
| C | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀硫酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| D | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,滴加稀氢氧化钠溶液,用湿润的红色石蕊试纸放试管口 | 不变蓝,证明溶液中无铵根离子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液,滴定曲线,如图所示,下列说法不正确的是
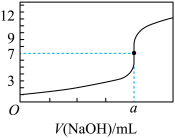

| A.a=20.00 |
B.滴定过程中,可能存在: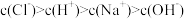 |
| C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】可逆反应有一定的反应限度,平衡常数的大小能反映化学反应进行的程度。为测定可逆反应 的平衡常数K,实验步骤如下。
的平衡常数K,实验步骤如下。
I.一定温度下,将0.01mol/L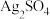 溶液与0.04mol/L
溶液与0.04mol/L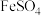 溶液等体积混合。
溶液等体积混合。
Ⅱ.待实验I中反应达到平衡状态时,取V mL上层清液,用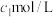
 标准溶液进行滴定,达到终点时,消耗
标准溶液进行滴定,达到终点时,消耗 标准溶液
标准溶液
 。
。
已知: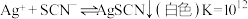
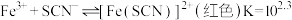
下列操作使测定的K值偏小的是
 的平衡常数K,实验步骤如下。
的平衡常数K,实验步骤如下。I.一定温度下,将0.01mol/L
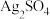 溶液与0.04mol/L
溶液与0.04mol/L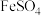 溶液等体积混合。
溶液等体积混合。Ⅱ.待实验I中反应达到平衡状态时,取V mL上层清液,用
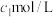
 标准溶液进行滴定,达到终点时,消耗
标准溶液进行滴定,达到终点时,消耗 标准溶液
标准溶液
 。
。已知:
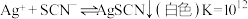
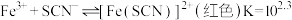
下列操作使测定的K值偏小的是
| A.取实验Ⅰ的浊液测定 |
| B.滴定过程中振荡剧烈,有待测液溅出 |
| C.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡 |
| D.达到终点时最后半滴标准液用蒸馏水冲入锥形瓶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】为了配制100mL 1mol•L﹣1的NaOH溶液,其中有下列几个操作:①NaOH固体放在纸上进行称量②选刚用蒸馏水洗净的100mL容量瓶进行配制③NaOH在烧杯里刚好完全溶解,立即把溶液转移到容量瓶中④用蒸馏水洗涤烧杯内壁和玻璃棒2次,洗涤液也均转入容量瓶中⑤使蒸馏水沿玻璃棒注入容量瓶,直到溶液的凹液面恰好与刻度线相切.其中错误的是( )
| A.①②③ | B.③④⑤ | C.②③⑤ | D.①③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】实验室保存的浓盐酸标签如图所示,某同学用此浓盐酸配制500mL浓度为0.2mol/L的稀盐酸,下列说法错误的是
| 盐酸 | |
| 分子式 | HCl |
| 相对分子质量 | 36.5 |
| 密度 | 1.19g/mL |
| HCl的质量分数 | 36.5% |
| A.该浓盐酸的物质的量浓度为11.9mol/L |
| B.需用量筒量取8.4mL的浓盐酸进行配制 |
| C.配制溶液所用的容量瓶不需要烘干 |
| D.使用量筒时俯视刻度线,所配溶液浓度偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验装置正确且能达到实验目的的是
| A | B | C | D |
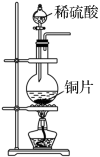 | 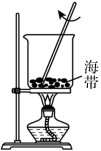 | 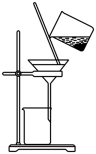 | 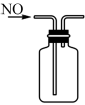 |
制备 | 灼烧海带 | 分离加入食盐后的蛋白质与水的混合物 | 排空气法收集 气体 气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
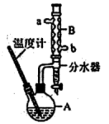
【推荐2】实验室制备苯甲酸乙酯,装置如图所示,原理是在环己烷中发生如下反应: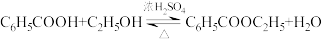 。已知:环己烷沸点为80.8℃,可与水形成共沸物,其混合物沸点为62.1℃,下列说法错误的是
。已知:环己烷沸点为80.8℃,可与水形成共沸物,其混合物沸点为62.1℃,下列说法错误的是
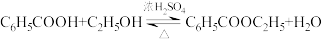 。已知:环己烷沸点为80.8℃,可与水形成共沸物,其混合物沸点为62.1℃,下列说法错误的是
。已知:环己烷沸点为80.8℃,可与水形成共沸物,其混合物沸点为62.1℃,下列说法错误的是
| A.装置B中b为冷凝水进水口 |
| B.加入的环己烷可提高苯甲酸乙酯产率 |
| C.反应后向A中的溶液加入氯化钠以除去硫酸和剩余的苯甲酸 |
| D.若分水器中水层超过支管口下沿,应打开分水器旋钮放水 |
您最近一年使用:0次