常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液,滴定曲线,如图所示,下列说法不正确的是
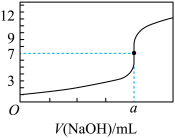

| A.a=20.00 |
B.滴定过程中,可能存在: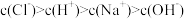 |
| C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00 |
11-12高三上·北京朝阳·期末 查看更多[2]
更新时间:2016-12-09 01:27:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,用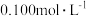 NaOH溶液分别滴定
NaOH溶液分别滴定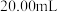
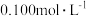 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

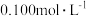 NaOH溶液分别滴定
NaOH溶液分别滴定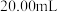
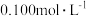 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

A. 时,滴定醋酸消耗的 时,滴定醋酸消耗的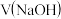 小于20mL 小于20mL |
| B.Ⅰ表示的是滴定盐酸的曲线 |
C.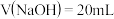 时,两份溶液中 时,两份溶液中 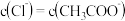 |
D.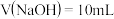 时,醋酸溶液中 时,醋酸溶液中 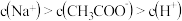 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,向20.00mL 盐酸中滴加
盐酸中滴加 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。下列说法错误的是
NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。下列说法错误的是
 盐酸中滴加
盐酸中滴加 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。下列说法错误的是
NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。下列说法错误的是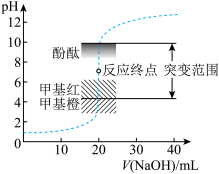
A.NaOH与盐酸恰好完全反应时, |
| B.选择变色范围在pH突变范围内的指示剂,可减小实验误差 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
D.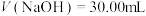 时,水电离受到抑制 时,水电离受到抑制 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】25℃时,水的离子积常数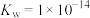 。下列说法正确的是
。下列说法正确的是
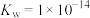 。下列说法正确的是
。下列说法正确的是A.0.005  溶液的pH=2,抑制了水的电离 溶液的pH=2,抑制了水的电离 |
B.向纯水中加入NaOH固体,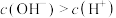 ,促进了水的电离 ,促进了水的电离 |
C.0.005  溶液与0.01 溶液与0.01 NaOH溶液等体积混合,pH=11 NaOH溶液等体积混合,pH=11 |
D.将100mL pH=5的 溶液稀释1000倍,pH=8 溶液稀释1000倍,pH=8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图示实验设计或实验操作错误的是
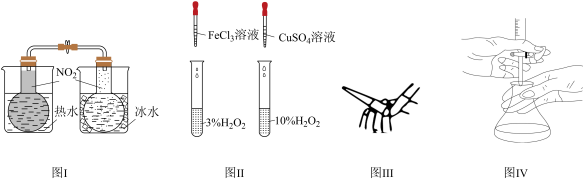

| A.图Ⅰ探究温度对化学平衡的影响 |
| B.图Ⅱ探究不同催化剂对H2O2分解速率的影响 |
| C.图Ⅲ除去碱式滴定管胶管中的气泡 |
| D.图Ⅳ用已知浓度的酸溶液滴定未知浓度的碱溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用下列装置进行实验,不能达到实验目的的是
| 选项 | A | B | C | D |
| 装置图 |  | 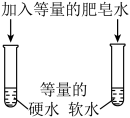 | 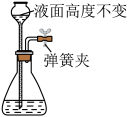 | 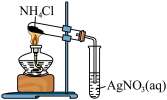 |
| 实验目的 | 碱式滴定管排气泡 | 鉴别硬水和软水 | 证明装置的气密性良好 | 证明氯化铵的不稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列操作不能达到实验目的的是
| 实验操作 | 实验目的 | |
| A | 向含少量水的乙醇中加入无水硫酸铜,蒸馏 | 制备无水乙醇 |
| B | 以甲基橙为指示剂,用盐酸滴定Na2CO3标准溶液 | 测定盐酸浓度 |
| C | 补铁药品粉碎并加水溶解,向其中滴加KSCN溶液 | 检验药品是否变质 |
| D | 含少量KNO3杂质的NaCl溶液蒸发结晶、趁热过滤、洗涤、干燥 | 提纯NaCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,向10.0mL纯碱(可能含有 )的稀溶液中逐滴加入0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
)的稀溶液中逐滴加入0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是

 )的稀溶液中逐滴加入0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
)的稀溶液中逐滴加入0.100mol/L盐酸,滴定曲线如图,其中p、q为滴定终点,下列分析正确的是
| A.p→q,选用酚酞做指示剂,到达滴定终点时溶液由红色变为无色 |
B.由滴定数据可知,原纯碱中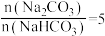 |
C.p点 的主要原因: 的主要原因: |
D.q点溶液中: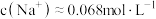 |
您最近一年使用:0次

 溶液
溶液

