下列图示实验设计或实验操作错误的是
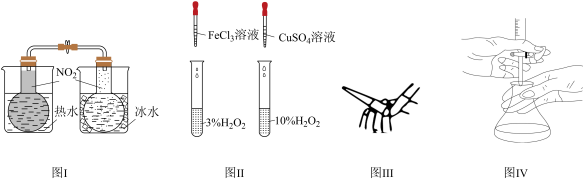

| A.图Ⅰ探究温度对化学平衡的影响 |
| B.图Ⅱ探究不同催化剂对H2O2分解速率的影响 |
| C.图Ⅲ除去碱式滴定管胶管中的气泡 |
| D.图Ⅳ用已知浓度的酸溶液滴定未知浓度的碱溶液 |
更新时间:2021-01-01 10:17:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量),下列结论正确的是
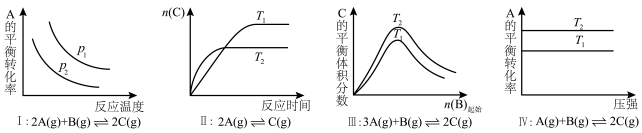

A.反应I: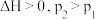 |
B.反应II: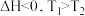 |
C.反应III: 或 或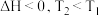 |
D.反应IV: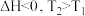 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】“蓝天保卫战”需要持续进行大气治理,有效处理 、
、 等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。已知反应:
等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。已知反应: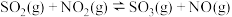
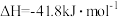 ,标准状况下,
,标准状况下,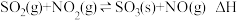 。下列有关说法
。下列有关说法错误 的是
 、
、 等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。已知反应:
等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。已知反应: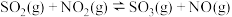
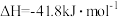 ,标准状况下,
,标准状况下,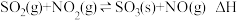 。下列有关说法
。下列有关说法| A.升高反应温度可提高废气转化率 |
B.该反应的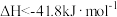 |
C.若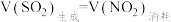 ,则该反应到达平衡状态 ,则该反应到达平衡状态 |
D.该反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定条件下存在反应:CO(g) + H2O(g)  CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
 CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是| A.容器I、II中正反应速率相同 |
| B.容器I中CO的转化率与容器II中CO2的转化率相等 |
| C.容器II、III中反应的平衡常数相同 |
| D.容器I中CO的物质的量比容器II中的多。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一支量程为25.00mL的滴定管,若液面在8.00mL处,将溶液全部放下来,液体的体积为( )
| A.大于17.00mL | B.大于8.00mL | C.等于17.00mL | D.等于8.00mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】莫尔法是用K2CrO4作指示剂,用AgNO3标准溶液测定Cl-(或Br-)浓度的方法。现用莫尔法测定亚硝酰氯样品中NOCl的纯度,实验步骤如下:
步骤1:配制AgNO3溶液。
步骤2:标定AgNO3溶液。准确称取0.585g干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至100mL容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份25.00mL,分别置于锥形瓶中,加25mL水、适量K2CrO4溶液,在不断摇动下用AgNO3溶液滴定至终点[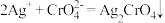 (砖红色)]。实验测得三次滴定消耗AgNO3溶液体积的平均值为25.00mL。
(砖红色)]。实验测得三次滴定消耗AgNO3溶液体积的平均值为25.00mL。
步骤3:测定亚硝酰氯样品中NOCl的纯度。取mgNOCl样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成250mL溶液,准确量取25.00mL溶液于锥形瓶中;加入适量K2CrO4溶液作指示剂,用上述AgNO3标准溶液滴定至终点,消耗AgNO3标准溶液的体积为VmL。
对于上述实验,下列说法正确的是
步骤1:配制AgNO3溶液。
步骤2:标定AgNO3溶液。准确称取0.585g干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至100mL容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份25.00mL,分别置于锥形瓶中,加25mL水、适量K2CrO4溶液,在不断摇动下用AgNO3溶液滴定至终点[
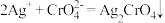 (砖红色)]。实验测得三次滴定消耗AgNO3溶液体积的平均值为25.00mL。
(砖红色)]。实验测得三次滴定消耗AgNO3溶液体积的平均值为25.00mL。步骤3:测定亚硝酰氯样品中NOCl的纯度。取mgNOCl样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成250mL溶液,准确量取25.00mL溶液于锥形瓶中;加入适量K2CrO4溶液作指示剂,用上述AgNO3标准溶液滴定至终点,消耗AgNO3标准溶液的体积为VmL。
对于上述实验,下列说法正确的是
| A.配制好的AgNO3溶液贮存于带玻璃塞的棕色广口瓶中 |
| B.可用移液管移取25.00mLNaCl溶液于锥形瓶中,使用时应用手握住移液管的中部 |
| C.滴定管使用前应“检漏”,向管内注入少量水,观察滴定管口及旋塞是否有水渗出,若不渗水即可使用 |
| D.NOCl与水反应的离子方程式为2NOCl+H2O=2H++2Cl-+NO↑+NO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,用相同浓度的KOH溶液,分别滴定浓度均为0.1 mol·L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断正确的是


| A.滴定至P点时,溶液中:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-) |
| B.当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)-c(OH-)=c(H+) |
| C.同浓度的KA、KB、KD三种盐溶液的pH大小关系:pH(KA) > pH(KB) > pH(KD) |
| D.当三种酸都中和至中性时,消耗KOH溶液的体积的大小关系为:V(HA) < V(HB) < V(HD) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化铁在金属蚀刻、污水处理等方面有广泛应用。某兴趣小组以废铁屑为原料,用如图所示装置制备
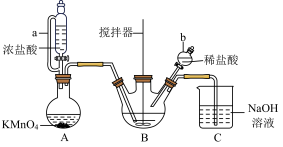
已知: 易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/L 溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
II. 溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含
溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含 的混合液。
的混合液。
III. 溶液的制备:由装置A制备氯气;向
溶液的制备:由装置A制备氯气;向 的混合液中缓慢通入足量的氯气。
的混合液中缓慢通入足量的氯气。
IV. 产品的分离提纯:将三颈烧瓶中的
产品的分离提纯:将三颈烧瓶中的 混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到
混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到 产品。
产品。
V. 产品的纯度测定:用碘量法滴定并计算。
产品的纯度测定:用碘量法滴定并计算。
上述实验步骤V中,碘量法的滴定反应原理是: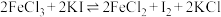 ,
,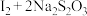
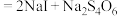 。
。
下列相关说法正确的是


已知:
 易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/L
 溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。II.
 溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含
溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含 的混合液。
的混合液。III.
 溶液的制备:由装置A制备氯气;向
溶液的制备:由装置A制备氯气;向 的混合液中缓慢通入足量的氯气。
的混合液中缓慢通入足量的氯气。IV.
 产品的分离提纯:将三颈烧瓶中的
产品的分离提纯:将三颈烧瓶中的 混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到
混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到 产品。
产品。V.
 产品的纯度测定:用碘量法滴定并计算。
产品的纯度测定:用碘量法滴定并计算。上述实验步骤V中,碘量法的滴定反应原理是:
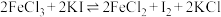 ,
,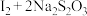
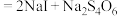 。
。下列相关说法正确的是
| A.用托盘天平称取5.000g样品 |
| B.用碱式滴定管取出25.00mL待测液于锥形瓶中 |
| C.用淀粉溶液作指示剂,进行两次滴定,取平均值 |
D.由于 与KI溶液的反应可逆,会导致测得纯度偏低 与KI溶液的反应可逆,会导致测得纯度偏低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用下列实验装置进行相应实验,能达到实验目的是
A.分离乙醇和乙酸混合溶液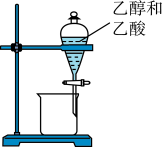 |
B.石油分馏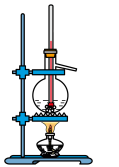 |
C.电解精炼铜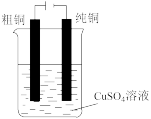 |
D.实验室用乙醇制取乙烯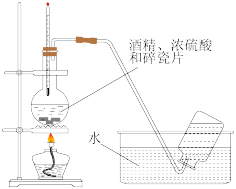 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关实验的操作正确的是
| 实验 | 操作 | |
| A | 检验焦炉煤气中含有甲烷 | 将焦炉煤气通入Cl2中,光照,观察现象 |
| B | 用粗锌(主要杂质Pb、ZnS等)与稀硫酸制备纯净的H2 | 将反应产生的气体经足最KMnO4溶液洗涤,再通过碱石灰干燥 |
| C | 检验炭与热的浓硝酸产生的气体中含有CO2 | 将生成的气体通入澄清石灰水,观察现象 |
| D | 用MnO2、NaCl及浓硫酸加热制取少量纯净干燥的Cl2 | 将反应产生的气体通过浓硫酸洗涤,再通过饱和食盐水洗涤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

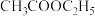 中混有的
中混有的
 溶液测定
溶液测定 溶液的浓度,可以选择酚酞或者甲基橙为指示剂
溶液的浓度,可以选择酚酞或者甲基橙为指示剂

