已知一定质量的锌粒与稀盐酸反应,生成H2的浓度与反应时间的关系如图所示,下列结论不正确的是
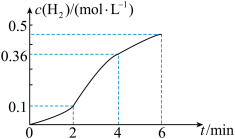

| A.反应速率υ(0-2min)﹥υ(2-4min)﹥υ(4-6min) |
| B.反应前4min内温度对反应速率的影响比浓度大 |
| C.若将锌粒改为锌粉,可加快产生H2的反应速率 |
| D.反应前4min内生成H2的平均速率υ(H2)=0.09mol·L-1·min-1 |
更新时间:2020-07-29 11:39:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一定温度下,将一定量的气体通入体积为2 L的密闭容器中,使其发生反应,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )


A.该反应的化学方程式为:3Z 2X+3Y 2X+3Y |
| B.t0时,反应停止,反应速率为0 |
| C.t0时,Z的浓度为1.2 mol/L |
| D.t0时,X、Y、Z的质量不再改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下,密闭容器中发生反应: ,其平均反应速率
,其平均反应速率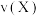 如下,其中反应速率最大的是
如下,其中反应速率最大的是
 ,其平均反应速率
,其平均反应速率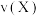 如下,其中反应速率最大的是
如下,其中反应速率最大的是A. | B. |
C.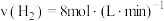 | D.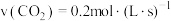 |
您最近一年使用:0次
【推荐1】设NA为阿伏加德罗常数值。如图表示N2O在Pt2O+表面与CO反应转化成无害气体的过程。下列说法正确的是


A.反应Ⅰ的离子方程式为N2O+Pt2O+=N2+Pt2O ,其中Pt2O+在反应中做氧化剂 ,其中Pt2O+在反应中做氧化剂 |
| B.每1molCO转化为CO2得电子数为2NA |
C.N2O与CO反应转化成无害气体的总反应为N2O+CO=N2+CO2,该反应的催化剂是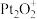 |
| D.1gCO2、N2O的混合气体中含有电子数为0.5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
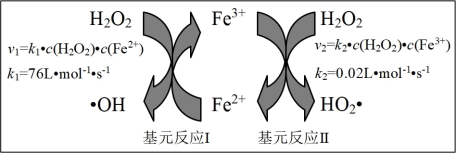
【推荐2】均相芬顿反应原理是高级氧化技术的经典工艺之一,如图所示( 和
和 为速率常数)。下列说法错误的是
为速率常数)。下列说法错误的是
 和
和 为速率常数)。下列说法错误的是
为速率常数)。下列说法错误的是
| A.相同条件下,基元反应I比II的活化能低 |
| B.基元反应I中氧元素的化合价发生变化 |
| C.基元反应II的化学方程式为H2O2+Fe3+=HO2·+Fe2++H+ |
D.芬顿反应进行的过程中,整个体系的 几乎不变(忽略体积变化) 几乎不变(忽略体积变化) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某研究人员通过测定不同条件下的化学反应速率得到以下两组数据(Ea为反应活化能)
第1组:
第2组:
基于数据分析和平衡原理以下认识错误的是
第1组:
| 实验 | 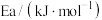 |  | 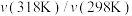 |
| A | 100 | 298→318 | 14.0 |
| 实验 | 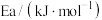 | 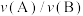 |
| A | 100 | 3205 |
| B | 120 |
| A.该实验的目的是为了对比温度和活化能对化学反应速率的影响程度 |
| B.其他条件相同时,温度升高,化学反应速率加快 |
| C.对于吸热反应,温度升高对于放热方向的反应速度影响较大 |
| D.一般离子反应的活化能接近于零,所以反应速率很快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】 分解速率(分解速率可用单位时间内
分解速率(分解速率可用单位时间内 物质的量浓度的减少量表示)受多种因素影响。实验测得70℃时不同条件下
物质的量浓度的减少量表示)受多种因素影响。实验测得70℃时不同条件下 浓度随时间的变化如图所示。表示下列说法正确的是
浓度随时间的变化如图所示。表示下列说法正确的是
 分解速率(分解速率可用单位时间内
分解速率(分解速率可用单位时间内 物质的量浓度的减少量表示)受多种因素影响。实验测得70℃时不同条件下
物质的量浓度的减少量表示)受多种因素影响。实验测得70℃时不同条件下 浓度随时间的变化如图所示。表示下列说法正确的是
浓度随时间的变化如图所示。表示下列说法正确的是
A.图甲表明,其他条件相同时, 浓度越小,其分解速率越快 浓度越小,其分解速率越快 |
B.图乙表明,其他条件相同时,溶液 越小, 越小, 分解速率越快 分解速率越快 |
C.图丙表明,少量 存在时,溶液碱性越强, 存在时,溶液碱性越强, 分解速率越快 分解速率越快 |
D.图丁表明,碱性溶液中, 对 对 分解速率的影响大 分解速率的影响大 |
您最近一年使用:0次

 发生如下反应
发生如下反应
 有关数据如下:
有关数据如下: 的平均生成速率/
的平均生成速率/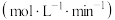
 的浓度大于
的浓度大于
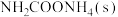 的反应速率为
的反应速率为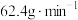



 值
值 2SO3,这是一个正反应放热的可逆反应.如果在密闭容器中通入2molSO2和足够多的氧气,按上述条件进行反应,下列有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应.如果在密闭容器中通入2molSO2和足够多的氧气,按上述条件进行反应,下列有关说法中错误的是

