氮及其化合物在化肥、医药、材料和国防工业中具有广泛应用。回答下列问题:
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类的温饱问题作出了极大贡献。写出实验室制备氨气的方程式_________ 。
(2)有人设想寻求合适的催化剂和电极材料,以 、
、 为电极反应物,以
为电极反应物,以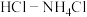 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。

①a电极是该电池的_______ (填正极或者负极);该电池正极的电极反应式是___________ 。
②该电池在工作过程中 的浓度将不断
的浓度将不断_________ (填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供
时,理论上电池能为外电路提供___________ mol电子。
(3)肼 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: 。请写出该电池放电时,负极的电极反应式:
。请写出该电池放电时,负极的电极反应式:__________ 。
(4)为了监测空气中NOx的含量,科学家成功研制出了一种NOx传感器,其工作原理示意图如图:
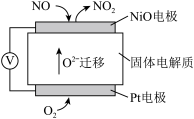
①固体电解质中 移向
移向___________ (填“正极”或“负极”)
②写出 电极发生的电极反应式:
电极发生的电极反应式:________ 。
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类的温饱问题作出了极大贡献。写出实验室制备氨气的方程式
(2)有人设想寻求合适的催化剂和电极材料,以
 、
、 为电极反应物,以
为电极反应物,以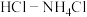 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
①a电极是该电池的
②该电池在工作过程中
 的浓度将不断
的浓度将不断 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供
时,理论上电池能为外电路提供(3)肼
 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: 。请写出该电池放电时,负极的电极反应式:
。请写出该电池放电时,负极的电极反应式:(4)为了监测空气中NOx的含量,科学家成功研制出了一种NOx传感器,其工作原理示意图如图:

①固体电解质中
 移向
移向②写出
 电极发生的电极反应式:
电极发生的电极反应式:
更新时间:2020-07-29 10:27:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】氮及其化合物有着广泛的应用。
(1)自然界中一些含氮的物质在细菌作用下实现氮的循环(如图所示),图中反应①~④中属于氮的固定的是___________ (填序号)。

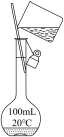
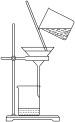
(2)某兴趣小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

①图中制取氨气的化学方程式是___________ 。湿润棉花的作用是___________ (填一条)。
②干燥管中的碱石灰___________ (填“能”或“不能”)用无水 代替。
代替。
③用上图装置进行喷泉实验,烧瓶中已装满干燥氨气,引发喷泉的操作是___________ 。
(3)铵盐是农业上常用的化肥,如硫酸铵、碳酸氢铵。检验某溶液中含有 的方法是取适量该溶液于试管中,加入
的方法是取适量该溶液于试管中,加入___________ 并加热,将湿润的红色石蕊试纸放于试管口,若试纸变___________ ,说明该溶液中含有 。
。
(1)自然界中一些含氮的物质在细菌作用下实现氮的循环(如图所示),图中反应①~④中属于氮的固定的是

(2)某兴趣小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

①图中制取氨气的化学方程式是
②干燥管中的碱石灰
 代替。
代替。③用上图装置进行喷泉实验,烧瓶中已装满干燥氨气,引发喷泉的操作是
(3)铵盐是农业上常用的化肥,如硫酸铵、碳酸氢铵。检验某溶液中含有
 的方法是取适量该溶液于试管中,加入
的方法是取适量该溶液于试管中,加入 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】根据要求完成下列问题。
(1)补齐物质与其用途之间的连线____________ 。
(2)选择完成下列实验的装置。
①除去粗盐水中的泥沙,用_______ (填序号,下同)。
②配制100mL NaCl溶液,用
NaCl溶液,用_______ 。
③加热 和浓盐酸的混合物制
和浓盐酸的混合物制 ,用
,用_______ 。
④加热 和
和 固体混合物制取
固体混合物制取 ,用
,用_______ 。
(3)化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下。 ,若反应中每生成6mol
,若反应中每生成6mol ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为_____ L,生成氮气的质量为____ g。
(1)补齐物质与其用途之间的连线
| 物质 | 用途 | |||
| A. | 氧化铁 | —————— | a. | 作红色颜料 |
| B. | 乙烯 | b | 作食用碱 | |
| C. | 乙醇 | c. | 制塑料 | |
| D. | 碳酸钠 | d. | 作消毒剂 |
|
|
|
|
A | B | C | D |
②配制100mL
 NaCl溶液,用
NaCl溶液,用③加热
 和浓盐酸的混合物制
和浓盐酸的混合物制 ,用
,用④加热
 和
和 固体混合物制取
固体混合物制取 ,用
,用(3)化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下。
 ,若反应中每生成6mol
,若反应中每生成6mol ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氨气的实验室制法
(1)反应原理:利用复分解反应强碱制弱碱。___________
药品的选择:
①铵盐:制取NH3时,一般用NH4Cl而不用NH4NO3、(NH4)2SO4或(NH4)2CO3,原因如下:
②碱:一般用熟石灰,不用NaOH或KOH,因为NaOH或KOH易吸水结块,而且对玻璃仪器腐蚀性较强。
装置:

氨气制备实验各部分装置的选择:
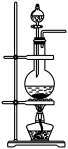
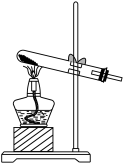
(2)其它实验室制取NH3的简易方法
(1)反应原理:利用复分解反应强碱制弱碱。
药品的选择:
①铵盐:制取NH3时,一般用NH4Cl而不用NH4NO3、(NH4)2SO4或(NH4)2CO3,原因如下:
| 铵盐 | 不选用的理由 |
| NH4NO3 | 受热分解,会发生爆炸,不安全 |
| (NH4)2SO4 | 与Ca(OH)2反应时生成CaSO4,反应物呈块状,不利于NH3逸出,且反应后试管难清洗 |
| (NH4)2CO3 | 受热分解会产生CO2,使收集到的NH3不纯 |
②碱:一般用熟石灰,不用NaOH或KOH,因为NaOH或KOH易吸水结块,而且对玻璃仪器腐蚀性较强。
装置:

氨气制备实验各部分装置的选择:
| 装置 | 选择 | 选择原因 |
| 制备装置 | 固+固 气 气 | 反应原理 |
| 净化装置 | 装有碱石灰的干燥管 | NH3具有碱性,不与碱石灰反应 |
| 不用浓硫酸和无水氯化钙 | NH3能被浓硫酸和无水氯化钙吸收 | |
| 收集装置 | 向下排空气法 | NH3的密度远小于空气,且常温下不与空气成分反应 |
| 不采用排水法 | NH3极易溶于水 | |
| 验满方法 | 将湿润的红色石蕊试纸置于试管口,试纸变蓝色 | 氨水显碱性 |
| 将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生 | 氨气遇挥发性酸反应生成固体铵盐小颗粒 | |
| 尾气处理 | 试管口放一团用水或稀硫酸浸湿的棉花球 | NH3极易溶于水,与酸反应 |
(2)其它实验室制取NH3的简易方法
| 方法 | 化学方程式(或原理) | 气体发生装置 |
| 加热浓氨水 |  | |
| 浓氨水+固体NaOH | NaOH溶于水放热,促使NH3·H2O分解,且OH-浓度的增大也有利于NH3的生成 |  |
| 浓氨水+固体CaO | CaO与水反应生成OH-,使溶剂(水)减少; 且反应放热,促使NH3·H2O分解。 化学方程式:NH3·H2O+CaO=NH3↑+Ca(OH)2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如下图:

(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇。
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为________________________________________ 。
(2)此流程的第I步反应为:CH4(g) + H2O(g) CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1
CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1_________ P2。(填“<”、“>”或“=”)100℃时,将1 mol CH4和2 mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K=____________ 。

(3)此流程的第II步反应CO(g) + H2O(g) CO2(g) + H2(g),
CO2(g) + H2(g),
的平衡常数随温度的变化如下表:
从上表可以推断:该反应是________ 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为__________ 。
右图表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图中t2时刻发生改变的条件是____ (写出一种)。

(4)某化学兴趣小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是____________________________ 。


(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇。
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为
(2)此流程的第I步反应为:CH4(g) + H2O(g)
 CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1
CO(g) + 3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图。则P1
(3)此流程的第II步反应CO(g) + H2O(g)
 CO2(g) + H2(g),
CO2(g) + H2(g),的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
从上表可以推断:该反应是
右图表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图中t2时刻发生改变的条件是

(4)某化学兴趣小组构想将NO转化为HNO3(NO3-),装置如图,电极为多孔惰性材料。则负极的电极反应式是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】焦亚硫酸钠 在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
(1)生产 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式___________ 。
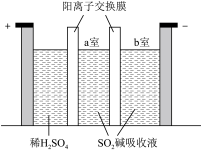
(2)制备 也可采用三室膜电解技术,装置如图所示,其中
也可采用三室膜电解技术,装置如图所示,其中 碱吸收液中含有
碱吸收液中含有 和
和 。阳极的电极反应式为
。阳极的电极反应式为___________ 。电解后,________ 室的 浓度增加。将该室溶液进行结晶脱水,可得到
浓度增加。将该室溶液进行结晶脱水,可得到 。
。
 在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:(1)生产
 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式(2)制备
 也可采用三室膜电解技术,装置如图所示,其中
也可采用三室膜电解技术,装置如图所示,其中 碱吸收液中含有
碱吸收液中含有 和
和 。阳极的电极反应式为
。阳极的电极反应式为 浓度增加。将该室溶液进行结晶脱水,可得到
浓度增加。将该室溶液进行结晶脱水,可得到 。
。
您最近一年使用:0次
【推荐3】氨是最重要的氮肥,是产量最大的化工品之一。其合成原理为:N2(g)+3H2(g) 2NH3(g), 某同学为了探究氮气和氢气反应生成氨气,在一恒温、恒容密闭容器中充入1 mol N2和3 mol H2混合发生下列反应,其中断裂1mol H2需要吸收436 kJ的能量,断裂1 mol N2需要吸收945 kJ的能量,断裂1 mol N-H键吸收391 kJ的能量。
2NH3(g), 某同学为了探究氮气和氢气反应生成氨气,在一恒温、恒容密闭容器中充入1 mol N2和3 mol H2混合发生下列反应,其中断裂1mol H2需要吸收436 kJ的能量,断裂1 mol N2需要吸收945 kJ的能量,断裂1 mol N-H键吸收391 kJ的能量。
(1)写出NH3的电子式___________________ 。
(2)该反应________ (填“吸收”或“放出”)热量______________ 。
(3)当反应达到平衡时,N2和H2的转化率之比为____________ 。
 2NH3(g), 某同学为了探究氮气和氢气反应生成氨气,在一恒温、恒容密闭容器中充入1 mol N2和3 mol H2混合发生下列反应,其中断裂1mol H2需要吸收436 kJ的能量,断裂1 mol N2需要吸收945 kJ的能量,断裂1 mol N-H键吸收391 kJ的能量。
2NH3(g), 某同学为了探究氮气和氢气反应生成氨气,在一恒温、恒容密闭容器中充入1 mol N2和3 mol H2混合发生下列反应,其中断裂1mol H2需要吸收436 kJ的能量,断裂1 mol N2需要吸收945 kJ的能量,断裂1 mol N-H键吸收391 kJ的能量。(1)写出NH3的电子式
(2)该反应
(3)当反应达到平衡时,N2和H2的转化率之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液。完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为:__________________________
(2)已知燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-= CO32-+7H2O,这个电极是燃料电池的_____ (填“正极”或“负极”),另一个电极上的电极反应式为:______
(3)随着电池不断放电,电解质溶液的碱性_________ (填“增大”、“减小”或“不变”)
(4)通常情况下,甲烷燃料电池的能量利用率________ (填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率。
(1)甲烷与氧气反应的化学方程式为:
(2)已知燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-= CO32-+7H2O,这个电极是燃料电池的
(3)随着电池不断放电,电解质溶液的碱性
(4)通常情况下,甲烷燃料电池的能量利用率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)有① 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是________ (填编号,下同),互为同素异形体的是_________ 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要__________ (填“放出”或“吸收”)___________ kJ能量。
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是______ (填“A”或“B”),负极反应式为 ______________ 。

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为_______ ,(填化学式),负极反应式为______________
 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为
您最近一年使用:0次