1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是______ (用元素符号表示)。
②用电子式表示M2Z的形成过程_______ 。
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是_____ (写化学式)。
④GQ3溶液与过量的MZX溶液反应的化学方程式为________ 。
⑤常温下,不能与G的单质发生反应的是______ (填序号)。
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置_______ 。
②关于铷的下列说法中不正确的是________ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
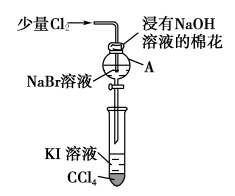
①棉花中浸有NaOH溶液的作用是___________________ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_______________ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________________ 。
(1)已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下均呈气态;Y的原子最外层电子数是其电子层数的2倍;M与X同族;Z、G分别是地壳中含量最高的非金属元素和金属元素。回答下列问题:
①Y、Z、M、G四种元素的原子半径由大到小的顺序是
②用电子式表示M2Z的形成过程
③上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是
④GQ3溶液与过量的MZX溶液反应的化学方程式为
⑤常温下,不能与G的单质发生反应的是
a.CuSO4溶液b.NaOH溶液c.Na2CO3固体d.氧化铁e.浓硝酸
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置
②关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
更新时间:2020-08-03 21:32:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学利用以下装置探究非金属元素性质的递变规律,并验证氯气的性质。
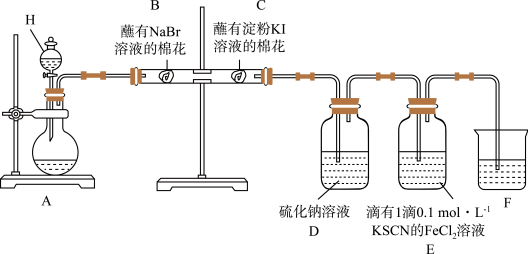
回答下列问题:
(1)仪器H的名称为_______ 。
(2)能说明氯气的氧化性强于溴的实验现象为_______ 。
(3)氯气进入D中,反应的离子方程式为_______ 。
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:a. 被氧化:b.
被氧化:b._______ ,设计实验方案验证以上假设,向褪色后的溶液中滴加_______ ,若观察到_______ ,可验证假设b成立。
(5)实验结束后,取出B处的棉花与另一个蘸有淀粉 溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。
溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。

回答下列问题:
(1)仪器H的名称为
(2)能说明氯气的氧化性强于溴的实验现象为
(3)氯气进入D中,反应的离子方程式为
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:a.
 被氧化:b.
被氧化:b.(5)实验结束后,取出B处的棉花与另一个蘸有淀粉
 溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。
溶液的棉花G接触,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填标号)。A.氧化性: | B.同主族元素从上到下非金属性减弱 |
| C.同周期元素从左到右非金属性减弱 | D. 对应含氧酸酸性逐渐减弱 对应含氧酸酸性逐渐减弱 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是元素周期表的一部分,回答下列问题:
(1)元素Ga在元素周期表中的位置为:第________ 周期第________ 族。
(2)Sn的最高正价为________ ,Cl的最高价氧化物对应的水化物的化学式为________ ,Bi的最高价氧化物的化学式为________ 。
(3)根据元素周期律,推断:
①最后一列部分元素氢化物热稳定性最高的是________ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________ H2SeO4(填“>”或“<”下同)。
(4)H2O2的电子式为_______________________ AS的原子结构示意图为__________________________
(5)3.01×1023个OH-含有质子的物质的量为________ mol,这些OH-和________ gNa+含有的电子数相同。
(6)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为________ ;
(7)等质量的SO2和SO3的物质的量之比________ ;氧原子个数比为________ ;
| B | C | N | O | F |
| Al | Si | P | S | Cl |
| Ga | Ge | As | Se | Br |
| In | Sn | Sb | Te | I |
| Tl | Pb | Bi | Po | At |
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①最后一列部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
(4)H2O2的电子式为
(5)3.01×1023个OH-含有质子的物质的量为
(6)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为
(7)等质量的SO2和SO3的物质的量之比
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】Ⅰ.如图为元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:
(1)元素①的一种核素中,含有1个质子和1个中子,该核素组成的符号是_______ 。
(2)上述元素中,金属性最强的是_______ (写元素符号)。其过氧化物中含有的化学键为_______ 。
(3)元素⑦的单质与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)④⑤⑥形成的简单离子半径由大到小的顺序为_______ (填离子符号);②③④简单氢化物的稳定性由强到弱的顺序为_______ (填化学式)。
Ⅱ.已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
(5)铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
(6)预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
(7)下列推断正确的是_______(填字母)。
| 族/周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ |
(2)上述元素中,金属性最强的是
(3)元素⑦的单质与元素⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)④⑤⑥形成的简单离子半径由大到小的顺序为
Ⅱ.已知Cs元素位于元素周期表中第六周期第ⅠA族,请回答下列问题:
(5)铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为(6)预测铯单质的还原性比钠单质的还原性
(7)下列推断正确的是_______(填字母)。
| A.与铯处于同一主族的元素都是金属元素 |
| B.铯单质发生反应时,铯原子易失去电子 |
| C.碳酸铯是一种可溶性碱 |
| D.铯离子的氧化性强于钾离子 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的学科,实验是检验化学理论正确与否的试金石。根据下列问题设计合适的实验:
(1)某同学为验证元素N、C、Si的非金属性依次减弱,设计了如图所示装置(已略去夹持装置),有同学认为这个装置不一定能证明C与Si的非金属性强弱,原因是___________ ,改进的方法为______________________ 。
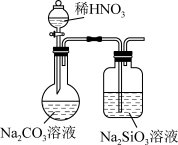
(2)若要证明非金属性:Cl>S,从下图 (仅略去夹持装置)中选取装置并按气流方向从左至右的连接顺序为___________ ,实验过程中可观察到的主要现象为___________ 。
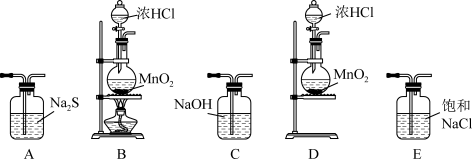
(3)根据(2)的实验方案,某同学认为把Cl2通入NaBr溶液中可证明非金属性:Cl>Br。这种方案__________ (填“能”或“不能”)达到预期目的,用化学方程式解释其原因:___________ 。
(1)某同学为验证元素N、C、Si的非金属性依次减弱,设计了如图所示装置(已略去夹持装置),有同学认为这个装置不一定能证明C与Si的非金属性强弱,原因是

(2)若要证明非金属性:Cl>S,从下图 (仅略去夹持装置)中选取装置并按气流方向从左至右的连接顺序为

(3)根据(2)的实验方案,某同学认为把Cl2通入NaBr溶液中可证明非金属性:Cl>Br。这种方案
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图___ ,R的简单离子的电子式___ 。
②X与Y元素可形成一种常用的消毒剂,其结构式为__ 。
③Y、Z、W、R形成的简单离子半径由大到小顺序为___ (用化学符号表示)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置___ 。
②关于铷的下列说法中不正确的是___ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
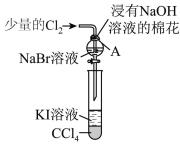
①棉花中浸有NaOH溶液的作用是___ (用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到___ ;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是____ 。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图
②X与Y元素可形成一种常用的消毒剂,其结构式为
③Y、Z、W、R形成的简单离子半径由大到小顺序为
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置
②关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①棉花中浸有NaOH溶液的作用是
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。
Ⅰ.上图是元素周期表的一部分,回答下列问题:
(1)⑧所对应的元素在周期表中的位置_______ 。
(2)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质的电子式_______ 。
(3)写出⑤的最高价氧化物对应的水化物与⑦的最高价氧化物反应的化学方程式_______ 。
(4)比较④与⑨的简单气态氢化物的稳定性_______>_______(填化学式)。______
Ⅱ.某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(5)实验①中反应的离子方程式是_______ 。
(6)实验②观察到的现象是_______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)⑧所对应的元素在周期表中的位置
(2)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质的电子式
(3)写出⑤的最高价氧化物对应的水化物与⑦的最高价氧化物反应的化学方程式
(4)比较④与⑨的简单气态氢化物的稳定性_______>_______(填化学式)。
Ⅱ.某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 | 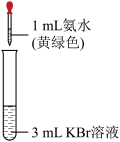 |  |
| 现象 | 溶液变为黄色 | _______ |
(6)实验②观察到的现象是
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子的价层电子排布式为 ;③R原子核外L层电子数为奇数;④Q、X原子p轨道上的电子数分别为2和4。请回答下列问题:
;③R原子核外L层电子数为奇数;④Q、X原子p轨道上的电子数分别为2和4。请回答下列问题:
(1)基态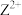 的核外电子排布式是
的核外电子排布式是______ 。
(2)Q、Y形成的最简单气态氢化物分别为甲、乙,则稳定性:甲______ (填“>”或“<”)乙。
(3)Q、R、Y三种元素的第一电离能由小到大的顺序为______ (用元素符号表示)
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物为______ (填化学式)。
 ;③R原子核外L层电子数为奇数;④Q、X原子p轨道上的电子数分别为2和4。请回答下列问题:
;③R原子核外L层电子数为奇数;④Q、X原子p轨道上的电子数分别为2和4。请回答下列问题:(1)基态
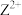 的核外电子排布式是
的核外电子排布式是(2)Q、Y形成的最简单气态氢化物分别为甲、乙,则稳定性:甲
(3)Q、R、Y三种元素的第一电离能由小到大的顺序为
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期元素A、B、C、D、E的原子序数依次增大,其中B和E同主族。A元素的最高正化合价和最低负化合价的绝对值之差为2;1 mol C单质与冷水反应,在标准状况下生成11.2 L H2;D原子最外层电子数等于其周期序数;E-的电子层结构与Ar原子相同。
(1)用元素符号表示各元素A________ 、B_________ 、C_________ 、D__________ 、E_________ ;
(2)能形成共价键的元素____________________ ;
(3)A的单质的电子式为______________ ;
(4)C和B形成化合物的电子式__________ ;
(5)写出C与水反应的离子方程式:_________________ 。
(1)用元素符号表示各元素A
(2)能形成共价键的元素
(3)A的单质的电子式为
(4)C和B形成化合物的电子式
(5)写出C与水反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的18e-分子。
(1)简单离子半径:Z>X>Y_______ ;
(2)X和Y的最简单氢化物的沸点:X>Y_______ 。
(1)简单离子半径:Z>X>Y
(2)X和Y的最简单氢化物的沸点:X>Y
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_____ ;N的简单离子的核外电子排布示意图为_____ 。
(2)用电子式表示化合物YN的形成过程:_____ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:_____ 。
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_____ (填字母)。
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:_____ 。
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。
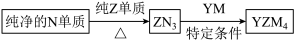
特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为_____ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_____ (填编号)。
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为_____ (用代数式表示)。
(1)Y在周期表中的位置是
(2)用电子式表示化合物YN的形成过程:
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。

特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】五种短周期元素A、B、C、D、E原子序数依次增大。B的最外层电子数是其电子层数的3倍;C、D、E的最高价氧化物对应水化物两两均可反应;A的单质在E的单质中能安静地燃烧,产生苍白色火焰。回答下列问题:
(1)B元素在元素周期表中的位置是____ ,B、C、D形成的简单离子的半径由大到小的顺序是____ (用化学符号表示)。
(2)B与C能形成一种淡黄色的固体,其电子式为____ ,它能用于呼吸面具的原因是____ (用其中一个化学方程式表示)。
(3)D的单质常用于焊接钢轨,请用化学方程式表示其反应原理____ 。D、E的最高价氧化物对应水化物之间发生反应的离子方程式为____ 。
(1)B元素在元素周期表中的位置是
(2)B与C能形成一种淡黄色的固体,其电子式为
(3)D的单质常用于焊接钢轨,请用化学方程式表示其反应原理
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。医学中常用QR溶液配制生理盐水。化合物乙由X、R两种元素组成。请回答下列问题:
(1)Z的离子结构示意图为_______________ ,由X、Z、Q三种元素组成的化合物中含有的化学键为___________________ 。
(2)Y元素的单质及其化合物能发生如图所示的转化,则Y元素为__________ (填元素符号)。在甲溶液中通入足量 气体,写出该反应的离子方程式:
气体,写出该反应的离子方程式:_________________________________ 。
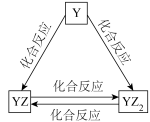
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。常温下,将W的单质和甲溶液混合,发生反应的离子方程式_________________________________ 。
(1)Z的离子结构示意图为
(2)Y元素的单质及其化合物能发生如图所示的转化,则Y元素为
 气体,写出该反应的离子方程式:
气体,写出该反应的离子方程式:
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。常温下,将W的单质和甲溶液混合,发生反应的离子方程式
您最近一年使用:0次



