制取氨气并完成氨气的性质实验。完成下列填空:
(1)写出实验室制氨气的化学方程式:__________ ;
(2)收集氨气应采用______ 法,要得到干燥的氨气可选用______ 做干燥剂;
(3)实验室制取少量干燥的氨气涉及下列装置,其中正确的是_________ ;
a.①是氨气发生装置 b.②是氨气吸收装置 c.③是氨气发生装置 d.④是氨气收集,检验装置

(4)用下图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发烧杯中溶液向上喷出的操作是______ ,除喷泉外还能观察到的实验现象是_______ 。
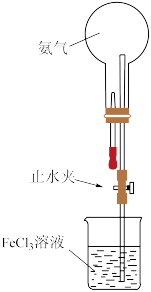
(5)某次实验收集的气体对氢气的相对密度为10,若将该烧瓶中的气体进行喷泉实验,进入烧瓶中的液体体积占烧瓶容积的体积分数是________ (已知空气的平均式量为29)。
(1)写出实验室制氨气的化学方程式:
(2)收集氨气应采用
(3)实验室制取少量干燥的氨气涉及下列装置,其中正确的是
a.①是氨气发生装置 b.②是氨气吸收装置 c.③是氨气发生装置 d.④是氨气收集,检验装置

(4)用下图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发烧杯中溶液向上喷出的操作是

(5)某次实验收集的气体对氢气的相对密度为10,若将该烧瓶中的气体进行喷泉实验,进入烧瓶中的液体体积占烧瓶容积的体积分数是
更新时间:2020-08-16 00:01:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)

请回答:
(1)实验室制备氨气的化学方程式为_____ 。
(2)收集氨气时,选择排空气法收集的理由为:_____ 。
(3)你选择的氨气的进气口为_____ (填“a”或“b"),并说明选择的理由_____ 。
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_____ 。
(5)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_____ (填序号)。


请回答:
(1)实验室制备氨气的化学方程式为
(2)收集氨气时,选择排空气法收集的理由为:
(3)你选择的氨气的进气口为
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(5)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置

(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”)____ 。
(2)写出制取氨气的化学方程式__________________________________ 。
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)__________ 。
(4)氨是一种重要的化工产品,其化学式为____________ ,具有______________ 气味,密度比空气_____________ 。

(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”)
(2)写出制取氨气的化学方程式
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)
(4)氨是一种重要的化工产品,其化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】肼(N2H4)又称联氨是一种重要的化工原料,易溶于水,具有强还原性;碱性条件下能与AgNO3溶液反应生成Ag和N2。回答下列问题:
I.联氨制备(夹持及加热装置已省略):
①氯气和氨气在丙酮中生成丙酮联氮[(CH3)2C=NN=C(CH3)2]且有白烟生成。
②丙酮联氮水解可得到丙酮和水合肼(N2H4•H2O)。
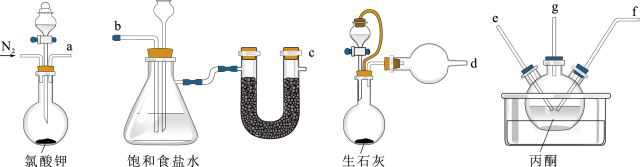
(1)按照接口顺序a→______→______→______→______←d进行实验___ ,反应前先通入一段时间的氮气排出空气,丙酮中生成丙酮联氮的化学方程式为____ 。
(2)盛放丙酮溶液的仪器名称为____ ,饱和食盐水中长颈漏斗的作用是___ ;反应过程中要控制氯气的通入量不能过量的原因是____ 。
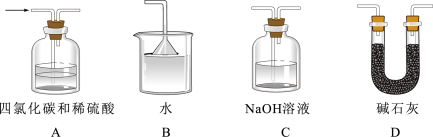
(3)装置存在明显缺陷,g后所接装置图可以是___ (填标号)。
II.产品纯度测定:
(4)量取水解液50.0mL加水调至弱碱性,配成250mL溶液,移出25.00mL,再加入足量AgNO3溶液;充分反应后,过滤、洗涤、干燥、称量,得固体质量为0.216g。则水解液中肼的含量为____ g•L-1。
I.联氨制备(夹持及加热装置已省略):
①氯气和氨气在丙酮中生成丙酮联氮[(CH3)2C=NN=C(CH3)2]且有白烟生成。
②丙酮联氮水解可得到丙酮和水合肼(N2H4•H2O)。

(1)按照接口顺序a→______→______→______→______←d进行实验
(2)盛放丙酮溶液的仪器名称为
(3)装置存在明显缺陷,g后所接装置图可以是

II.产品纯度测定:
(4)量取水解液50.0mL加水调至弱碱性,配成250mL溶液,移出25.00mL,再加入足量AgNO3溶液;充分反应后,过滤、洗涤、干燥、称量,得固体质量为0.216g。则水解液中肼的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
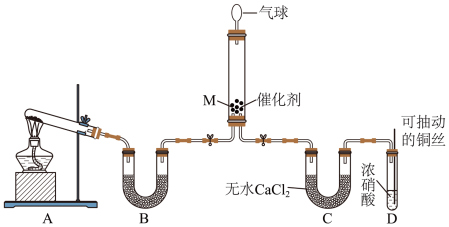
(1)用装置A制备NH3,反应的化学方程式为___________ ;装置B内的试剂是___________ 。
(2)装置D中发生反应的离子方程式是___________ ;可抽动铜丝的优点是___________ 。
(3)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为___________ 。
(4)如图是喷泉实验装置,在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有相同液体。下列组合能形成喷泉的是___________(填字母序号)。

(5)工业生产中利用氨水吸收少量SO2和NO2,原理如图所示,NO2被吸收过程的离子方程式是___________ 。
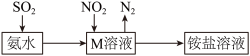

(1)用装置A制备NH3,反应的化学方程式为
(2)装置D中发生反应的离子方程式是
(3)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为
(4)如图是喷泉实验装置,在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有相同液体。下列组合能形成喷泉的是___________(填字母序号)。

| A.HCl与水 | B.Cl2与饱和氯化钠溶液 |
| C.SO2与NaOH溶液 | D.CO2与水 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组的同学利用下图所示实验装置进行 NH3 的制备、性质等实验。
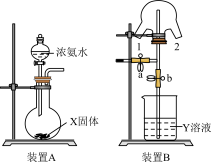
(1)装置 A 中的烧瓶内的 X 固体可选________
A.硫酸铜 B.氯化钙 C.五氧化二磷 D.生石灰
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,工业上也常用来检验氯气的管道是否漏气,请写出反应的化学方程式:___________
(3) 为防止环境污染, 以下装置( 盛放的液体均为水) 可用于吸收多余氨气的是_____
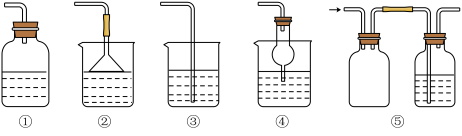
(4)有四个干燥的烧瓶,在常温常压下,向①瓶中装入干燥、纯净的氨气,②瓶中装入干燥的含一半空气的氨气,③瓶中装入干燥、纯净的二氧化氮,④瓶中装入干燥的体积比V(NO2):V(O2)=4∶1 的混合气体。做喷泉实验时四个烧瓶中所得溶液的物质的量浓度之比为(假设溶质不扩散)___________
A.2∶1∶2∶2 B.5∶5∶5∶4
C.1∶1∶1∶1 D.4∶4∶4∶5
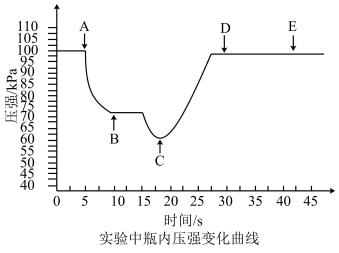
(5)可用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理:装置 A 与装置 B 相连,打开 a,关闭 b,开始实验,使三颈瓶内充满 NH3。将吸有 2 mL H2O 的胶头滴管塞进颈口 1,通过颈口 2 将数据采集器的探头插入三颈瓶中。打开 b,关闭 a,挤压胶头滴管,进行喷泉实验,电脑绘制三颈瓶内气压变化曲线如下图。该图中_______ 点时喷泉最剧烈。

(1)装置 A 中的烧瓶内的 X 固体可选
A.硫酸铜 B.氯化钙 C.五氧化二磷 D.生石灰
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,工业上也常用来检验氯气的管道是否漏气,请写出反应的化学方程式:
(3) 为防止环境污染, 以下装置( 盛放的液体均为水) 可用于吸收多余氨气的是
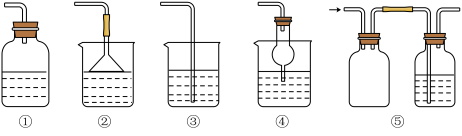
(4)有四个干燥的烧瓶,在常温常压下,向①瓶中装入干燥、纯净的氨气,②瓶中装入干燥的含一半空气的氨气,③瓶中装入干燥、纯净的二氧化氮,④瓶中装入干燥的体积比V(NO2):V(O2)=4∶1 的混合气体。做喷泉实验时四个烧瓶中所得溶液的物质的量浓度之比为(假设溶质不扩散)
A.2∶1∶2∶2 B.5∶5∶5∶4
C.1∶1∶1∶1 D.4∶4∶4∶5
(5)可用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理:装置 A 与装置 B 相连,打开 a,关闭 b,开始实验,使三颈瓶内充满 NH3。将吸有 2 mL H2O 的胶头滴管塞进颈口 1,通过颈口 2 将数据采集器的探头插入三颈瓶中。打开 b,关闭 a,挤压胶头滴管,进行喷泉实验,电脑绘制三颈瓶内气压变化曲线如下图。该图中

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氨气广泛应用于化工、轻工、化肥、制药、合成纤维等领域。同学们利用下图装置探究氨气的制备和性质。回答以下问题:
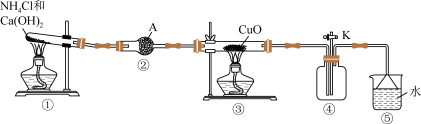
(1)装置①中反应化学方程式为_______ 。
(2)装置②中的A药品是_______ ;装置⑤的作用是吸收尾气,用倒扣水面上的漏斗代替直接插入水中的导管,其目的是_______ 。
(3)先加热装置①中的酒精灯,检验氨气已经充满整个装置的方法是:用玻璃棒蘸取漏斗口附近的溶液少许,_______ (补充完实验)。
(4)然后用酒精灯加热装置③,观察到黑色固体逐渐变红,预测固体产物有哪些可能?_______ 。装置④中气体仍为无色,利用装置设计实验证明没有产生NO,操作与现象是_______ 。据此分析,该实验的目的是检验NH3的_______ 性。

(1)装置①中反应化学方程式为
(2)装置②中的A药品是
(3)先加热装置①中的酒精灯,检验氨气已经充满整个装置的方法是:用玻璃棒蘸取漏斗口附近的溶液少许,
(4)然后用酒精灯加热装置③,观察到黑色固体逐渐变红,预测固体产物有哪些可能?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学清洗银镜实验后试管内壁上的银并探究其中的反应原理,进行下列实验。
(1)用稀硝酸可以清洗试管内壁上的银,反应的化学方程式为____________________________ 。
(2)为消除(1)中所产生的污染问题,改为如下实验。
①该同学由现象推测H2O2将Ag氧化为Ag+,但通过实验排除了这种可能性。他的操作及现象是:取实验I所得液体于试管中,_________________________________ 。
②经查阅资料,发现:实验I中银镜溶解后经一系列反应,最后产物为Ag,但是因为颗粒很小(直径在1~100 nm间)分散在液体中,肉眼无法识别。该同学设计实验,证实了a中存在直径在1~100 nm间的颗粒。他的操作及现象是:_____________________________________ 。
③写出实验I的化学方程式:_________________________________________________ 。
(3)进一步探究银的化合物在H2O2分解反应中的作用,进行如下实验。
①实验II的目的是___________________________________________________ 。
根据实验Ⅲ的现象提出假设:
假设1:Ag2O在H2O2分解反应中作氧化剂;假设2:Ag2O在H2O2分解反应中作催化剂。
②若假设1成立,请写出该反应的化学方程式:________________________________ 。
③结合所给试剂,请设计一个简单的实验证明假设1,并将表格填写完整。
可选试剂:1 mol·L-1盐酸、0.1 mol·L-1氨水、1 mol·L-1 NaOH溶液
(1)用稀硝酸可以清洗试管内壁上的银,反应的化学方程式为
(2)为消除(1)中所产生的污染问题,改为如下实验。
| 实验编号 | 操 作 | 现 象 |
I | 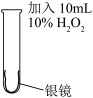 | 剧烈反应,有大量无色气体产生,该气体可以使带火星的木条复燃;反应停止后,试管内壁上的银全部溶解,得到澄清液体a。 |
②经查阅资料,发现:实验I中银镜溶解后经一系列反应,最后产物为Ag,但是因为颗粒很小(直径在1~100 nm间)分散在液体中,肉眼无法识别。该同学设计实验,证实了a中存在直径在1~100 nm间的颗粒。他的操作及现象是:
③写出实验I的化学方程式:
(3)进一步探究银的化合物在H2O2分解反应中的作用,进行如下实验。
| 实验编号 | 操 作 | 现 象 |
II | 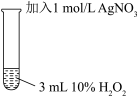 | 振荡,溶液无明显现象。 |
III |  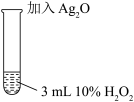 | 剧烈反应,产生大量无色气体,同时在试管底部仍有少量黑色固体。 |
根据实验Ⅲ的现象提出假设:
假设1:Ag2O在H2O2分解反应中作氧化剂;假设2:Ag2O在H2O2分解反应中作催化剂。
②若假设1成立,请写出该反应的化学方程式:
③结合所给试剂,请设计一个简单的实验证明假设1,并将表格填写完整。
可选试剂:1 mol·L-1盐酸、0.1 mol·L-1氨水、1 mol·L-1 NaOH溶液
| 实验步骤和操作 | 实验现象及结论 |
| 取3 mL 10% H2O2在试管中,加入少量Ag2O,充分反应后, |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】【变式探究】某化学兴趣小组利用如下装置制取氨气并探究氨气的有关性质。

甲
(1)图甲中,仪器A的名称是________ ,A中盛放的固体是________ 。
(2)已知单质B是空气中含量最多的成分,则玻璃管中发生反应的化学方程式为_________________ 。
(3)C装置的作用是______________ 。
(4)若按如图乙所示装置进行NH3性质实验。

乙
①先打开旋塞1,B瓶中的现象是____________ ,原因是_____________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________________ 。

甲
(1)图甲中,仪器A的名称是
(2)已知单质B是空气中含量最多的成分,则玻璃管中发生反应的化学方程式为
(3)C装置的作用是
(4)若按如图乙所示装置进行NH3性质实验。

乙
①先打开旋塞1,B瓶中的现象是
②再打开旋塞2,B瓶中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组设计实验探究氨催化氧化反应原理(忽略潮湿NH3与Na2O2的反应),装置如图所示。
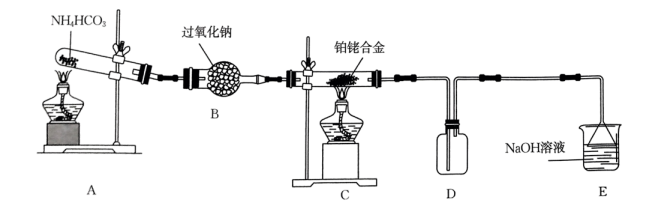
实验中观察到D中产生“白烟”。
回答下列问题:
(1)装置A中试管应向下倾斜,其原因是___________ 。
(2)装置E中倒置漏斗的作用是___________ 。
(3)装置B作用是___________ ,将铂铑合金粉末撒在玻璃丝上,其目的是___________ 。
(4)写出装置A中反应的化学方程式:___________ 。
(5)“白烟”的成分是___________ (填化学式)。
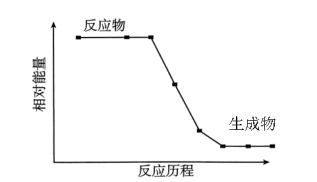
(6)实验测得装置C中主要反应的能量变化如图所示。该反应是___________ (填“放热”或”吸热”)反应。
(7)已知:装置B中有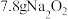 参与反应,则生成气体的体积是
参与反应,则生成气体的体积是___________ mL(标准状况)。

实验中观察到D中产生“白烟”。
回答下列问题:
(1)装置A中试管应向下倾斜,其原因是
(2)装置E中倒置漏斗的作用是
(3)装置B作用是
(4)写出装置A中反应的化学方程式:
(5)“白烟”的成分是
(6)实验测得装置C中主要反应的能量变化如图所示。该反应是

(7)已知:装置B中有
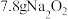 参与反应,则生成气体的体积是
参与反应,则生成气体的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知氨可以与灼热的氧化铜反应得到氮气和金属铜:3CuO+2NH3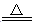 3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应。
3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应。
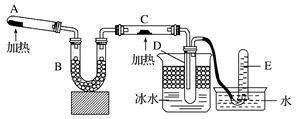
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是:____________________。
(2)B中加入的是碱石灰,其作用是___________________。
(3)D中收集到的物质是________,检验该物质的方法____________现象是___________________。
 3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应。
3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应。
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是:____________________。
(2)B中加入的是碱石灰,其作用是___________________。
(3)D中收集到的物质是________,检验该物质的方法____________现象是___________________。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产,某化学兴趣小组利用如图装置制备氨气并探究相关性质。

(1)该实验中A装置制备NH3不能用的药品是_______ 。
a.Ca(OH)2和NH4Cl的固体混合物 b.NH4Cl固体 c.NH4HCO3固体
(2)D装置后接尾气吸收装置,下列能用来吸收尾气的装置是_______ (填装置序号)。

(3)若将D与a相连,在E中产生白色沉淀,其化学式为:_______ 。若向a处分别通入_______ (填下列气体编号),在E中会产生另外一种白色沉淀。
a.Cl2 b.NO2 c.N2 d.CO2
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:_______ ;若充分反应后红色固体有剩余,再加入下列的_______ 试剂,
固体又可以继续溶解。
a.稀H2SO4 b.FeCl3溶液 c.FeCl2溶液 d.KNO3溶液
(5)将NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好),烧杯Z中盛装NaOH溶液(已知:2NO2+2NaOH=NaNO3+NaNO2+H2O),在一定温度下按如图装置进行实验。

①打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,红棕色气体慢慢变浅,生成一种无污染气体单质与一种常见物质。发生反应的化学方程式为_______ 。
②将注射器活塞退回原处并固定,待装置恢复到室温。打开K2,Z中NaOH溶液产生_______ 现象。
(6)利用(5)中装置探究SO2能否与Na2O2发生氧化还原反应。将Y中的药品更换为少量Na2O2,将注射器X中SO2缓慢推入Y中,Y装置中的现象为_______ 。

(1)该实验中A装置制备NH3不能用的药品是
a.Ca(OH)2和NH4Cl的固体混合物 b.NH4Cl固体 c.NH4HCO3固体
(2)D装置后接尾气吸收装置,下列能用来吸收尾气的装置是

(3)若将D与a相连,在E中产生白色沉淀,其化学式为:
a.Cl2 b.NO2 c.N2 d.CO2
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:
固体又可以继续溶解。
a.稀H2SO4 b.FeCl3溶液 c.FeCl2溶液 d.KNO3溶液
(5)将NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好),烧杯Z中盛装NaOH溶液(已知:2NO2+2NaOH=NaNO3+NaNO2+H2O),在一定温度下按如图装置进行实验。

①打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,红棕色气体慢慢变浅,生成一种无污染气体单质与一种常见物质。发生反应的化学方程式为
②将注射器活塞退回原处并固定,待装置恢复到室温。打开K2,Z中NaOH溶液产生
(6)利用(5)中装置探究SO2能否与Na2O2发生氧化还原反应。将Y中的药品更换为少量Na2O2,将注射器X中SO2缓慢推入Y中,Y装置中的现象为
您最近一年使用:0次


 收集氨气时,氨气的进气口是
收集氨气时,氨气的进气口是 ”或“
”或“ ”),理由是
”),理由是 ,继续通入氨气,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
,继续通入氨气,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是

