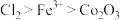有一混合溶液,其中只含有Fe2+、Cl-、Br-、I- (忽略水的电离),Cl-、Br-、I- 的个数比为2:3:4,向该溶液中通入氯气使溶液中Cl-和Br-的个数比为3:1,则通入氯气的物质的量与溶液中剩余Fe2+的物质的量之比为
| A.7:4 | B.7:3 | C.7:2 | D.7:1 |
9-10高三·湖北荆州·阶段练习 查看更多[33]
河南省鹤壁高中2021-2022学年高三上学期一轮复习第二次质量检测化学试题江西省九江市柴桑区第一中学2021-2022学年高三上学期第二次月考化学试题黑龙江省鹤岗市第一中学2020-2021学年高二6月月考化学试题安徽省池州市第一中学2021届高三上学期9月月考化学试题黑龙江省大庆中学2021届高三10月月考化学试题(已下线)江西省宜丰中学2018_2019学年高一化学上学期期末考试试卷吉林省白城市洮南市第一中学2021届高三上学期第一次月考化学试题天津市南开中学2020届高三第二次月考化学试题黑龙江省哈尔滨市第六中学校2021届高三上学期开学考试化学试题湖南师范大学附属中学2019-2020学年高二上学期入学考试化学试题湖南省长沙市湖南师范大学附属中学2019-2020学年高二上学期入学考试化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的综合分析(基础过关)2020届高考化学知识点必练——氧化还原反应的规律江西省宜春九中(外国语学校)2019-2020学年高一上学期第二次月考化学试题河南省鹤壁市淇滨高级中学2019-2020学年高一上学期期中考试化学试题江苏省常州市第一中学2019-2020学年高一上学期期中考试化学试题山西省晋中市平遥县第二中学2020届高三10月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第2讲 氯及其化合物 (题型专练)【全国百强校】山东省济南市历城第二中学2019届高三上学期11月调研检测化学试题江西省鹰潭市2017-2018学年高一上学期期末质量检测化学试题(已下线)2012届辽宁省铁岭中学高三上学期第三次月考化学试卷(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷2017届甘肃省天水一中高三上12月月考化学试卷2017届甘肃省天水一中高三上学期12月月考化学卷2017届江西省鹰潭一中高三上学期第二次月考化学试卷(已下线)2011届年山东省淄博市重点中学高三上学期期中考试化学试卷(已下线)2010年湖北省监利县一中2011届高三八月月考化学试题2016届甘肃省天水市第一中学高三上学期期中测试化学试卷2015届辽宁省丹东市高三总复习质量测试(一)理综化学试卷(已下线)2014届江西省师大附中高三上学期期中考试化学试卷(已下线)2014届江西省师大附中高三上学期期中考试化学试卷2014届河北省衡水中学高三上学期一调考试化学试卷(已下线)2010~2011学年河北省唐山一中高二下学期期末考试化学
更新时间:2020-08-20 13:36:05
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O有关判断正确的是
| A.氧化性:KMnO4<Cl2 |
| B.500mL12.8mol/L的盐酸与足量的KMnO4反应,可生成1.6 molCl2 |
| C.此反应中氧化剂与还原剂的物质的量之比为1︰8 |
| D.实验室使用硫酸而不用盐酸酸化高锰酸钾,因为盐酸会被高锰酸钾氧化 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知H2SO3+I2+H2O=H2SO4+2HI,将0.2 mol Cl2通入100 mL含等物质的量的HI与H2SO3的混合溶液中,有一半的HI被氧化,下列说法正确的是
| A.物质的还原性:HI>H2SO3>HCl |
| B.H2SO3的物质的量浓度为0.8 mol·L-1 |
| C.若再通入0.04 mol Cl2,则恰好能将HI和H2SO3完全氧化 |
D.通入0.2 mol Cl2发生反应的离子方程式为5Cl2+4H2SO3+2I-+16OH- =4SO +I2+10Cl-+12H2O +I2+10Cl-+12H2O |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是
| A.11:5 | B.5:6 | C.6:5 | D.11:6 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】将铜和镁的合金完全溶于浓HNO3溶液中,若反应中HNO3被还原产生4.48L(标准状况,下同)NO2气体和0.336 L N2O4气体,向反应后的溶液中加入足量的NaOH溶液,生成沉淀的质量为8.51g,则合金的质量为
| A.2.7g | B.4.6g | C.8.2g | D.无法计算 |
您最近半年使用:0次

 浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液
浓硫酸中加热,充分反应后锌完全溶解,同时生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液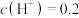
 和
和 的混合物
的混合物 、②
、② 、③
、③ 。下列有关说法正确的是
。下列有关说法正确的是 、
、 、
、
 生成,则被氧化的
生成,则被氧化的 为4个
为4个