下表为元素周期表的一部分,用元素符号或化学式 回答下列问题。
(1)10种元素中,化学性质最不活泼的是_____ , 除⑩外原子半径最大的是______ 。
(2)①③⑤三种元素最高价氧化物对应的水化物碱性最强的是____ ;⑧⑨形成氢化物的稳定性由强到弱顺序为_____ 。
(3)①②③⑤⑧五种元素形成的离子半径由大到小的顺序为_____ 。
(4)元素④的原子结构示意图是____ ,元素⑦的氢化物和元素①单质反应的化学方程式为_____ 。
(5)①⑨形成的化合物灼烧时火焰焰色为______ ;该化合物的溶液与元素⑧的单质反应的离子方程式为______ 。
(6)①、⑤和⑧最高价氧化物对应的水化物之间两两相互反应的离子方程式为________ 。
(7)元素③的单质在元素⑥⑦形成的某化合物中燃烧的化学方程式为_______ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10种元素中,化学性质最不活泼的是
(2)①③⑤三种元素最高价氧化物对应的水化物碱性最强的是
(3)①②③⑤⑧五种元素形成的离子半径由大到小的顺序为
(4)元素④的原子结构示意图是
(5)①⑨形成的化合物灼烧时火焰焰色为
(6)①、⑤和⑧最高价氧化物对应的水化物之间两两相互反应的离子方程式为
(7)元素③的单质在元素⑥⑦形成的某化合物中燃烧的化学方程式为
更新时间:2020-08-21 23:51:17
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型。A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态。
请回答下列问题(填空时用实际符号):
(1) C的元素符号是______________ ;元素F在周期表中的位置__________ 。
(2) B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物 B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为________ ,其固体时的晶体类型是____________________________ 。
(3) 最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如图所示,已知断裂lmolC-C吸收167kJ热量,生成1molC≡C放出942kJ热量。根据以上信息和数据,下列说法正确的是_______ 。

① C4属于一种新型的化合物
② C4沸点比P4(白磷)低
③ lmol C4气体转变为C2吸收882kJ热量
④ C4与C2互为同素异形体
⑤ C4稳定性比P4(白磷)差
⑥ C4属于原子晶体
⑦ C4和P4(白磷)的晶体都属于分子晶体
⑧ C4与C2互为同分异构体
(4) C与F两种元素形成一种化合物分子,各原子最外层达8电子结构,则该分子的结构式为__________ ,其空间构型为__________ 。
(5) 为了除去化合物乙(A2ED4)的稀溶液中混有的A2ED3,常采用A2D2为氧化剂,发生反应的离子方程式为:___________
(6) E与F形成的化合物E2F2在橡胶工业上有重要用途,遇水易水解,其空间结构与A2D2极为相似。对此以下说法正确的是______________ 。
a .E2F2的结构式为:F- E—E- F
b.E2F2为含有极性键和非极性键的非极性分子
c. E2Br2与E2F2结构相似,熔沸点:E2Br2> E2F2
d. E2F2与H2O反应的化学方程式可能为:2 E2F2+2H2O=EO2↑+ 3E↓+4HF
(7) 举出一种事实说明E与F的非金属性强弱(用化学方程式或用语言文字表达均可):
_________________________________________________________________
请回答下列问题(填空时用实际符号):
(1) C的元素符号是
(2) B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物 B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为
(3) 最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如图所示,已知断裂lmolC-C吸收167kJ热量,生成1molC≡C放出942kJ热量。根据以上信息和数据,下列说法正确的是

① C4属于一种新型的化合物
② C4沸点比P4(白磷)低
③ lmol C4气体转变为C2吸收882kJ热量
④ C4与C2互为同素异形体
⑤ C4稳定性比P4(白磷)差
⑥ C4属于原子晶体
⑦ C4和P4(白磷)的晶体都属于分子晶体
⑧ C4与C2互为同分异构体
(4) C与F两种元素形成一种化合物分子,各原子最外层达8电子结构,则该分子的结构式为
(5) 为了除去化合物乙(A2ED4)的稀溶液中混有的A2ED3,常采用A2D2为氧化剂,发生反应的离子方程式为:
(6) E与F形成的化合物E2F2在橡胶工业上有重要用途,遇水易水解,其空间结构与A2D2极为相似。对此以下说法正确的是
a .E2F2的结构式为:F- E—E- F
b.E2F2为含有极性键和非极性键的非极性分子
c. E2Br2与E2F2结构相似,熔沸点:E2Br2> E2F2
d. E2F2与H2O反应的化学方程式可能为:2 E2F2+2H2O=EO2↑+ 3E↓+4HF
(7) 举出一种事实说明E与F的非金属性强弱(用化学方程式或用语言文字表达均可):
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z是短周期主族元素,它们的核电荷数依次增大。下表列出它们的性质和原子结构:
(1)元素符号:X_______________ ,Z________________ 。
(2)Y元素原子的核外电子排布式为__________________ 。
(3)X元素原子的核外有_________ 种不同形状的电子云。
(4)Y元素的单质在W和X形成的化合物中反应的离子方程式为____________________ 。
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
(1)元素符号:X
(2)Y元素原子的核外电子排布式为
(3)X元素原子的核外有
(4)Y元素的单质在W和X形成的化合物中反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】四种短周期主族元素在元素周期表中的相对位置如图所示,X元素的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
(1)元素Y在周期表中的位置是第________ 周期________ 族。
(2)这四种元素最高价氧化物对应的水化物中,酸性最强的是_________ (填化学式,下同),碱性最强的是________ 。
(3)气体分子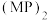 的电子式为
的电子式为_________ 。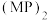 称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为__________ 。
M | P | ||
X | Y |
(1)元素Y在周期表中的位置是第
(2)这四种元素最高价氧化物对应的水化物中,酸性最强的是
(3)气体分子
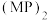 的电子式为
的电子式为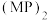 称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
称为拟卤素,性质与卤素类似,其与NaOH溶液反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
(1)D在元素周期表中的位置为____ 。
(2)AE2的结构式为____ 。
(3)C、E、F的简单氢化物中热稳定性最强的是____ (填化学式)。
(4)C、D、E、F的简单离子半径由大到小的顺序是____ (填离子符号)。
(5)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____ 。
| A | ||
| E |
(2)AE2的结构式为
(3)C、E、F的简单氢化物中热稳定性最强的是
(4)C、D、E、F的简单离子半径由大到小的顺序是
(5)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
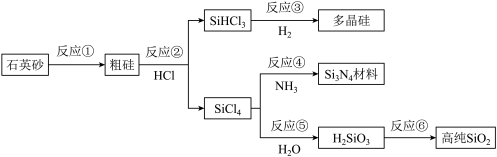
【推荐2】如图,通过工业联产可有效解决多晶硅(Si)生产中副产物SiCl4._______ 。
(2)反应①工业生产采用焦炭高温还原法制备,其化学方程式为_______ 。
(3)流程中涉及的化学反应属于氧化还原反应的有_______ (填反应序号)。
(4)高温下,反应④的化学方程式为_______ 。
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光导纤维的是_______ 。
(6)实验室不能使用玻璃塞的细口瓶装氢氧化钠,原因是_______ (用化学方程式表示)。
(7)Si和Ge属于同主族元素,下列预测合理的是_______ (填选项序号)。
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料
(2)反应①工业生产采用焦炭高温还原法制备,其化学方程式为
(3)流程中涉及的化学反应属于氧化还原反应的有
(4)高温下,反应④的化学方程式为
(5)在多晶硅、Si3N4材料和高纯SiO2中,可用于制造光导纤维的是
(6)实验室不能使用玻璃塞的细口瓶装氢氧化钠,原因是
(7)Si和Ge属于同主族元素,下列预测合理的是
a.Ge与H2化合难于Si
b.GeO2既有氧化性又有还原性
c.酸性H2GeO3>H2SiO3
d.Si和Ge都可做半导体材料
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】常见的短周期元素A、B、C、D、E的原子序数依次增大。常温下,A、C可形成A2C2和A2C两种液态化合物,B原子最外层电子数是次外层电子数的2倍,D原子电子层数与最外层电子数相等,E与C同主族。
(1)写出上述五种元素的元素符号;B._______ D._______ E._______ 。
(2)上述五种元素中,非金属性最强的是_______ (填写元素名称),最高价氧化物对应水化物酸性最强的是_______ (写化学式)。
(3)D的单质与第三周期A的同主族元素最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)B的单质与E的最高价氧化物对应水化物浓溶液反应的化学方程式为_______ 。
(5)由A2和C2形成的燃料电池中,用KOH做电解质溶液则负极发生的电极反应式为_______ ,正极发生了_______ (填氧化或还原)反应。
(1)写出上述五种元素的元素符号;B.
(2)上述五种元素中,非金属性最强的是
(3)D的单质与第三周期A的同主族元素最高价氧化物对应水化物反应的离子方程式为
(4)B的单质与E的最高价氧化物对应水化物浓溶液反应的化学方程式为
(5)由A2和C2形成的燃料电池中,用KOH做电解质溶液则负极发生的电极反应式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F为6种20号以前的元素,其核电荷数依次增大,A、B同周期,两者相隔一元素;B、E同主族相邻,A、B、E三种元素的核电荷数之和为30。C是所有短周期元素中金属性最强的元素,C、F能形成CF型化合物。元素D的最高价氢氧化物是两性氢氧化物。回答:
(1)写出各元素名称:A._______ ;B._______ ;C._______ ;D._______ ;E._______ ;F._______ 。
(2)A、E、F最高价氧化物对应的水化物酸性由强到弱的顺序:_______ (填化学式,下同)。C、D最高价氧化物对应的水化物碱性由强到弱的顺序:_______ 。
(3)比较A、B气态氢化物的稳定性:_______ 。比较E、F氢化物的还原性:_______ 。
(1)写出各元素名称:A.
(2)A、E、F最高价氧化物对应的水化物酸性由强到弱的顺序:
(3)比较A、B气态氢化物的稳定性:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】今年是门捷列夫发现元素周期律150周年。下表为元素周期表的一部分。
回答下列问题:
(1)Y元素在周期表中的位置为_________ ,其氢化物H2Y的稳定性__________ (填“>”或“<”)H2S。
(2)表中元素原子半径最大的是(填元素符号)_______ ,最高价氧化物对应的水化物酸性最强的是____________ (填化学式)。
(3)下列含碳化合物中互为同分异构体的是____________ 。
a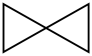 b
b 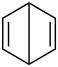 c
c d
d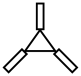
(4)写出W的最高价含氧酸的稀溶液与足量铁粉反应的离子方程式_____________ 。
(5)碳与镁可形成化合物M,若1molM与水反应生成2 mol Mg(OH)2和1mol烃N,N分子中碳氢质量比为9:1,N的电子式为_______ ;M与水反应的化学方程式为___________ 。
| 碳 | W | Y | |
| X | 硫 | Z |
回答下列问题:
(1)Y元素在周期表中的位置为
(2)表中元素原子半径最大的是(填元素符号)
(3)下列含碳化合物中互为同分异构体的是
a
 b
b  c
c d
d
(4)写出W的最高价含氧酸的稀溶液与足量铁粉反应的离子方程式
(5)碳与镁可形成化合物M,若1molM与水反应生成2 mol Mg(OH)2和1mol烃N,N分子中碳氢质量比为9:1,N的电子式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体。
⑤D的气态氢化物有臭鸡蛋气味。请写出:
(1)A元素的最高价氧化物的结构式_______
(2)C元素在周期表中的位置_______
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有_______
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为_______
(5)元素D与元素E相比,非金属性较弱的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ (填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物水溶液酸性比D的氢化物水溶液酸性强
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质。
(6)C分别与B、E形成的简单化合物中,熔沸点较高的是_______
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体。
⑤D的气态氢化物有臭鸡蛋气味。请写出:
(1)A元素的最高价氧化物的结构式
(2)C元素在周期表中的位置
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
(5)元素D与元素E相比,非金属性较弱的是
a.常温下D的单质和E的单质状态不同
b.E的氢化物水溶液酸性比D的氢化物水溶液酸性强
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质。
(6)C分别与B、E形成的简单化合物中,熔沸点较高的是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表列出了①~⑨九种元素在周期表中的位置。
回答下列问题:
(1)①~⑨九种元素中,化学性质最不活泼的是_______ (填元素符号)。
(2)元素②的原子结构示意图是_______ ,元素②与⑨组成的化合物中化学键类型为_______ (填“离子键”或“共价键”)。
(3)元素②和③中原子半径较大的是_______ (填元素符号)。
(4)元素③和④中气态氢化物稳定性较强的是_______ (填化学式)。
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是_______ (填化学式)。
(6)元素⑦的单质与⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①~⑨九种元素中,化学性质最不活泼的是
(2)元素②的原子结构示意图是
(3)元素②和③中原子半径较大的是
(4)元素③和④中气态氢化物稳定性较强的是
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是
(6)元素⑦的单质与⑥的最高价氧化物对应的水化物反应的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
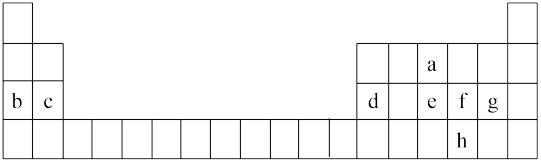
【推荐2】如图是元素周期表的一部分,表中所列字母分别代表一种元素。根据表中所列元素回答下列问题:_______ ,a的离子结构示意图是_______ 。
(2)h在元素周期表中的位置为_______ ,下列说法能证明元素f和h非金属性强弱的是_______ (填字母)。
a.比较两种元素简单阴离子的还原性
b.比较两种元素简单氢化物的热稳定性
c.比较两种元素单质的沸点
d.比较两种元素氧化物对应水化物的酸性
(3)元素e与元素b的最高价氧化物对应的水化物按计量数1∶2反应,写出反应的化学方程式_______ 。
(4)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。酸性:
_______  (填“>”或“<”),氧化镓与
(填“>”或“<”),氧化镓与 反应的离子方程式为
反应的离子方程式为_______ 。
(5)写出实验室制备g单质的离子方程式_______ 。
(2)h在元素周期表中的位置为
a.比较两种元素简单阴离子的还原性
b.比较两种元素简单氢化物的热稳定性
c.比较两种元素单质的沸点
d.比较两种元素氧化物对应水化物的酸性
(3)元素e与元素b的最高价氧化物对应的水化物按计量数1∶2反应,写出反应的化学方程式
(4)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。酸性:

 (填“>”或“<”),氧化镓与
(填“>”或“<”),氧化镓与 反应的离子方程式为
反应的离子方程式为(5)写出实验室制备g单质的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】1869年,俄国化学家门捷列夫制作了第一张元素周期表,如图是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
(1)元素b的一种核素可以测定文物年代,该核素是____ (填化学符号),e在元素周期表中所在的位置是____ 。
(2)a、c、d三种元素形成一种化合物的电子式为____ ,该化合物含有的化学键类型____ (填“离子键”、“极性键”、“非极性键”)。
(3)写出单质f与d的最高价氧化物对应水化物反应的离子反应方程式____ 。
(4)元素g、h、i的最高价氧化物对应水化物的酸性由强到弱的顺序为____ (用化学式表示)。
(5)元素c所在族元素的简单氢化物中沸点最高的是____ (填化学式),原因是____ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | h | i | ||||||||||||
| j |
(2)a、c、d三种元素形成一种化合物的电子式为
(3)写出单质f与d的最高价氧化物对应水化物反应的离子反应方程式
(4)元素g、h、i的最高价氧化物对应水化物的酸性由强到弱的顺序为
(5)元素c所在族元素的简单氢化物中沸点最高的是
您最近半年使用:0次



