Ⅰ.燃料电池是一种高效、环境友好的供电装置,下图是甲烷燃料电池原理示意图:
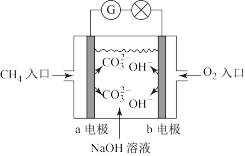
(1)a电极为__________ (填“正极”或“负极”),b电极发生_________ 反应(填“氧化”或“还原”);
(2)外电路中电子从b电极_________ (填“流入”或“流出”),内电路中OH-移向__________ 极(填”a”或”b”);
(3)写出该装置中负极上的电极反应式:________________________ 。
Ⅱ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
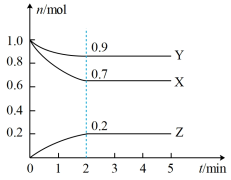
(4)图中对应的化学反应方程式为:________________________
(5)从开始至2min,Z的平均反应速率为____________ ;达到平衡状态时,X的转化率为____________
(6)将amolX与bmolY混合发生上述反应,反应到某时刻,各气体的物质的量恰好满足n(X)=n(Y)=2n(Z),则原混合气体中a:b=____________

(1)a电极为
(2)外电路中电子从b电极
(3)写出该装置中负极上的电极反应式:
Ⅱ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(4)图中对应的化学反应方程式为:
(5)从开始至2min,Z的平均反应速率为
(6)将amolX与bmolY混合发生上述反应,反应到某时刻,各气体的物质的量恰好满足n(X)=n(Y)=2n(Z),则原混合气体中a:b=
更新时间:2020-08-21 20:41:39
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】化学反应原理与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
求2~4min时间段以盐酸的浓度变化来表示的该反应速率为________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中等体积的下列溶液以减慢反应速率,你认为可行的是________ (填字母)。
A.蒸馏水 B.KNO3溶液 C.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
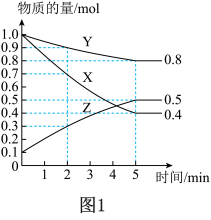
①该反应的化学方程式是_______ 。
②能判断该反应达到平衡状态的标志有_______ (填字母)。
A.Y在混合气体中的体积分数保持不变 B.X、Y的反应速率比为3:1
C.容器内气体密度保持不变 D.生成3molY的同时生成2molZ
③4min时,正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
④5min内Y的转化率为_______ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 200 | 480 | 928 | 1152 | 1240 |
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中等体积的下列溶液以减慢反应速率,你认为可行的是
A.蒸馏水 B.KNO3溶液 C.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②能判断该反应达到平衡状态的标志有
A.Y在混合气体中的体积分数保持不变 B.X、Y的反应速率比为3:1
C.容器内气体密度保持不变 D.生成3molY的同时生成2molZ
③4min时,正反应速率
④5min内Y的转化率为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)下列反应属于放热反应的是___________
A.铝片与稀H2SO4反应制取H2
B.碳酸钙高温分解成氧化钙和二氧化碳
C.葡萄糖在人体内氧化分解
D.氢氧化钾和硫酸中和
E.Ba(OH)2∙8H2O与NH4Cl固体反应
(2)一定条件下,某恒容密闭容器中充入SO2与O2反应,经5min后,若SO2和SO3物质的量浓度分别为2mol/L和5mol/L,则SO2起始物质的量浓度为___________ :用SO3表示这段时间该化学反应速率为___________ ,以下操作会引起化学反应速率变快的是___________ 。
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
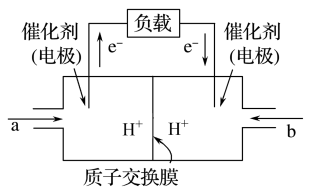
(3)如图是某笔记本电脑使用的甲醇空气燃料电池的结构示意图。放电时甲醇应从___________ 处通入(填“a”或“b”),电池内部H+向___________ (填“左”或“右”)移动,写出负极的电极反应式___________ 。
(1)下列反应属于放热反应的是
A.铝片与稀H2SO4反应制取H2
B.碳酸钙高温分解成氧化钙和二氧化碳
C.葡萄糖在人体内氧化分解
D.氢氧化钾和硫酸中和
E.Ba(OH)2∙8H2O与NH4Cl固体反应
(2)一定条件下,某恒容密闭容器中充入SO2与O2反应,经5min后,若SO2和SO3物质的量浓度分别为2mol/L和5mol/L,则SO2起始物质的量浓度为
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
(3)如图是某笔记本电脑使用的甲醇空气燃料电池的结构示意图。放电时甲醇应从

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】已知在某温度下2L的密闭容器中进行合成氨的反应,测得如表数据:
根据表中数据计算:
(1)若反应进行到2h时放出的热量为27.78 kJ,试写出该反应的热化学方程式___________
(2)0~1h内N2的平均反应速率为___________ mol•L﹣1•h﹣1。
(3)此温度下该反应第___________ 小时达到平衡,试计算达到平衡时N2的浓度___________ mol•L﹣1
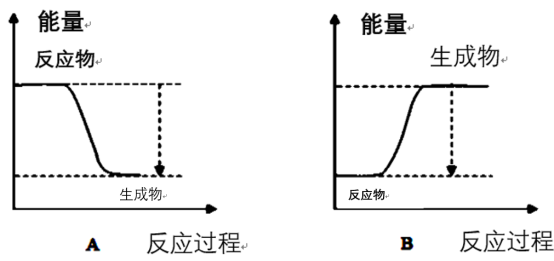
(4)下图能正确表示该反应中能量变化的是___________ (填“A”或“B”)。
(5)下列说法能说明该反应达到平衡状态的是___________ 。
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N﹣H键的同时生成2n mol H﹣H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
d.混合气体的物质的量不变
e.容器内的气体密度不变
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
根据表中数据计算:
(1)若反应进行到2h时放出的热量为27.78 kJ,试写出该反应的热化学方程式
(2)0~1h内N2的平均反应速率为
(3)此温度下该反应第
(4)下图能正确表示该反应中能量变化的是

(5)下列说法能说明该反应达到平衡状态的是
a.单位时间内生成2n mol NH3的同时生成3n mol H2
b.单位时间内生成6n mol N﹣H键的同时生成2n mol H﹣H键
c.用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
d.混合气体的物质的量不变
e.容器内的气体密度不变
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g);ΔH=-196.6kJ/mol。2min时反应达到化学平衡,此时测得反应物O2还剩余0.8mol。请填写下列空白:
(1)下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)
A.容器内压强不再发生变化B.SO2的体积分数不再发生变化
C.容器内气体质量不再发生变化D.容器内气体密度不再发生变化
(2)从反应开始至达到化学平衡,生成SO3平均反应速率为
(3)反应达到化学平衡后,以下操作将引起平衡向正反应方向移动并能提高SO2转化率的是
A.向容器中通入少量O2B.向容器中通入少量SO2C.使用催化剂D.降低温度E.向容器中通入少量氦气(已知氦气和SO2、O2、SO3都不发生反应)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】某温度下CO2加氢制甲醇的总反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:_______ (填“大于”“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)2 min末时v正_______ (填“<”“>”或“=”)v逆。
(3)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为_______ 。
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。 CO(g)+H2O(g)。
CO(g)+H2O(g)。
②_______ (用化学方程式表示)。
总反应可表示为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH_______ (填“>”或“<”)0。
 CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)(该反应为放热反应),在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。请回答: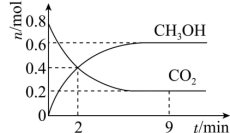
(2)2 min末时v正
(3)恒温恒容条件下,能说明反应已达平衡状态的是
A.混合气体的密度保持不变
B.消耗1molCO2的同时消耗1molCH3OH
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.CO2(g)体积分数保持不变
E.v(H2) = 3v(CH3OH)
(4)该反应平衡时H2的转化率为
(5)二氧化碳加氢制甲醇一般认为可通过两步反应来实现,物质变化与体系能量变化如题图所示。
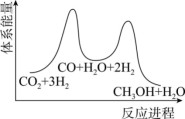
 CO(g)+H2O(g)。
CO(g)+H2O(g)。②
总反应可表示为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】CH4—CO2催化重整可以得到合成气(CO和H2),还可以减少温室气体的排放,该反应为:CH4(g)+CO2(g) 2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。
2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。
Ⅰ.回答下列问题:
(1)0~5min时间内用H2表示的化学反应速率为___ mol/(L•min)。
(2)达平衡时CH4的物质的量分数为___ ,CO2的转化率是___ 。
(3)反应前后混合气体的压强之比为___ 。
(4)为了加快反应速率,可采取什么措施___ (任意一条)。
(5)下列能表示该反应已经达到化学平衡状态的是___ 。
(6)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,则该燃料电池的负极的电极反应为:___ 。
 2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。
2CO(g)+2H2(g)。某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行重整反应,5min时达到平衡,测得CO的浓度为0.5mol/L。Ⅰ.回答下列问题:
(1)0~5min时间内用H2表示的化学反应速率为
(2)达平衡时CH4的物质的量分数为
(3)反应前后混合气体的压强之比为
(4)为了加快反应速率,可采取什么措施
(5)下列能表示该反应已经达到化学平衡状态的是
| A.v逆(CH4)=2v正(CO) |
| B.CO2的浓度保持恒定 |
| C.混合气体平均相对分子质量不变 |
| D.混合气体密度保持不变 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。
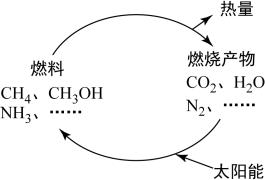
(1)在上图构想的物质和能量循环中太阳能最终转化为____________ 能。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g) 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。
一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
①用CH3OH表示0~3 min内该反应的平均反应速率为______________________ 。
②能说明该反应已达到平衡状态的是_______________ 。
a.v正(H2O)=2v逆(CO2)b.n(CH3OH) :n(O2)=2 :3
c.容器内密度保持不变d.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的____ 极(填“正”或“负”),通入氧气的一极的电极反应式为_______________ 。

(1)在上图构想的物质和能量循环中太阳能最终转化为
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)
 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如下表所示:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①用CH3OH表示0~3 min内该反应的平均反应速率为
②能说明该反应已达到平衡状态的是
a.v正(H2O)=2v逆(CO2)b.n(CH3OH) :n(O2)=2 :3
c.容器内密度保持不变d.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。
(1)在图构想的物质和能量循环中太阳能终化为___ 能。
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)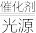 2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
①用CH3OH表示0~3min内该反应的平均反应速率为___ 。
②能说明该反应已达到平衡状态的是___ 。
A. 正(H2O)=2
正(H2O)=2 逆(CO2)
逆(CO2)
B.n(CH3OH):n(O2)=2:3
C.容器内密度保持不变
D.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的极___ (填“正”或“负”),通入氧气的一极的电极反应式为___ 。
(4)为了延长电池寿命,将锌锰干电池内的电解质NH4Cl换成湿的___ ,制成碱性锌锰电池。镍镉电池以Cd为负极,___ 为正极。

(1)在图构想的物质和能量循环中太阳能终化为
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)
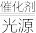 2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:| 间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
①用CH3OH表示0~3min内该反应的平均反应速率为
②能说明该反应已达到平衡状态的是
A.
 正(H2O)=2
正(H2O)=2 逆(CO2)
逆(CO2)B.n(CH3OH):n(O2)=2:3
C.容器内密度保持不变
D.容器内压强保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的极
(4)为了延长电池寿命,将锌锰干电池内的电解质NH4Cl换成湿的

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随有能量变化,能量、速率与限度是认识和研究化学反应的重要视角。
I.化学能与电能之间可以相互转化。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____
A.Ba(OH)2·8H2O与NH4Cl反应B.氢氧化钠与稀盐酸反应
C.灼热的炭与CO2反应D.H2与Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①电池的负极反应式为:___________________ 。
②电池工作时OH-向_________ 移动(填“正极”或“负极”)。
③正极上消耗标况下4.48L气体时,转移电子的数目为__________ 。
II.在2L绝热密闭容器中投入2molSO2和bmolO2,图是部分反应物随时间的变化曲线。
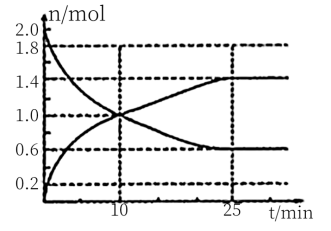
①10min时,v(SO3)=________ 。
②反应达到平衡时,SO2的转化率为______________ 。
③下列情况能说明该反应达到化学平衡的是______________ 。
A.v(SO3)=v(SO2)B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变D.混合气体的总物质的量不再改变
I.化学能与电能之间可以相互转化。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是
A.Ba(OH)2·8H2O与NH4Cl反应B.氢氧化钠与稀盐酸反应
C.灼热的炭与CO2反应D.H2与Cl2燃烧反应
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①电池的负极反应式为:
②电池工作时OH-向
③正极上消耗标况下4.48L气体时,转移电子的数目为
II.在2L绝热密闭容器中投入2molSO2和bmolO2,图是部分反应物随时间的变化曲线。

①10min时,v(SO3)=
②反应达到平衡时,SO2的转化率为
③下列情况能说明该反应达到化学平衡的是
A.v(SO3)=v(SO2)B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变D.混合气体的总物质的量不再改变
您最近一年使用:0次



